Enneaegse sünnituse ja enneaegse vastsündinu perinataalperioodi käsitlus (ajakohastatud)
Siinne ravijuhend on 2016. aastal valminud ravijuhendi „Enneaegse sünnituse ja enneaegse vastsündinu perinataalperioodi käsitlus“ ajakohastatud versioon.Ravijuhendi koostajad
| Pille Andresson (juht) | Lastearst, neonatoloogia osakonna juhataja, AS Ida-Tallinna Keskhaigla; Eesti Perinatoloogia Selts |
| Liis Toome | Lastearst, ravijuht, SA Tallinna Lastehaigla; Eesti Perinatoloogia Selts |
| Tuuli Metsvaht | Anestesioloog, lastekliiniku juht, SA Tartu Ülikooli Kliinikum; laste ja vastsündinute intensiivravi ja farmakoteraapia professor, Tartu Ülikool; Eesti Anestesioloogide Selts, Eesti Perinatoloogia Selts |
| Mari-Liis Ilmoja | Anestesioloog, AS Ida-Tallinna Keskhaigla; Eesti Anestesioloogide Selts |
| Aune Siller | Naistearst-õppejõud, SA Tartu Ülikooli Kliinikum; naistearst, AS Medita Baltics; õppejõud, Tartu Ülikool; Eesti Naistearstide Selts; STILEÜ; töörühma liige kuni juuli 2023 |
| Anne Rohtmets | Arst-õppejõud sünnitusabi ja günekoloogia alal, SA Tartu Ülikooli Kliinikum; (õppejõud) assistent, Tartu Ülikooli Naistekliinik; naistearst, AS LEH Võru Haigla; Eesti Naistearstide Selts; Eesti Arstide Liit; töörühma liige alates juuli 2023 |
| Kadi Ploom | Naistearst-juhtivarst, AS Ida-Tallinna Keskhaigla; Eesti Perinatoloogia Selts |
| Roksolana Goshka | Naistearst, naistehaiguste ja sünnitusabiosakonna vanemarst, SA Ida-Viru Keskhaigla; Eesti Naistearstide Selts; Eesti Perinatoloogia Selts |
| Birgit Suits | Lastearst, SA Pärnu Haigla, AS Ida-Tallinna Keskhaigla; Eesti Perinatoloogia Selts, Eesti Lastearstide Selts |
| Merilin Lumpre | Lastearst, SA Pärnu Haigla; Eesti Perinatoloogia Selts; Eesti Lastearstide Selts |
| Irena Bartels | Ämmaemandusjuht, AS Lääne-Tallinna Keskhaigla; Eesti Ämmaemandate Ühing |
| Svetlana Müürsepp | Vastutav õde, SA Tallinna Lastehaigla; Eesti Õdede Liit |
| Kristel Kukk | Patsientide esindaja, MTÜ Enneaegsed Lapsed |
Ravijuhendi sekretariaadi liikmed (2026)
| Liina Süvari (juht) | Lastearst, neonatoloog, AS Lääne-Tallinna Keskhaigla; Helsingi Ülikooli Haigla |
| Maarja Hallik | Anestesioloog, anestesioloogia ja intensiivravi keskuse juhataja, AS Ida-Tallinna Keskhaigla; anestesioloog, SA Tallinna Lastehaigla |
| Kadri Mägi | Arst-õppejõud sünnitusabi ja günekoloogia alal, SA Tartu Ülikooli Kliinikum; naistearst, Viljandi Haigla |
| Kristel Soonets | Arst-resident pediaatria erialal, SA Tartu Ülikooli Kliinikum |
| Triin Laaneleht | Naistearst, AS Ida-Tallinna Keskhaigla; naistearst, Tallinna Eriarstikeskus OÜ |
| Berit Lomp | Arst-resident pediaatria erialal, SA Tartu Ülikooli Kliinikum |
| Jana Rojak | Lastearst, neonatoloog, Päijät-Häme Keskhaigla, SA Tallinna Lastehaigla, AS Ida- Tallinna Keskhaigla |
| Anna Vesper | Metoodikanõunik, Tartu Ülikool; sekretariaadis kuni märts 2026 |
| Kadi Kallavus | Metoodik, Tartu Ülikool; sekretariaadis alates märts 2026 |
Ravijuhendi töörühma liikmed (2017)
| Pille Andresson (juht) | lastearst, EPS-i esindaja, TTK, ELS |
| Pille Vaas | naistearst, EPS-i esindaja, ENS |
| Aune Siller | naistearst, ENS-i esindaja, EPS |
| Kadi Ploom | naistearst, EPS-i esindaja |
| Jana Klementsov | naistearst, EPS-i esindaja, ENS |
| Ena Volmer | naistearst, EPS-i esindaja, ENS |
| Liis Toome | lastearst, ELS-i esindaja, EPS |
| Heili Varendi | lastearst, ELS-i esindaja, EPS |
| Birgit Suits | lastearst, EPS-i esindaja, ELS |
| Tuuli Metsvaht | anestesioloog, EAS-i esindaja, EPS, ELS |
| Vivian Arusaar | ämmaemand, EPS-i esindaja, TTK |
| Svetlana Müürsepp | õde, EÕL-i esindaja, EPS |
| Triinu Kalle | patsientide esindaja, MTÜ Enneaegsed Lapsed |
| Pille Teesalu | ämmaemand, EÄÜ esindaja, EPS |
Ravijuhendi sekretariaadi liikmed (2017)
| Anette Aija (juht) | neonatoloogia eriala arst-resident, EPS, ELS |
| Valeria Angioni | naistearst, EPS, ENS |
| Imbi Eelmäe | lastearst-anestesioloog, EPS, ELS, EAS |
| Reet Moor | lastearst, anestesioloogia eriala arst-resident, EPS, ELS |
| Anne Antson | lastearst, EPS, ELS |
| Maie Veinla | lastearst, EPS, ELS |
| Liisa Perk | günekoloogia ja sünnitusabi eriala arst-resident, ENS |
| Annemai Jallai (Noorkõiv) | günekoloogia ja sünnitusabi eriala arst-resident, ENS |
| Anna Vesper | metoodiline tugi |
Keeletoimetaja: Merily Šmidt
Tervisekassa esindaja: Silja Vanaisak
Lühendid ja mõisted
Lühendid
| AAP | American Academy of Pediatrics |
| ACOG | American College of Obstetricians and Gynecologists |
| AGA | gestatsioonivanusele vastav, ingl appropriate for gestational age |
| BiPAP | mitteinvasiivse ventilatsiooni režiim, kus opereeritakse kahe erineva rõhuga, st sissehingamisel on kasutusel kõrgem rõhk kui väljahingamisel, ingl Bi-level Positive Airway Pressure |
| BPD | bronhopulmonaalne düsplaasia, ingl bronchopulmonary dysplasia |
| CLD | krooniline kopsuhaigus, ingl chronic lung disease |
| CP | laste tserebraalparalüüs, ingl cerebral palsy |
| CPAP | pidev positiivne rõhk hingamisteedes, ingl continuous positive airway pressure |
| CRT | kapillaartäitumus, ingl capillary refill time |
| CRP | C-reaktiivne valk |
| EhhoKG | ehhokardiograafia, südame ultraheliuuring |
| ELBW | erakordselt väike sünnikaal, ingl extremely low birth weight |
| ELGA | erakordselt väike gestatsioonivanus, ingl extremely low gestational age |
| ERS | erütrotsüütide suspensioon |
| EvSu | tõendusmaterjali kokkuvõte, ingl evidence summary |
| FiO2 | hapniku osakaal sissehingatavas õhus, ingl fraction of inspired oxygen |
| GBS | B-grupi streptokokk, ingl group B streptococcus |
| GKS | glükokortikosteroid |
| GN | gestatsiooninädal ehk rasedusnädal |
| HF | mitteinvasiivne hingamistoetus, mida rakendatatakse suure peavooluga soojendatud ja niisutatud õhuga ja/või hapnikulisaga, ingl high-flow |
| IGFBP-1 | insuliinisarnast kasvufaktorit siduv proteiin 1, ingl insulin-like growth factor binding protein-1 |
| INSURE | INSURE meetod (intubatsioon, surfaktandi manustamine, ekstubatsioon), ingl INtubation-SURfactant- Extubation |
| IUGR | üsasisene kasvupeetus, ingl intrauterine growth restriction |
| IVH | intraventrikulaarne hemorraagia, ingl intraventricular hemorrhage |
| KKV | kopsude kunstlik ventilatsioon |
| KNS | kesknärvisüsteem |
| LBW | väike sünnikaal, ingl low birth weight |
| LISA | vähem invasiivne surfaktandi manustamine, ingl less invasive surfactant administration |
| MAP | keskmine arteriaalne vererõhk, ingl mean arterial blood pressure |
| NAVA | mitteinvasiivne sünkroniseeritud ventilatsioonimeetod, kus hingamistoetust reguleerib vahelihase elektriline impulss ja sissehingamine on abistatud reguleeritud rõhuga, ingl neurally adjusted ventilatory assist |
| NEK | nekrotiseeriv enterokoliit, ingl necrotizing enterocolitis |
| NHFOV | nina kaudu vahendatav kõrgsagedusventilatsioon, ingl nasal high frequency oscillatory ventilation |
| NICE | National Institute for Health and Care Excellence |
| NICU | vastsündinute intensiivravi osakond, ingl neonatal intensive care unit |
| NIDCAP | enneaegsete vastsündinute individuaalset arengut ja vajadusi arvestav hooldus, ingl newborn individualised developmental care and assessment programm |
| NIPPV | mitteinvasiivne positiivse rõhuga ventilatsioon, ingl nasal intermittent/non-invasive positive pressure ventilation |
| NIV | mitteinvasiivne ventilatsioon, ingl noninvasive ventilation |
| NSAID | mittesteroidsed põletikuvastased ravimid, ingl non-steroidal anti-inflammatory drugs |
| PAMG-1 | platsenta alfa-1-mikroglobuliin, ingl placental alphamicroglobulin-1 |
| PDA | avatud arterioosjuha, ingl patent ductus arteriosus |
| PEEP | positiivne ekspiratoorne lõpprõhk; positiivne rõhk hingamisteedes väljahingamise lõpul, ingl positive end- expiratory pressure |
| PICO | patsiendi-/sihtrühma-sekkumisvõrdluse tulemusnäitaja, ingl population/patient-intervention-comparison-outcome |
| PIP | inspiratoorne tipprõhk; maksimaalne rõhk hingamisteedes sissehingamisel, ingl peak-inspiratory pressure |
| PMV | postmenstruaalvanus |
| PPROM | lootevee puhkemine ajavahemikul 22+0–36+6 rasedusnädalat, ingl preterm premature rupture of membranes |
| PROM | lootevee puhkemine pärast 37. rasedusnädalat (alates 37+0), ingl premature rupture of membranes |
| PVL | periventrikulaarne leukomalaatsia, ingl periventricular leucomalacia |
| RCOG | Royal College of Obstetricians and Gynaecologists |
| RCT | juhuslikustatud kontrolluuring, ingl randomized controlled trial |
| RDS | respiratoorse distressi sündroom, ingl respiratory distress- syndrome |
| ROP | enneaegsuse retinopaatia, ingl retinopathy of prematurity |
| SGA | gestatsioonivanuse kohta väike, ingl small for gestational age |
| SI | prolongeeritud ehk pikendatud sissehingamisaeg, ingl sustained inflation |
| SoKo | soovituse kokkuvõtte tabel, ingl evidence to decision table |
| SpO2 | saturatsioon – perifeerse vere hemoglobiini hapnikuga küllastatus |
| TõKo | tõenduse kokkuvõtte tabel, ingl summary of findings table |
| VLBW | väga väike sünnikaal, ingl very low birth weight |
| VLGA | väga väike gestatsioonivanus, ingl very low gestational age |
Mõisted
| Apgari hinne | ühtlustatud hinnang vastsündinu seisundile esimesel, viiendal ja kümnendal eluminutil |
| Antenataalne periood | ajavahemik alates raseduskestusest 22+0 nädalat kuni sünd |
| Enneaegne sünnitus | regulaarsete emaka kokkutõmmete teke enne 37. rasedusnädala lõppu koos samaaegsete muutustega emakakaelas |
| Enneaegne vastsündinu (ingl preterm infant) |
ajavahemikul 22+0–36+6 rasedusnädalat sündinud laps |
| Enneaegse vastsündinu mõiste sünnikaalu järgi | |
| Väikese sünnikaaluga (LBW) vastsündinu | vastsündinu sünnikaaluga alla 2500 g |
| Väga väikese sünnikaaluga (VLBW) vastsündinu | vastsündinu sünnikaaluga alla 1500 g |
| Erakordselt väikese sünnikaaluga (ELBW) vastsündinu | vastsündinu sünnikaaluga alla 1000 g |
| Enneaegse vastsündinu mõiste gestatsioonivanuse järgi sünnil | |
| Hilisenneaegne vastsündinu | raseduskestuse korral 34+0–36+6 nädalat sündinud laps |
| Mõõdukalt enneaegne vastsündinu | raseduskestuse korral 32+0–33+6 nädalat sündinud laps |
| Väga väikese gestatsioonivanusega (VLGA) vastsündinu | raseduskestuse korral 28+0–31+6 nädalat sündinud laps |
| Erakordselt väikese gestatsioonivanusega (ELGA) vastsündinu | raseduskestuse korral 22+0–27+6 nädalat sündinud laps |
| Äärmiselt ebaküps vastsündinu | raseduskestuse korral 22+0–23+6 nädalat sündinud laps |
| Gestatsioonivanus | raseduskestus (loote vanus), mida arvutatakse ema viimase menstruatsiooni esimesest päevast nädalates ja päevades (nt 22 nädalat ja 0 päeva, väljendatakse 22+0) |
| Hiline surfaktantravi | surfaktandi manustamine kaks või enam tundi pärast sündi |
| Hingamistoetus | invasiivne – hingamistoetus, mida viiakse läbi alumistesse hingamisteedesse ulatuva hingamistee (intubatsioonitoru, trahheostoomia kanüüli) kaudu |
| mitteinvasiivne – hingamistoetus, mida viiakse läbi invasiivset hingamisteed (intubatsioonitoru, trahheostoomia kanüüli) kasutamata | |
| Inotroopne ravi | südamelihase jõudlust parandav ravi |
| Intranataalne periood | periood sünnitegevuse algusest kuni lapse sünnini |
| Kofeiinravi | kofeiintsitraat on valikravim enneaegsete apnoe farmakoloogiliseks raviks |
| Koorionamnioniit | lootekestade põletik |
| Känguruhooldus, ingl Kangaroo Mother Care | terviklik hooldusviis peamiselt enneaegsetele ja/või väikese sünnikaaluga imikutele, mis seisneb pikaajalises lapse-vanema nahakontaktis ning rinnapiimaga lapse toitmisel (ema oma või doonorpiim) ja lapse-vanema sideme tugevdamisel |
| Nabaväädi hiline sulgemine, ingl delayed cord clamping | nabaväädi sulgemine alates 60 sekundit pärast sündi |
| Nabaväädi lüpsmine | protseduur, mille käigus haaratakse õrnalt pöidla ja nimetissõrmega kinni kas sulgemata või läbilõigatud nabaväädist ning kaks kuni neli korda õrnalt surudes suunatakse veri kuni 25 cm pikkusest nabaväädist 15–20 sekundi jooksul vastsündinu poole |
| Nabaväädi varajane sulgemine, ingl early cord clamping | nabaväädi sulgemine kohe sünni järel, enne 30 sekundi möödumist |
| Nahakontakt, ingl skin-to-skin contact |
riieteta või mähkmega lapse asetamine vähemalt üheks tunniks lapsevanema paljale rindkerele või kõhule |
| Neonataal- ehk vastsündinuperiood | lapse 0.–28. elupäev |
| Normotermia | kehatemperatuur 36,5–37,5 °C |
| Oksügenisatsioon | kudede varustatus hapnikuga |
| Perekeskne ravi | vanemate kaasamine ja nende aktiivne osalemine lapse hooldus- ja raviprotsessis sünnijärgsel haiglaperioodil |
| Perinataalperiood | ajavahemik alates raseduskestusest 22+0 nädalat kuni vastsündinu esimese sünnijärgse elunädala lõpuni |
| Postmenstruaalvanus, ingl postmenstrual age | gestatsioonivanusele sünnil liidetud lapse sünnijärgne vanus |
| Preduktaalne saturatsiooninäit | perifeerne hemoglobiini hapnikuga küllastatuse näit mõõdetuna vastsündinu paremal käel |
| Proaktiivne ravi | aktiivne sekkumine perinataalperioodis, eesmärk on vastsündinu parem tervisetulem. Proaktiivse ravi all mõistetakse üldiselt antenataalset GKS-ravi, tokolüüsi, antibakteriaalset ravi, neuroprotektsiooni, keisrilõiget lootepoolsetel näidustustel, vastsündinu elustamist ja intensiivravi |
| Profülaktiline surfaktantravi | surfaktandi manustamine enneaegsele vastsündinule kohe sünnil, et vältida RDS-i teket või selle süvenemist |
| Prolongeerimine | sünnituse edasilükkamine |
| Prolongeeritud ehk pikendatud sissehingamisaeg, ingl sustained inflation |
esimestel hingetõmmetel kontrollitud rõhuga (20 cm H2O) pikem sissehingamisaeg, mida kasutatakse sünnil kopsude kiirema avanemise saavutamiseks |
| Perepalat vastsündinute intensiivravi osakonnas | palat, kus haiglasoleku ajal saab pere ööpäev läbi koos olla |
| Sünnituse induktsioon | sünnituse esilekutsumine vähemalt 22+0 GN-i kestnud raseduse korral ema- või lootepoolsetel näidustustel |
| T-kontuur | T-kujuline hingamiskontuur, mis võimaldab vastsündinu elustamisel rakendada kontrollitud rõhuga hingamistoetust |
| Toidutaluvus/ maojääk | kliiniliste sümptomiteta maojääk alla 4 ml/kg või alla 50% viimasest toidukorrast kolme tunni jooksul, ei ole vajadust vähendada toidukogust ega katkestada toitmist |
| Tokolüüs | sünnitustegevuse pärssimine ravimitega |
| Troofiline toitmine | enteraalne toitmine väikestes kogustes (10–15 ml/ kg päevas) ilma toidukoguseid suurendamata |
| Varajane enteraalne toitmine | enteraalse toitmise alustamine enne 6. elutundi |
| Varajane neonataalperiood | lapse 1.–7. elupäev |
| Varajane surfaktantravi | surfaktandi manustamine RDS-iga vastsündinule 1.–2. elutunnil |
| Vastsündinu | laps vanuses 0–28 elupäeva |
| Väljaõppe saanud meeskond | vastavat aparatuuri omav, intensiivravi väljaõppe ja kogemustega meeskond, kes osutab abi enneaegselt sündinud lapsele |
| Väga enneaegne vastsündinu | enne 32. GN-i sündinud laps |
| Üsasisene transport, ingl in utero transport | raseda transport enne lapse sündi kõrgema etapi haiglasse, et vältida vastsündinu sünnijärgset transporti |
Sissejuhatus
Enneaegseks sünnituseks nimetatakse regulaarsete emaka kokkutõmmete teket enne 37. GN-i koos samaaegsete muutustega emakakaelas. Sünnitus enne
34. GN-i on raseduse raske komplikatsioon. Vajalik on võimalikult täpselt ära tunda enneaegse sünnituse riskiga rasedad ja rakendada tänapäevasel teadusel põhinevaid ravivõtteid, nagu raseduse prolongeerimine ravimitega, sünnieelne glükokortikosteroidravi loote kopsude ettevalmistuseks, neuroprotektsioon loote/ lapse ebaküpse aju kaitseks ja antibakteriaalse ravi rakendamine rasedal vastavate näidustuste olemasolu korral, et parandada emade ja laste tervisetulemit.
Enneaegne sünd on üle maailma üks peamisi haigestumise ja surma põhjusi lastel varajases ja hilises neonataalperioodis ning imikueas. Vastsündinute suremus, tervise- ja arenguprobleemid on pöördvõrdelises sõltuvuses sünnikaalust ja gestatsioonivanusest sünnil. Meditsiini edusammud väga enneaegsena ehk enne 32. GN-i sündinud laste ravis on suurendanud elumust ja vähendanud vastsündinuea haigestumust.
Eesti Haigekassa tegi 2017. aasta lõpus Eesti Perinatoloogia Seltsile, Eesti Naistearstide Seltsile, Eesti Lastearstide Seltsile, Eesti Õdede Liidule ja Eesti Ämmaemandate Ühingule ettepaneku teha audit „Enneaegse sünnituse ja enneaegse vastsündinu perinataalperioodi käsitlus“. Auditi eesmärk oli kaardistada perinataalabi ravikvaliteet väga enneaegse sünnituse ja väga enneaegse vastsündinu ravikäsitluse korral ning hinnata väga enneaegsete laste ravitulemust Eestis aastatel 2015−2016 enne ravijuhendi rakendumist. Valim moodustati perioodil 01.01.2015–31.12.2016 Eestis toimunud elus- ja surnultsündidest raseduskestuses 22+0–31+6 GN-i. Vaadeldaval perioodil sündis Eestis 316 väga väikese gestatsioonivanusega last (2).
Auditi tulemused näitasid, et väga enneaegsete sündide osakaal kesk- ja üldhaiglates, kus puudub vastsündinute intensiivravi võimalus, oli alla 0,5%. See tähendab, et toimib regionaliseerimine: enneaegse sünnituse korral suunatakse enamikul juhtudel sünnitajad piirkondliku funktsiooniga haiglasse. Enamasti manustati väga enneaegsete sünnituste korral glükokortikosteroide (GKS). GKS-i manustamise osakaal väga enneaegsete sünnituste korral aastatel 2015−2016 ja 2020−2023 oli 96%, olles veidi kõrgem kui kohordis aastatel 2011–2012, kus GKS-i manustati 94,8%-l. GKS-i manustamine on märkimisväärselt suurenenud võrreldes aastatega 2002−2003 ja 2007−2008, mil GKS-i rakendamise osakaal oli vastavalt 73% ja 81% (3, 4).
1.jaanuarist 2020 kehtib Eestis uuendatud sünnikaart koos enneaegse vastsündinu lisakaardiga. Need võimaldavad analüüsida väga enneaegsete laste sündimust, perinataalset suremust, varast ja hilist neonataalset suremust ning suremust postmenstruaalvanuses (PMV) 44 nädalat või haiglaravi lõpul (sõltuvalt, kumb saabub varem), haigestumist esmasel haiglaravil, laste hilist tervist ja arengut ning ravi lähi- ja hilistulemit mõjutavaid tegureid (5).
Aastatel 2002–2016 Eestis korraldatud rahvastikupõhised uuringud, Eesti Haigekassa kliiniline audit ja sünniregistri andmed näitavad, et väga enneaegsena sündinud laste elumus on aja jooksul suurenenud, ulatudes 78%-ni aastatel 2002– 2003 ja 92,7%-ni aastatel 2020–2023 (2–5).
Lapse arengu ja tervise kaugprognoosi mõjutavate neonataalsete haiguste (bronhopulmonaalne düsplaasia, enneaegsuse retinopaatia, nekrotiseeriv enterokoliit ja intraventrikulaarne hemorraagia) sagedus on ajas vähenenud, kui võrrelda varasemate Eesti väga enneaegsete laste kohortide andmetega aastatest 2002–2003, 2007–2008 ja 2011–2012 (vt lisa 1). (2)
Rahvastikupõhised uuringud näitasid aastatel 2007 ja 2011–2012 vaatlusperioodi jooksul väga enneaegsena sündinutel kaheaastaselt tervise- ja arenguprobleemide vähenemist. EPICE uuringu andmetel oli Eestis tõsiste arenguprobleemidega laste osakaal Euroopa piirkondade keskmiste näitajatega sarnane või neist väiksem. (6, 7)
Enneaegsete vastsündinute ravi peaeesmärk on viia lapse edaspidist tervist ja arengut mõjutav vastsündinuea haigestumine miinimumini ning vältida raskete tüsistuste teket ja surma. Vähem invasiivsel ravitaktikal, mida on rakendatud esimestel elutundidel ja -päevadel, on seos laste suremuse ja vastsündinuea haigestumuse vähenemisega ning sellel on positiivne mõju laste hilisemale tervisele ja arengule.
Juurdunud on tõenduspõhiste ravivõtete kasutus. EPICE uuringus analüüsiti väga enneaegsete vastsündinute nelja tõenduspõhise ravitaktika (sünd kõrgema tasemega keskuses, sünnieelne glükokortikosteroidprofülaktika, hüpotermia ennetamine, surfaktantravi või hingamisteedes pideva positiivse rõhu rakendamine kahel esimesel elutunnil) mõju ravitulemile. Eestis oli kõiki nelja taktikat kasutatud 75,4%-l lastest, Euroopa kohordis keskmiselt 58,3%-l (eri piirkondades 32,1–75,5%-l) (4).
Enneaegne sünnitus ja sünd on suur tervishoiu kuluallikas. Vastsündinute intensiivravi on küll kallis, kuid hea ravikvaliteedi korral kulutõhus meditsiiniabi, kuna nimetatud patsiendirühma ootab ees palju kvaliteedile kohandatud eluaastaid. 2015.–2016. aastal analüüsiti tervishoiuteaduste võimekuse edendamise programmi
„Tervisetehnoloogiate hindamine“ raames väga väikeses gestatsioonivanuses sündinud laste ravitulemuse ja ravi kulutõhusust Eestis kolmel perioodil ajavahemikul 2002–2012. Analüüs näitas, et nii väga väikese kui ka erakordselt väikese gestatsioonivanusega (VLGA) laste elumuse paranemisega Eestis ei ole kaasnenud esmase haiglaravi pikenemist. Vähenenud on laste rehospitaliseerimine esimesel eluaastal, kuid mitte teisel eluaastal. Peamised hospitaliseerimise riskitegurid kahel esimesel eluaastal on meessugu ja haigused esmasel haiglaravil (8).
Eestis tehtud uuringute alusel on leitud, et VLGA-laste ravi kvaliteedi ja hilisema tervisetulemi parandamiseks on vaja perinataalse ja vastsündinute abi korraldust tõenduspõhiselt ajakohastada, järgida perinataalmeditsiini tõenduspõhiseid meetodeid, süstemaatiliselt koguda ja analüüsida haigete, sealhulgas enneaegsete vastsündinute terviseandmeid ning koostada riiklikke ravijuhendeid.
Ravijuhendi ajakohastamise vajadus
• glükokortikosteroidide täieliku või osalise skeemi efektiivsuse võrdlus üsasisese kasvupeetuse, koorionamnioniidi, raseda 1. ja 2. tüüpi diabeedi, rasedusaegse diabeedi korral vastsündinu parema ravitulemuse saavutamiseks loote kopsude ettevalmistamisel;
• rasedale magneesiumsulfaadi korduva manustamise vajadus (kui ravi alustamisest on möödunud 24 või enam tundi) ähvardava enneaegse sünnituse korral, et enneaegse vastsündinu ravitulemust parandada;
• raseduse prolongeerimise (rohkem kui 48 tundi) näidustus lootevee enneaegse puhkemisega ähvardava väga enneaegse sünnituse korral, et ema ja vastsündinu ravitulemust parandada;
• atosibaani või nifedipiini eelistamine tokolüüsi vajava ähvardava enneaegse sünnitusega rasedal ema ja vastsündinu parema ravitulemuse saavutamiseks;
• probiootikumide kasutamine enneaegsel vastsündinul ˂ 1500 g / ˂ 32+0 GN, et ravitulemusi parandada;
• A-vitamiini kasutamine enneaegsel vastsündinul ˂ 1500 g / ˂ 32+0 GN, et ravitulemusi parandada;
• südame ultraheliuuringu tegemine enne 72 elutundi või hiljem, et enneaegsel vastsündinul hemodünaamiliselt olulist arterioosjuha õigel ajal diagnoosida ja ravitulemust parandada;
• konservatiivse ravi (vedeliku piiramine, diureetikumid, mittesteroidsed põletikuvastased ained) või kirurgilise ravi kasutamine enneaegsel vastsündinul, et saavutada parem ravitulemus hemodünaamiliselt olulise arterioosjuha korral;
• valuskooringu kasutamise vajadus kõikidel enneaegsetel vastsündinutel, et ravitulemust parandada;
• farmakoloogilise ravi kasutamine, et ennetada valu invasiivsete ja valulike toimingute läbiviimisel enneaegsetel vastsündinutel;
• aju ultraheliuuringu rutiinse tegemise vajadus, et hinnata prognoosi ja parandada ravitulemusi enneaegsetel vastsündinutel.
Ajakohastatava ravijuhendi eesmärk on ühtlustada enneaegse sünnituse ja enneaegse vastsündinu perinataalperioodi kliinilise käsitluse põhimõtted Eestis, parandada nimetatud tervishoiuvaldkonnas perinataalabi ravikvaliteeti ning tagada tõenduspõhine tervishoiukorraldus.
Ravijuhendi käsitlusala ja sihtrühm
Ravijuhendi peamine sihtrühm on lastearstid, naistearstid, anestesioloogid- intensiivraviarstid, ämmaemandad, õed, patsiendid ja lapsevanemad.
Ravijuhendis ei ole käsitletud enneaegse sünnituse preventsiooni ega enneaegse vastsündinu haiguste diagnostikat ja ravi pärast esimest elunädalat. Proaktiivset tegevust (tokolüüs, antibiootikumravi alustamine, antenataalne kopsude ettevalmistus glükokortikosteroidiga) ähvardava enneaegse sünnituse korral saab alustada haiglatevahelise transpordi ajal, kui patsient suunatakse juba diagnoositud ähvardava enneaegse sünnitusega kõrgemasse etappi.
Ravijuhendi soovitustes lähtutakse tõenduspõhiste uuringute ja kliinilise praktika tulemustest, kuid need ei asenda vajadust kohaldada igale patsiendile sobivat lähenemist tema seisundi põhjal. Selles patsiendirühmas on vajalik individuaalne käsitlus. Ravijuhendis ei anta üksikasjalikku teavet konkreetsete ravimite kohta ja nende kasutamisel tuleb lähtuda ravimite omaduste kokkuvõtetest (www. ravimiamet.ee).
Ravijuhendi koostamine
Ravijuhendi ajakohastamiseks moodustati eri kutsealade esindajatest koosnev 12-liikmeline töörühm (koosseis on esitatud ravijuhendi alguses), kellest osa liikmeid kuulus ka algse juhendi töörühma. Ravijuhendi sekretariaati kuulus kaheksa liiget. Metoodilist nõu andis Tartu Ülikooli ravijuhendite püsisekretariaadi metoodikanõunik. Ravijuhendite Nõukoda kinnitas ravijuhendi töörühma ja sekretariaadi liikmete koosseisu 24. mail 2022 ja ravijuhendi käsitlusala 13. septembril 2022.
Ravijuhendi ajakohastamiseks vaatas töörühm läbi algse ravijuhendi koostamisel esitatud kliinilised küsimused ja neile vastamisel antud soovitused ning arutas uue tõendusmaterjali otsimise vajadust. Kui mõne kliinilise küsimuse kohta oli vahepealse viie aasta jooksul töörühma liikmete hinnangul suure tõenäosusega lisandunud uut tõenduspõhist infot, siis avati see küsimus, et otsida uut tõendusmaterjali. Kokku võttis töörühm arutelu alla algse juhendi 20 kliinilist küsimust ja esitas 11 uut kliinilist küsimust.
Enne ravijuhendi lõplikku kinnitamist retsenseerisid ravijuhendit välised eksperdid dr Heili Varendi, dr Kristiina Rull ja Piret Viiklepp ning ravijuhend läbis avaliku tagasisideringi. Pärast ravijuhendi kinnitamist ajakohastatakse seda uue olulise info lisandumisel või viie aasta pärast.
Kui juhendi ajakohastamisel läbi töötatud teaduslik jm tõendusmaterjal ei andnud põhjust muuta algses ravijuhendis antud soovitust, ajakohastati vaid soovituse sõnastust. Kui ajakohastatud ravijuhendis muudeti uue teadusliku tõendusmaterjali põhjal või muudel kaalutlustel soovituse sisu, tehti soovituse juurde märge „[AJAKOHASTATUD 2026]“. Kui koostati täiesti uus soovitus, siis lisati soovitusele märge „[UUS 2026]“.
Ravijuhendi käsitlusala, täistekst, tõendusmaterjali kokkuvõtte tabelid, soovituste koostamise tabelid, rakenduskava, ravijuhendi koostajate huvide deklaratsioonide kokkuvõte ja töörühma koosolekute protokollid leiab veebiaadressilt www. ravijuhend.ee.
Tõendusmaterjali otsimine ja hindamine
Pärast AGREE II struktureeritud instrumendiga hindamist kaasati ravijuhendi koostamisse 17 ravijuhendit.
1. NICE. Preterm labour and birth. NICE guideline [NG25] (2015, ajakohastatud 2022);
2. World Health Organization. WHO recommendations on interventions to improve preterm birth outcomes (2015);
3. Suomalainen Lääkäriseura Duodecim ja Suomen Gynekologiyhdistys. Ennenaikainen synnytys. Käypä hoito-suositus (2018);
4. Queensland Health. Queensland Clinical Guidelines. Preterm labour and birth. Guideline No. MN20.6-V9-R25 (2020);
5. NICE. Twin and triplet pregnancy (2019, ajakohastatud 2024)
6. Royal College of Obstetricians and Gynaecologists. Management of Breech Presentation. Green-top Guideline No. 20b (2017);
7. Royal College of Obstetricians and Gynaecologists. Care of Women Presenting with Suspected Preterm Prelabour Rupture of Membranes from 24+0 Weeks of Gestation. Green-top Guideline No. 73 (2019);
8. Royal College of Obstetricians and Gynaecologists. Prevention of Early-onset Neonatal Group B Streptococcal Disease. Green-top Guideline No. 36 (2017);
9. Royal College of Obstetricians and Gynaecologists. Antenatal corticosteroids to reduce neonatal morbidity and mortality. Green-top Guideline No. 74 (2022);
10. Queensland Health. Early onset Group B Streptococcal disease. Guideline No. MN22.20-V6-R27 (2022);
11. Queensland Health. Perinatal care of the extremely preterm baby. Guideline No. MN20.32-V2-R25 (2020);
12. European Resuscitation Council. Guidelines 2021: Newborn resuscitation and support of transition of infants at birth (2021);
13. American Heart Association. Part 5: Neonatal Resuscitation: 2020 Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care (2020);
14. NICE. Specialist neonatal respiratory care for babies born preterm. NICE guideline [NG124] (2019);
15. Queensland Health. Respiratory distress and CPAP. Guideline No. MN20.3- V9-R25 (2020)
16. European Consensus Guidelines on the Management of Respiratory Distress Syndrome (2019, ajakohastatud 2022);
17. NICE. Neonatal infection: antibiotics for prevention and treatment. NICE guideline [NG195] (2021, ajakohastatud 2024)
Kaasatud ravijuhendites vaadati läbi koostatava juhendi käsitlusalaga haakuvad soovitused, nende aluseks olnud teaduslik tõendusmaterjal ning muud soovituse suunda ja tugevust mõjutanud tegurid.
Tõendusmaterjali kokkuvõtte koostamiseks tehti lisaks süstemaatilised otsingud andmebaasis PubMed. Kaasati süstemaatilisi ülevaateid, metaanalüüse ja üksikuuringuid, eelistades jälgimisuuringutele juhuslikustatud kontrolluuringuid (RCT). Ravijuhendi koostamisel kasutatud teadusartiklid on juhendi tekstis viidatud.
Sekretariaat koostas iga kliinilise küsimuse kohta tõenduse kokkuvõtte (TõKo) tabeli ja valmistas ette soovituse kokkuvõtte (SoKo) tabeli, kasutades veebipõhist tarkvara GRADEpro. Peale huvipakkuva sekkumise kohta teadusuuringutest leitud kasu ja kahju ning tõendusmaterjali kvaliteedi kaalumist võttis töörühm kliinilise soovituse koostamisel arvesse ka patsientide eelistusi ja väärtushinnanguid, sekkumise vastuvõetavust kõigile sellega seotud osapooltele ja soovitusega kaasneda võivat patsientide ebavõrdsesse olukorda jätmist. Lisaks arvestati võimaluste ja ressurssidega (sh ravimite kättesaadavusega) soovitatava tegevuse rakendamiseks Eestis. Soovituste suuna ja tugevuse otsustas ning soovituse sõnastas töörühm üksmeelselt nii teadusliku tõendusmaterjali kui ka teiste eelnimetatud kriteeriumite põhjal. Kõik tabelid on kättesaadavad ravijuhendite veebilehel www.ravijuhend.ee.
Ravijuhendi käsikirjas on toodud soovituste juures analüüsitud tõendusmaterjali kokkuvõte ning töörühma arutelu tulemused. Kõik tabelid on kättesaadavad ravijuhendite veebilehel www.ravijuhend.ee.
Ravijuhendi soovitused
ANTENATAALNE PERIOOD
Enneaegse sünnituse diagnostika
| 1 |
Ähvardava enneaegse sünnituse diagnoosimise korral tehke rasedale emakakaela pikkuse hindamiseks transvaginaalne ultraheliuuring. |
|
| 2 |
Ähvardava enneaegse sünnituse sümptomitega rasedal, kellel on enne 34.+0 gestatsiooninädalat (GN-i) transvaginaalsel ultraheliuuringul emakakaela pikkus 15 mm või lühem, alustage tokolüüsi ja loote kopsude ettevalmistust glükokortikosteroidiga (GKS-iga). |
|
| 3 |
Lootevee enneaegse puhkemise kahtluse korral, kui lootevee eritumine ei visualiseeru, kaaluge rasedal insuliinisarnase kasvufaktorit siduva proteiin 1 määramist tupekaapest (Vag-IGFBP-1). |
Tsentraliseerimine
| 4 |
Ähvardava enneaegse sünnituse sümptomitega rase suunake vastavate ravivõimalustega kõrgema etapi keskusesse. Tugev positiivne soovitus, madal tõendatuse aste |
|
| 5 |
Ähvardava enneaegse sünnituse korral eelistage üsasisest transporti järgmiselt: • kui rasedus on kestnud 34+0–36+6 GN-i ja haiglas puudub lastearsti ööpäevaringne valve, transportige patsient keskhaiglasse või piirkondlikul tasemel sünnitusabi osutavasse haiglasse; • kui rasedus on kestnud 28+0–33+6 GN-i, transportige patsient Tallinnas või Tartus asuvasse keskhaiglasse või piirkondlikul tasemel haiglasse; • kui rasedus on kestnud 22+0–27+6 GN-i, transportige patsient piirkondlikul tasemel sünnitusabi osutavasse haiglasse. [AJAKOHASTATUD 2026] Praktiline soovitus |
Vastsündinu varajane transport
| 6 |
Enneaegse vastsündinu varast sünnijärgset transporti võimaluse korral vältige. Nõrk negatiivne soovitus, madal tõendatuse aste |
|
| 7 |
Enneaegse vastsündinu meditsiiniliseks transpordiks kasutage sellele spetsialiseerunud meeskonda. Tugev positiivne soovitus, madal tõendatuse aste |
Proaktiivne ravi (kui rasedus on kestnud 22+0–23+6 GN-i) (vt lisa 2)
| 8 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 22+0–22+6 GN-i, eelistage üsasisest transporti keskusesse. Nõrk positiivne soovitus, mõõdukas tõendatuse aste |
|
| 9 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 23+0–23+6 GN-i, kasutage üsasisest transporti keskusesse. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 10 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 22+0–22+6 GN-i, kaaluge antenataalset kopsude ettevalmistust GKS-iga. Nõrk positiivne soovitus, mõõdukas tõendatuse aste |
|
| 11 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 23+0–23+6 GN-i, kasutage antenataalset kopsude ettevalmistust GKS-iga. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 12 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 22+0–23+6 GN-i, kaaluge tokolüüsi. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 13 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 22+0–23+6 GN-i, kaaluge neuroprotektsiooni magneesiumsulfaadiga (vt lisa 2). Nõrk positiivne soovitus, mõõdukas tõendatuse aste |
|
| 14 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 22+0–22+6 GN-i, ärge tehke keisrilõiget lootepoolsete näidustuste tõttu. Tugev negatiivne soovitus, mõõdukas tõendatuse aste |
|
| 15 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 23+0–23+6 GN-i, ärge pigem tehke keisrilõiget lootepoolsete näidustuste tõttu. Nõrk negatiivne soovitus, mõõdukas tõendatuse aste |
Loote kopsude ettevalmistus
| 16 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 23+0–33+6 GN-i, kasutage antenataalset kopsude ettevalmistust GKS-iga. |
|
| 17 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 22+0–22+6 GN-i, kaaluge antenataalset kopsude ettevalmistust GKS-iga. Nõrk positiivne soovitus, mõõdukas tõendatuse aste |
|
| 18 |
Ähvardava enneaegse sünnituse korral kasutage antenataalseks loote kopsude ettevalmistuseks beetametasooni või deksametasooni. Annustamine: lihasesisesi beetametasooni 12 mg kaks annust 24-tunnise intervalliga või deksametasooni 6 mg neli annust 12-tunnise intervalliga. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 19 |
Rasedal, kes on saanud GKS-i esialgse kuuri seitsme või enama päeva eest, kuid kellel endiselt esineb enneaegse sünnituse risk enne 34.+0 GN-i järgneva seitsme päeva jooksul, kaaluge ühe GKS-i lisaannuse manustamist. |
|
| 20 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 23+0–33+6 GN-i, kaaluge GKS-i manustamist ka juhul, kui sünnitus toimub enne 24 tunni möödumist. |
|
| 21 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 34+0–36+6 GN-i, ärge pigem kasutage rutiinselt GKS-ravi. |
Loote neuroprotektsioon
| 22 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 24+0 –31+6 GN-i, kasutage rasedal loote neuroprotektsiooniks magneesiumsulfaati. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 23 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 32+0 –33+6 GN-i, kaaluge rasedal loote neuroprotektsiooniks magneesiumsulfaadi kasutamist. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 24 |
Ähvardava enneaegse sünnituse korral, kui sünnitus toimub tõenäoliselt järgmise 24 tunni jooksul, tuleks lootele neuroprotektsiooni alustada vähemalt 4 tundi enne sünnitust. Annustamine: veenisisesi 4–6 g magneesiumsulfaati boolusena 20–30 minuti jooksul ja edasi 1 g tunnis kuni sünnituseni maksimaalselt 24 tunni jooksul (vt lisa 3). Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 25 |
Ähvardava enneaegse sünnituse korral, kui sünnitus ei toimu 24 tunni jooksul pärast ravi alustamist ja enneaegse sünnituse oht tekib uuesti enne 32.+0 GN-i, kaaluge korduvat magneesiumsulfaadi manustamist. Praktiline soovitus |
Mikrobioloogilised uuringud rasedale
| 26 |
Ähvardava või käigusoleva enneaegse sünnituse korral kaaluge rasedal uriinikülvi tegemist. Praktiline soovitus |
|
| 27 |
Ähvardava enneaegse sünnituse korral võtke rasedalt B-grupi streptokoki (GBS) külv tupe alumisest kolmandikust ja rektumi piirkonnast; käigusoleva enneaegse sünnituse korral kaaluge kiirtesti Streptococcus agalactiae DNA tupekaapes (Vag-S agalactiae DNA). Tugev positiivne soovitus, madal tõendatuse aste |
|
| 28 |
Ähvardava või käigusoleva enneaegse sünnituse korral ärge tehke rasedal rutiinselt emakakaelakanalist külvi. Praktiline soovitus |
Antibakteriaalne ravi rasedale
| 29 |
Lootevee enneaegse puhkemiseta, bakteriaalse infektsiooni kliiniliste tunnusteta ähvardava enneaegse sünnituse korral ärge alustage rasedal antibakteriaalset ravi. Tugev negatiivne soovitus, mõõdukas tõendatuse aste |
|
| 30 |
Lootevee enneaegse puhkemisega ähvardava enneaegse sünnituse korral alustage antibakteriaalset ravi erütromütsiiniga, selle puudumise korral kasutage penitsilliini. Penitsilliiniallergia puhul kasutage klindamütsiini. Tugev positiivne soovitus, kõrge tõendatuse aste [RAKENDUSPIIRANG] |
|
| 31 |
Koorionamnioniidi puhul alustage laia toimespektriga või kombineeritud antibakteriaalset ravi, rasedust prolongeerimata (vt lisa 4). |
|
| 32 |
Vältige rasedal amoksitsilliini-klavulaanhappe kasutamist vastsündinu nekrotiseeriva enterokoliidi suurenenud riski tõttu. Tugev negatiivne soovitus, mõõdukas tõendatuse aste |
|
| 33 |
Enneaegse sünnituse ajal alustage rasedal GBS-i kandluse või teadmata GBS-i staatuse korral veenisisest profülaktilist antibakteriaalset ravi bensüülpenitsilliiniga. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
INTRANATAALNE PERIOOD
Sünnitusviisi valik
| 34 |
Enneaegse sünnituse korra ärge tehke keisrilõiget, kui loode on peaseisus ja keisrilõike ainuke näidustus on enneaegsus. |
|
| 35 |
Enneaegse sünnituse korral, kui rasedus on kestnud vähemalt 24.+0 GN-ini ja kui loode on tuharseisus, kaaluge keisrilõike tegemist. Nõrk positiivne soovitus, väga madal tõendatuse tase
|
|
| 36 |
Enneaegse kaksiksünnituse korral, kui esimene kaksik on peaseisus, eelistage vaginaalset sünnitust. Nõrk positiivne soovitus, väga madal tõendatuse aste
|
|
| 37 |
Enam kui kahe loote korral eelistage keisrilõike tegemist. Praktiline soovitus |
Episiotoomia
| 38 |
Enneaegse sünnituse korral ärge tehke rutiinselt episiotoomiat. Praktiline soovitus |
Raseduse prolongeerimine
| 39 |
Ähvardava enneaegse sünnituse korral, kui lootevesi on enneaegselt puhkenud ja raseduse kestus on lühem kui 34+0 GN-i, eelistage raseduse prolongeerimist, kui ei esine vastunäidustust (vt lisa 5). |
|
| 40 |
Lootevee enneaegse puhkemisega spontaanselt alanud sünnituse korral, kui raseduse kestus on 34+0–36+6 GN-i, ärge kasutage tokolüüsi. |
|
| 41 |
Ähvardava enneaegse sünnituse korral, kui lootevesi on enneaegselt puhkenud ja raseduse kestus on 34+0–36+6 GN-i, kaaluge induktsiooni. |
Tokolüüs (sünnitustegevuse pärssimine ravimitega)
| 42 |
Ähvardava enneaegse sünnituse korral kasutage tokolüüsi kuni 48 tundi loote kopsude ettevalmistuse, neuroprotektsiooni ja transpordi eesmärgil. Tugev positiivne soovitus, kõrge tõendatuse aste |
|
| 43 |
Ähvardava enneaegse sünnituse korral ärge kasutage tokolüüsi üle 48 tunni. Tugev negatiivne soovitus, kõrge tõendatuse aste |
|
| 44 |
Ähvardava enneaegse sünnituse korral ärge kasutage tokolüüsi järgmistes olukordades, kus raseduse prolongeerimine ei ole soovitatav: • surnud loode; • loote eluks sobimatu väärarend; • loote hüpoksia, mis vajab kohest sekkumist; • äge verejooks ja/või ema ebastabiilne hemodünaamika; • raske preeklampsia; • platsenta irdumine; • koorionamnioniit. Tugev negatiivne soovitus, kõrge tõendatuse aste |
|
| 45 |
Ähvardava enneaegse sünnituse korral kasutage tokolüüsiks valikravimina nifedipiini, kui puuduvad vastunäidustused selle ravimi kasutamiseks (vt lisa 5). Tugev positiivne soovitus, kõrge tõendatuse aste |
|
| 46 |
Ähvardava enneaegse sünnituse korral, kui tokolüüsiks on nifedipiini kasutamine vastunäidustatud, võib kasutada beetamimeetikumi (heksoprenaliin), oksütotsiini retseptori antagonisti (atosibaan), tsüklooksügenaasi inhibiitorit (indometatsiin). |
Nabaväädi sulgemine
| 47 |
Enneaegse vastsündinu sünni järel oodake nabaväädi sulgemisega võimaluse korral vähemalt 60 sekundit. |
|
| 48 |
Enneaegse vastsündinu nabaväädi sulgemisega ärge oodake, kui vastsündinu või ema vajab kohe elupäästvaid tegevusi. |
|
| 49 |
Enneaegsel vastsündinul, kes on sündinud pärast 28. GN-i, kaaluge nabaväädi lüpsmist kolm-neli korda, kui nabaväädi hiline sulgemine ei ole võimalik. |
|
| 50 |
Enneaegsel vastsündinul kaaluge hilist nabaväädi sulgemist ka juhul, kui ta vajab kohe sünni järel hingamistoetust (kui mõlemat saab teha samal ajal). |
ENNEAEGSE VASTSÜNDINU POSTNATAALNE PERIOOD
Kehatemperatuuri kontroll
| 51 |
Enneaegsel vastsündinul tagage seisundi esmase stabiliseerimise käigus normotermia. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
Esmane hingamistoetus
| 52 |
Enneaegsel vastsündinul, kes on sündinud enne 30.+0 GN-i ja kellel on respiratoorse distressi sündroomi (RDS-i) kujunemise risk, kasutage seisundi esmasel stabiliseerimisel mitteinvasiivset hingamistoetust (CPAP, NIV). Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 53 |
Enneaegse vastsündinu seisundi esmasel stabiliseerimisel kasutage võimaluse korral kontrollitud rõhuga hingamistoetust (Neopuff või muu T-kontuur või muu CPAP või NIV aparatuur). |
|
| 54 |
Spontaanhingamisel oleva enneaegse vastsündinu seisundi esmasel stabiliseerimisel kasutage CPAP-ravi korral hingamisteedes pidevat positiivset ekspiratoorset lõpprõhku vähemalt 5–6 cm H2O. |
|
| 55 |
Enneaegse vastsündinu seisundi esmasel stabiliseerimisel kontrollitud rõhuga ventileerimisel eelistage inspiratoorset tipprõhku (PIP) 20–25 cm H2O. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 56 |
Enneaegse vastsündinu seisundi esmasel stabiliseerimisel vältige pikendatud sissehingamisaja kasutamist. Nõrk negatiivne soovitus, madal tõendatuse aste |
|
| 57 |
Suurema gestatsioonivanusega enneaegsel vastsündinul võite individuaalse otsusena esmase hingamistoetusena kaaluda HF-i kasutamist. |
Esmane hingamistoetus (hapniku kontsentratsioon, FiO2)
| 58 |
Enneaegse vastsündinu esmasel stabiliseerimisel hingamistoetuse rakendamisel valige hapniku osakaalu algväärtus sissehingatavas õhus sõltuvalt gestatsiooninädalast sünnil: - alates 32+0 GN-i 21% hapnikku; - 28+0–31+6 GN-i 21–30% hapnikku; - enne 28 GN-i 30% hapnikku. |
|
| 59 |
Enneaegsel vastsündinul, kellel puudub efektiivne vereringe ja kui rakendatakse kaudset südamemassaaži, eelistage hapniku osakaalu sissehingatavas õhus 100%. |
Esmane hingamistoetus (saturatsioonipiirid, SpO2)
| 60 |
Enneaegsel vastsündinul, kes on sündinud enne 32.+0 GN-i, tiitrige hapniku kontsentratsioon sissehingatavas õhus, et pulssoksümeetril mõõdetuna parema käe randmel tõuseks saturatsioon (SpO2) viie minuti jooksul pärast sündi järkjärgult üle 80%. |
|
| 61 |
Enneaegsel vastsündinul hoidke hapnikravi kasutamisel SpO2 väärtused 90–95% juures. |
|
| 62 |
Enneaegse vastsündinu saturatsiooniväärtuse jälgimiseks võib kasutada FiO2-SpO2 automaatse korrigeerimise aparatuuri. Praktiline soovitus |
Profülaktiline surfaktantravi
| 63 |
Kõikidel enneaegsetel vastsündinutel ärge kasutage profülaktilist surfaktantravi. Tugev negatiivne soovitus, mõõdukas tõendatuse aste |
|
| 64 |
Kõikidele enne 30.+0 GN-i sündinud enneaegsetele vastsündinutele, kes vajavad esmase stabiliseerimise käigus intubatsiooni, manustage surfaktanti. |
Varajane CPAP-ravi ja varajane surfaktantravi
| 65 |
Kuni 30.+0 GN-il sündinud enneaegsel vastsündinul, kellel on hingamishäire ja kes ei vaja invasiivset hingamistoetust, alustage varast CPAP-ravi. Tugev positiivne soovitus, kõrge tõendatuse aste |
Surfaktantravi
| 66 |
Enneaegsel vastsündinul, kellel süvenevad RDS-i kliinilised tunnused ja FiO2 on > 0,3 CPAP hingamistoetusel rõhuga ≥ 6 cm H2O või kopsu ultraheliuuringu leid ennustabsurfaktandi vajadust, kasutage varast surfaktantravi. |
|
| 67 |
Mitteinvasiivsel hingamistoetusel oleval enneaegsel vastsündinul manustage surfaktanti peenikese kateetri teel. |
|
| 68 |
Enneaegsel vastsündinul kaaluga üle 1 kg võib alternatiivina manustada surfaktanti kõrimaski kaudu. |
|
| 69 |
RDS-iga enneaegsel vastsündinul kasutage eelistatult naturaalset surfaktanti (vt lisa 6). Tugev positiivne soovitus, kõrge tõendatuse aste |
|
| 70 |
RDS-iga enneaegsel vastsündinul kasutage võimalikult kontsentreeritud surfaktandipreparaati (poraktant alfa). Annustamine: poraktant alfa algannus 200 mg/kg, korduv annus 100 mg/kg. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 71 |
Enneaegsel vastsündinul, kelle RDS on raske kuluga ning püsib oluline lisahapniku ja/või invasiivse hingamistoetuse vajadus, on näidustatud surfaktandi korduv manustamine intervalliga vähemalt kuus tundi, kokku mitte rohkem kui kolm annust. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
Kofeiinravi
| 72 |
Enneaegsel vastsündinul kasutage kofeiinravi, et apnoed ennetada ja ravida ning invasiivsest hingamistoetusest võõrutada. |
|
| 73 |
Kõikidel enneaegsetel vastsündinutel, kes on sündinud enne 30.+0 GN-i, kasutage rutiinselt kofeiinravi. Alustage kofeiinravi nii vara kui võimalik, enne kolmandat elupäeva. |
|
| 74 |
Kõikidel enneaegsetel vastsündinutel, kellel esineb apnoe, kaaluge kofeiinravi kasutamist. |
|
| 75 |
Kõikidel enneaegsetel vastsündinutel annustage kofeiintsitraati järgmiselt: veeni või suu kaudu on soovituslik küllastusannus 20 mg/kg ööpäevas; säilitusannus 5–10 mg/ kg ööpäevas, mida võib suurendada apnoede püsimisel kuni 20 mg/kg-ni ööpäevas ühekordse annusena. [AJAKOHASTATUD 2026] Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 76 |
Enneaegsel vastsündinul postmenstruaalvanuses 33–35 nädalat kaaluge kofeiinravi lõpetamist, kui vastsündinu on kliiniliselt stabiilne. |
Hemodünaamika hindamise kriteeriumid
| 77 |
Enneaegse vastsündinu vereringet hinnake kompleksselt järgmiste koeperfusiooni näitajate alusel: jume, kapillaartäitumus, südamelöögisagedus, keskmine vererõhk, ajukoe regionaalne saturatsioon, diurees, happe-aluse tasakaal, laktaat. Ärge ravige enneaegse vastsündinu hüpotensiooni ainult vererõhu lävendist lähtudes. |
Hüpotensiooni, hüpoperfusiooni ravimeetodid
| 78 |
Vereringehäirega enneaegsele vastsündinule kaaluge südame- ja vereringepuudulikkuse põhjuse täpsustamiseks südame ultraheliuuringu tegemist. |
|
| 79 |
Enneaegsel vastsündinul ärge kasutage rutiinselt ringleva veremahu asendust ega vasoaktiivset ravi. |
|
| 80 |
Enneaegsel vastsündinul kaaluge hüpotensiooni ravi sõltuvalt põhjusest, kui ilmnevad hüpoperfusiooni tunnused: oliguuria, atsidoos, halb kapillaarne täituvus (vt lisa 7). |
|
| 81 |
Enneaegse vastsündinu hüpotensiooni/hüpoperfusiooni, mille põhjus on verekaotus või hüpovoleemia, ravige esmalt ringleva veremahu täitmisega 10 ml/kg, vajaduse järgi võib sama annust korrata. Massiivse verekaotuse korral jätkake esimesel võimalusel erütrotsüütide suspensiooni ja teiste verekomponentide ülekannetega massiivse transfusiooni põhimõtete alusel. |
Parenteraalne toitmine (vt lisa 8)
| 82 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g, keda ei ole võimalik toita piisavas mahus enteraalselt, eelistage parenteraalse toitmisega alustamist esimesel elupäeval, soovitatavalt esimestel elutundidel. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 83 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g eelistage glükoosi infusiooni alustada 4–8 mg/kg minutis (5,8–11,5 g/kg päevas) ja edaspidi juhinduge vere glükoosisisalduse jälgimisest. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 84 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g ärge kasutage hüperglükeemia ennetamiseks insuliini. Tugev negatiivne soovitus, madal tõendatuse aste |
|
| 85 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g eelistage alustada aminohapete lahuste manustamist võimalikult kiiresti sünni järel, hiljemalt 24 tunni vanuselt. Ohutu on alustada aminohapete pakkumist 2–2,5 g/kg päevas, suurendades järgnevatel päevadel valgukogust kuni annuseni 3,5 g/kg päevas. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 86 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g eelistage alustada lipiidide manustamist esimesel elupäeval. Soovitatav algannus on 1,0 g/kg päevas, edaspidi suurendada taluvuse korral lipiidide kogust annuseni 3,0 g/kg päevas. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 87 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g eelistage niisutatud kuvöösi tingimustes alustada vedeliku pakkumisega 70–80 ml/kg päevas, suurendades vedeliku pakkumist järk-järgult füsioloogiliselt. Enne 28.+0 GN-i sündinud enneaegsed vastsündinud võivad vajada rohkem vedelikku. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 88 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g korrigeerige vedeliku pakkumist individuaalselt, arvestades seerumi naatriumi kontsentratsiooni ja kaalulangust. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 89 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g pigem piirake esimestel elupäevadel naatriumi pakkumist, alustades sellega pärast diureesi vallandumist ning jälgides vedelikubilanssi ja elektrolüütide taset. Nõrk positiivne soovitus, madal tõendatuse aste |
Enteraalne toitmine (vt lisa 8)
| 90 |
Enneaegsel vastsündinul alustage enteraalset toitmist võimaluse korral oma ema rinnapiimaga, selle puudumisel doonoripiimaga, ema rinnapiima ja doonoripiima puudumisel enneaegsete piimaseguga. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 91 |
Enneaegsel vastsündinul, kes on sündinud enne 28.+0 GN-i, alustage minimaalset enteraalset toitmist esimesel elupäeval võimalikult vara, soovitatavalt esimestel elutundidel. Sobiv kogus ühel toidukorral on 1 ml/kg iga kahe-kolme tunni järel. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 92 |
Enneaegse vastsündinu enteraalse toitmise taluvuse korral suurendage toidu kogust 10–30 ml/kg ööpäevas. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 93 |
Enneaegse vastsündinu boolusena toitmise korral suurendage toidukogust 1 ml/kg 8–12 tunni järel. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 94 |
Enneaegse vastsündinu pideva toitmise korral suurendage toidukogust 0,5–1,0 ml/kg 8–12 tunni järel. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 95 |
Enneaegse vastsündinu rinnapiima rikastamist kaaluge alates toidukogusest 100 ml/kg ööpäevas. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 96 |
Enneaegsel vastsündinul, kes on sündinud enne 32.+0 GN- i, tagage täisenteraalsel toitmisel energiavajadus 110–130 kcal/kg ööpäevas ja valguvajadus 3,0–4,5 g/kg ööpäevas. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
Probiootikumid
| 97 |
Enneaegsel vastsündinul, kes on sündinud enne 34.+0 GN-i ja/või sünnikaaluga alla 1500 g, kasutage probiootikumi kohe koos toitmise alustamisega. |
|
| 98 |
Enneaegsel vastsündinul sünnikaaluga alla 1000 g kaaluge probiootikumi kasutamist. |
|
| 99 |
Kriitiliselt haigetel enneaegsetel vastsündinutel (baktersepsis, NEK) ärge kasutage probiootikumi. |
|
| 100 |
Enneaegsel vastsündinul lõpetage probiootikumi kasutamine pärast kuut nädalat või kojuminekul. |
|
| 101 |
Enneaegsel vastsündinul kaaluge kombineeritud probiootikumide preparaadi kasutamist, eelistatult B infantis Bb-02, B lactis Bb-12 ja Str thermophilus TH-4 annuses 3,0–3,5 × 108 pesa moodustavat ühikut (iga tüve kohta). |
A-vitamiin
| 102 |
Enneaegsele vastsündinule kaaluge A-vitamiini manustamist alates neljandast elupäevast suu kaudu või parenteraalse toitmise osana. |
Avatud arterioosjuha (vt lisa 9 ja 10)
| 103 |
Enneaegsel vastsündinul ärge kasutage avatud arterioosjuha ennetamiseks mittesteroidset põletikuvastast ravi (ibuprofeen, indometatsiin) ega paratsetamooli. |
|
| 104 |
Enneaegsel vastsündinul ärge forsseerige avatud arterioosjuha ennetamiseks diureesi (furosemiid, teofülliin). Tugev negatiivne soovitus, madal tõendatuse aste |
|
| 105 |
Enneaegsel vastsündinul vältige avatud arterioosjuha ennetamiseks liiga liberaalset vedeliku manustamist. |
|
| 106 |
Enneaegsel vastsündinul, kes on sündinud enne 28.+0 GN- i, kasutage sümptomaatilise ja/või hemodünaamiliselt olulise avatud arterioosjuha sulgemiseks ravi kõrges doosis ibuprofeeni (veeni või suu kaudu) või paratsetamooliga (vt annused lisas 9). Paratsetamooli eelistada patsientidel, kellel on vastunäidustus ibuprofeeni kasutamiseks (trombotsütopeenia, neerupuudulikkus). |
|
| 107 |
Enneaegsele vastsündinule tehke ehhokardiograafia, kui objektiivsete tunnuste alusel jääb hemodünaamiliselt olulise avatud arterioosjuha kahtlus. |
Antibakteriaalne ravi vastsündinule
| 108 |
Infektsiooni riskiteguritega enneaegsel vastsündinul kaaluge profülaktilist antibakteriaalset ravi (vt lisa 11). Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 109 |
Enneaegsel vastsündinul kasutage empiirilise antibakteriaalse ravi esmavalikuna penitsilliini (bensüülpenitsilliin või ampitsilliin) ja gentamütsiini kombinatsiooni (vt lisa 12). |
|
| 110 |
Enneaegse vastsündinu empiiriline antibakteriaalne ravi lõpetage 48–72 tunni pärast, kui puudub infektsioonile viitav kliiniline ja laboratoorne leid ning bakteriaalsed külvid on negatiivsed. Tugev positiivne soovitus, madal tõendatuse aste |
Valu hindamine ja valuravi
| 111 |
Enneaegse vastsündinu valu hindamiseks kasutage standarditud skooringut. Skooringu korrektseks rakendamiseks peavad kasutajad olema vastavalt koolitatud. |
|
| 112 |
Kõikidel enneaegsetel vastsündinutel (k.a invasiivsel või mitteinvasiivsel hingamistoetusel olevatel) ärge kasutage rutiinselt farmakoloogilist valuravi. |
|
| 113 |
Enneaegsel vastsündinul kasutage valuravi selektiivselt, lähtudes valuskooringu tulemustest ja planeeritava sekkumise iseloomust (vt lisa 13). |
Aju piltdiagnostika
| 114 |
Enneaegsel vastsündinul, kes on sündinud enne 32.+0 GN-i või kelle sünnikaal on < 1500 g, eelistage aju ultraheliskriiningut. |
|
| 115 |
Enneaegsele vastsündinule, kes on sündinud 32.+0–36.+6 GN-il, ärge pigem tehke aju ultraheliskriiningut (vt lisa 14). |
|
| 116 |
Enneaegsel vastsündinul, kes on sündinud 32.+0–36.+6 GN-il ja kellel kaasuvad enneaegsusega teised haigusseisundid või riskitegurid, eelistage aju ultraheliuuringut. Uuringu ajastus sõltub lapse seisundist (vt lisa 14). |
|
| 117 |
Enneaegsel vastsündinul, kes on sündinud enne 28. GN-i, kaaluge PMV-s 38–40 nädalat aju MRT uuringut. |
Perekeskne hooldus ja ravi (vt lisa 15 ja 16)
| 118 |
Enneaegse vastsündinu hoolitsust ja ravi kohandage individuaalselt, soodustades tema arengut ning kaasates, arvestades ja toetades peret. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 119 |
Enneaegse vastsündinuga perele tagage optimaalsed tingimused perekeskseks raviks (piiramata juurdepääs lapsele, vanemate ja personali koostöö, võimaluse korral perepalat, psühhosotsiaalne tugi). Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 120 |
Enneaegsel vastsündinul alustage vaginaalse sünnituse ja keisrilõike järel nahakontakti ema või isaga kohe pärast seisundi esmast stabilisatsiooni, kui vastsündinu seisund seda võimaldab. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 121 |
Enneaegse vastsündinu nahakontakti soodustage kogu haiglaravi jooksul, CPAP-ravi ja invasiivne hingamistoetus ei ole nahakontakti vastunäidustuseks. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 122 |
Enneaegse vastsündinu nahakontakti eelistage kestusega vähemalt üks tund korraga. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 123 |
Enneaegsel vastsündinul viige valulike vahelesegamiste arv miinimumini, kasutage valu ja stressi leevendamiseks mittefarmakoloogilisi võtteid. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
Ravijuhendi soovitused koos tõendusmaterjali lühikokkuvõtetega
Enneaegse sünnituse diagnostika
| 1 |
Ähvardava enneaegse sünnituse diagnoosimise korral tehke rasedale emakakaela pikkuse hindamiseks transvaginaalne ultraheliuuring. |
|
| 2 |
Ähvardava enneaegse sünnituse sümptomitega rasedal, kellel on enne 34.+0 gestatsiooninädalat (GN-i) transvaginaalsel ultraheliuuringul emakakaela pikkus 15 mm või lühem, alustage tokolüüsi ja loote kopsude ettevalmistust glükokortikosteroidiga (GKS-iga). |
|
| 3 |
Lootevee enneaegse puhkemise kahtluse korral, kui lootevee eritumine ei visualiseeru, kaaluge rasedal insuliinisarnase kasvufaktorit siduva proteiin 1 määramist tupekaapest (Vag-IGFBP-1). |
Ravijuhendi ajakohastamise käigus soovis töörühm teada, kas kõikidele ähvardava enneaegse sünnitusega (enne 35.+0 GN-i) rasedatele on näidustatud transvaginaalne ultraheliuuring. Teemakohaseid uuemaid allikaid ei leidunud, kuid 2022. aastal ajakohastatud NICE ähvardava enneaegse sünnituse ja sünni ravijuhendis soovitatakse emakakaela pikkust hinnata ultraheliuuringul, kui objektiivsel läbivaatusel on kahtlus ähvardavale enneaegsele sünnitusele (10). Ravijuhendite põhjal on diagnostiliselt täpseim emakakaela pikkuse hindamine transvaginaalsel ultraheliuuringul (10, 11). NICE ravijuhendisse kaasatud uuringute põhjal on ähvardava enneaegse sünnituse tõenäosus suurem, kui emakakaela pikkus on 15 mm või lühem. Sellisel juhul tuleb kaaluda terapeutilisi sekkumisi. Kui emakakaela pikkus on üle 15 mm, on enneaegne sünnitus järgmise 48 tunni jooksul ebatõenäoline (10).
Juhul, kui emakakaela pikkust ja avatust ei ole võimalik ultraheliuuringuga hinnata, võib kasutada digitaalset palpatsiooni. Vaginaalse ultraheliuuringu võimekuse puudumine ei ole näidustus patsiendi edasisuunamiseks kõrgemasse etappi. Lootevee enneaegse puhkemise kahtluse korral tuleb esmalt teha vaginaalne läbivaatus tupepeegliga. Kui lootevee eritumine ei ole nähtav, võib kasutada lootevee puhkemise kindlakstegemiseks insuliinisarnast kasvufaktorit siduva proteiin 1 määramist tupekaapes (Vag-IGFBP-1). Biomarkeri kontsentratsioon lootevees on kõrge ja lootevee puhkemisel saab seda tupesekreedist määrata. Positiivse testi korral tuleb arvestada patsiendi kliinilist pilti, anamneesi ja raseduse kestust, et otsustada võimalik terapeutiline sekkumine (10). Arvestada tuleb kliinilist pilti tervikuna, kasutades ultraheliuuringut abistava meetodina, et teha kindlaks patsiendid, kellel on enneaegse sünnituse risk suur, ning vältida ebavajalikke terapeutilisi sekkumisi patsientidel, kellel on enneaegse sünnituse risk väike.
Fibronektiini määramise kohta enneaegse sünnituse ennustamisel on uuringute tulemused varieeruvad. Suure negatiivse ennustusväärtuse tõttu on see olnud kasutusel eelkõige enneaegset sünnitust välistava testina (12, 13).
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K1 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 1 TõKo ja SoKo tabelit.
Tsentraliseerimine
| 4 |
Ähvardava enneaegse sünnituse sümptomitega rase suunake vastavate ravivõimalustega kõrgema etapi keskusesse. Tugev positiivne soovitus, madal tõendatuse aste |
|
| 5 |
Ähvardava enneaegse sünnituse korral eelistage üsasisest transporti järgmiselt: • kui rasedus on kestnud 34+0–36+6 GN-i ja haiglas puudub lastearsti ööpäevaringne valve, transportige patsient keskhaiglasse või piirkondlikul tasemel sünnitusabi osutavasse haiglasse; • kui rasedus on kestnud 28+0–33+6 GN-i, transportige patsient Tallinnas või Tartus asuvasse keskhaiglasse või piirkondlikul tasemel haiglasse; • kui rasedus on kestnud 22+0–27+6 GN-i, transportige patsient piirkondlikul tasemel sünnitusabi osutavasse haiglasse. [AJAKOHASTATUD 2026] Praktiline soovitus |
Tervise Arengu Instituudi juures töötava Eesti meditsiinilise sünniregistri (www. tai.ee) andmetel sündis Eestis 2024. aastal 544 enneaegset last, nendest elusana 528 last, mis on võrreldes 2019. aastaga 258 lapse võrra vähem. Kõikidest enneaegselt sündinud lastest sündis enne 32. gestatsiooninädalat (GN-i) 75 last (13,8%).
2017. aastal valminud algse ravijuhendi soovituste aluseks olid peamiselt retrospektiivsed kohortuuringud ja nende põhjal tehtud süstemaatilised ülevaated. Mitme uuringuga on tõestatud, et neonataalsed ravitulemused on paremad vastsündinutel, keda transporditi üsasiseselt (in utero), võrreldes nendega, keda transporditi sünni järel, eriti puudutab see enne 30.+0 GN-i sündinud lapsi (25– 27). Lastel, kes on sündinud enneaegselt väljaspool kõrgema etapi üksust, on suurem suremuse, III ja IV astme intraventrikulaarse hemorraagia (IVH), avatud arterioosjuha (PDA), RDS-i ja nosokomiaalse infektsiooni risk (15, 28–30).
Enneaegsetel vastsündinutel gestatsioonivanuses 22+0–28+6 GN-i võib sünd kõrgema etapi üksuses vähendada bronhopulmonaalse düsplaasia (BPD) teket. BPD tekkimise risk on suurem II astme osakondades võrrelduna kõrgema etapi intensiivravi osakondadega (31). Kohortuuringus, milles võrreldi enne 32.+0 GN-i sündinud või alla 1500 g kaalunud laste tervisetulemit, leiti, et madalama etapi haiglas sündinud ja ravitud lastel esines viie aasta vanuses rohkem enneaegsuse retinopaatiat (ROP), astmat, epilepsiat ja hüperkineetilist häiret (32).
Kõrgemas etapis jälgitud ja ravitud rasedate haigestumus ja suremus on väiksem ning üsasisene transport parandab vastsündinu tervisetulemit (19). Et tagada toimiv ja efektiivne haiglatevaheline infovahetus, on vaja luua optimaalne võrgustumine ja transpordiprotokollid. Efektiivse ravitulemuse saamiseks on ülioluline edastada info suunavalt arstilt kõrgema etapi raviasutuse arstile. Puudulik info edastamine on üks põhiline suboptimaalse ravi põhjus enneaegse sünnituse korral (33). Transpordi ajal peab olema tagatud ema ja loote seisundi jälgimine. Hinnata tuleb ema elulisi näitajaid (arteriaalne vererõhk, südamelöögisagedus, hingamissagedus, saturatsioon) ning emakakontraktsioonide ja loote südamelöökide sagedust. Üsasisese transpordi vastunäidustus on loote ja/või ema ebastabiilne seisund, mis võib kiiresti halveneda. Samuti ei transpordita sünnitajat avanemisperioodi aktiivses faasis, kui sünnitus on vältimatu (24).
Ravijuhendi ajakohastamise käigus avati kliiniline küsimus, et analüüsida vahepealsel ajal avaldatud uuemat tõendusmaterjali. Enamik tsentraliseerimist käsitlevast tõendusmaterjalist pärineb endiselt retrospektiivsetest kohortuuringutest ja nende põhjal tehtud süstemaatilistest ülevaadetest. Mitme uuringuga on tõestatud, et neonataalsed ravitulemused on paremad vastsündinutel, keda transporditi üsasiseselt (in utero), võrreldes nendega, keda transporditi sünni järel. On leitud, et perinataalse tsentraliseerimisega III astme vastsündinute intensiivravi osakonda on võimalik vähendada enneaegselt sündinud laste suremust. Neonataalne suremus oli statistiliselt suurem vastsündinutel, kes ei sündinud III astme vastsündinute intensiivravi osakonna kättesaadavusega haiglas, ja neonataalsel suremusel ei olnud vahet, kas rasedad olid hospitaliseeritud otse III astme vastsündinute intensiivravi võimalustega haiglasse või transporditud enne lapse sündi (34). Üsasisese transpordi teadlikkuse suurendamise ja järjepidevusega on võimalik parandada enneaegselt sündinud laste osakaalu haiglates, kus on olemas eeldused III astme intensiivraviks (35).
Väljaspool III astme vastsündinute intensiivravi osakonna valmidusega haiglat sündinud väga väikese sünnikaaluga lastel diagnoositi rohkem III ja IV astme IVH-d ning kopsuverejooksu. Märgatavat erinevust suremuses, I ja II astme IVH, periventrikulaarse leukomalaatsia (PVL), kroonilise kopsuhaiguse, ravi vajava ROP, nekrotiseeriva enterokoliidi (NEK), sepsise esinemises ega FiO2 erinevuses sünni järel ei leitud (36).
III astme vastsündinute intensiivravi osakonna valmidusega haiglas enne 28. GN-i sündinud laste tervisetulemid raske IVH, NEK, fokaalse soole perforatsiooni, kaugtulemina kognitiivsete häirete esinemise osas olid paremad. Suremuses statistiliselt olulist erinevust ei olnud (37).
Otsuse raseda edasisuunamise kohta teeb vastava haigla valves olev naistearst või patsiendi raviarst. Osal juhtudel soovitatakse edasisuunamine otsustada emakakaela avatuse või tuhude sageduse alusel, arvestada tuleb ka võimalikku tokolüüsi alustamist. Samuti tuleb arvestada, kas tegemist on esma- või korduvsünnitajaga. Üks edasisuunamise vastunäidustus on ka risk, et laps sünnib transpordivahendis.
Töörühma hinnangul peab neonataalses intensiivravi osakonnas olema võimekus ravida enneaegseid vastsündinuid alates 22.+0 GN-ist. Meeskonnas peavad olema lisaks lasteanestesioloogile lastekardioloog, lastekirurg ja lasteneuroloog. Enam on ohustatud enneaegsed vastsündinud, kes on sündinud 22.–24. GN-il. Eesti mahtu on keeruline võrrelda teiste riikidega, teiste riikide uuringute tulemusi ei saa otseselt Eesti konteksti üle võtta.
Töörühma soovituste aluseks on lisaks tõendusmaterjalile Eesti meditsiinilise sünniregistri perinataalne statistika ning viimasel aastakümnel Eestis tehtud uuringud väga enneaegsete sünnituste ja vastsündinute ravitulemuste kohta (vt lisa 1).
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K2 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 2 TõKo ja SoKo tabelit.
Vastsündinu varajane transport
| 6 |
Enneaegse vastsündinu varast sünnijärgset transporti võimaluse korral vältige. Nõrk negatiivne soovitus, madal tõendatuse aste |
|
| 7 |
Enneaegse vastsündinu meditsiiniliseks transpordiks kasutage sellele spetsialiseerunud meeskonda. Tugev positiivne soovitus, madal tõendatuse aste |
Ravijuhendi ajakohastamisel avati algse juhendi kliiniline küsimus, et analüüsida uuemat tõendusmaterjali. Tsentraliseerimisel on tähtis osa enneaegselt sündinud laste tervisetulemis. Enamik seda teemat käsitlevast tõendusmaterjalist pärineb retrospektiivsetest kohortuuringutest. On leitud, et enne 32. GN-i sündinud laste transport esimese 72 tunni jooksul suurendab III ja IV astme IVH esinemist. Eriti on ohustatud enne 28. GN-i sündinud enneaegsed vastsündinud, kes vajavad esimese 72 tunni jooksul transporti III astme intensiivravi osakonda (46).
Soome riigiüleses uuringus leiti, et enne 28. GN-i sündinud enneaegsetel vastsündinutel, kes transporditi sünni järel III astme vastsündinu intensiivravi osakonna valmidusega haiglasse, esines rohkem rasket ajukahjustust võrreldes kontrollrühmaga (47).
Tuntavalt väheneb enneaegsete vastsündinute suremus, kui vastsündinu esmane adekvaatne stabiliseerimine ja ravi on tagatud kohas, kus toimub sünnitus (48). Kui vastsündinu transport on vältimatu, peab patsiente transportima spetsiaalne meeskond, kellel on vastsündinu transpordiks ette nähtud varustus, väljaõpe ja kogemus (38, 48). Lähtudes eeldatavast patsiendi kasust, on töörühma hinnangul tegu tugeva soovitusega ning soovitusi ei ole vaja muuta.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K22.
Proaktiivne ravi (raseduskestuse korral 22+0–23+6 GN-i) (vt lisa 2)
| 8 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 22+0–22+6 GN-i, eelistage üsasisest transporti keskusesse. Nõrk positiivne soovitus, mõõdukas tõendatuse aste |
|
| 9 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 23+0–23+6 GN-i, kasutage üsasisest transporti keskusesse. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 10 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 22+0–22+6 GN-i, kaaluge antenataalset kopsude ettevalmistust GKS-iga. Nõrk positiivne soovitus, mõõdukas tõendatuse aste |
|
| 11 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 23+0–23+6 GN-i, kasutage antenataalset kopsude ettevalmistust GKS-iga. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 12 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 22+0–23+6 GN-i, kaaluge tokolüüsi. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 13 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 22+0–23+6 GN-i, kaaluge neuroprotektsiooni magneesiumsulfaadiga (vt lisa 2). Nõrk positiivne soovitus, mõõdukas tõendatuse aste |
|
| 14 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 22+0–22+6 GN-i, ärge tehke keisrilõiget lootepoolsete näidustuste tõttu. Tugev negatiivne soovitus, mõõdukas tõendatuse aste |
|
| 15 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 23+0–23+6 GN-i, ärge pigem tehke keisrilõiget lootepoolsete näidustuste tõttu. Nõrk negatiivne soovitus, mõõdukas tõendatuse aste |
Austraalia perinataalabi käsitleva ravijuhendi (49) järgi on proaktiivse ravi planeerimisel iga juhtum individuaalne, arvestades võimalikke prognostilisi tegureid (gestatsioonivanus, sünnikaal, sugu, loodete arv, GKS-i eelnev manustamine, antenataalselt diagnoositud patoloogiad, sh väärarendid) ning lapse elumuse ja haigestumise prognoosi.
Lapse elumus ja parem tervisetulem on tõenäolisem, kui tegemist on naissoost lootega, üksiksünnitusega ja gestatsioonivanuse kohta suurema sünnikaaluga lootega. Tervisetulemid ja prognoos on halvemad, kui lootel on diagnoositud raske väärarend (nt raske aju- või südamepatoloogia, diafragmaalhernia, oluline soolehaigus, väike sünnikaal gestatsioonivanuse kohta, Doppleri ultraheliuuringul tuvastatud oluline patoloogia, mitmike korral lootelt lootele transfusiooni sündroom) või rasedal on pikk looteveeta periood, koorionamnioniit või antenataalne verejooks.
Kõikide otsuste tegemisel tuleb kasutada perekeskset lähenemist, teavitades vanemaid igati ja põhjalikult võimalikest riskidest ning kasust emale ja lapsele. Raviplaan peab olema dünaamiline, võimaldades selle pidevat ülevaatamist ja muutmist, kui sünnitus ei leia aset kohe ning rasedus jätkub või kui ilmnevad muud prognoosi muutvad asjaolud. Vanematel on igal ajal õigus oma otsust sekkumiste kohta muuta. Kõik otsused tuleb haigusloos dokumenteerida. Iga sekkumise puhul tuleb teha individuaalne otsus selle rakendamise kohta. Ühe sekkumise rakendamine ei tähenda automaatselt kõikide sekkumiste kasutamist.
Üsasisene transport. Ravijuhendites on soovitatud üsasisest transporti kõrgema etapi haiglasse raseduskestuse korral 22+0–23+6 GN-i. Suurem tõenduspõhisus on soovitada üsasisest transporti raseduskestuse korral 23+0–23+6 GN-i (49, 50, 51).
Prospektiivsetes kohortuuringutes (19, 52) ja metaanalüüsi tulemusena (15) on leitud, et erakordselt väikese gestatsioonivanusega (ELGA) laste sündimine III taseme (kõrgema etapi) haiglas võrreldes madalama etapi haiglas sündimisega on seotud neonataalse surma väiksema riskiga.
Kopsude ettevalmistus. Ravijuhendites on soovitatud loote kopsude ettevalmistust GKS-iga alates raseduskestusest 23+0 GN-i, kuid kui rasedus on kestnud 22+0–22+6 GN-i, siis seda ei soovitata (9, 49, 51, 53). Süstemaatiliste ülevaadete tulemusena ei ole leitud, et ähvardava enneaegse sünnituse korral enne 26. GN-i oleks GKS- ist kasu lapse tervisetulemile, kuid uuringutesse oli kaasatud väga vähe ELGA- vastsündinuid (54, 55). Prospektiivne kohortuuring näitas, et nende laste puhul, kes sündisid gestatsioonivanuses 23+0–25+0 GN-i ning said antenataalselt GKS-i, esines palju vähem surma ja neuroloogilist kahjustust 18 ja 22 kuu vanuses, kuid enne 23.+0 GN-i sündinud lastel sellist seost ei leitud (56). Retrospektiivse uuringu tulemuste põhjal on kopsude ettevalmistus seotud raseduskestuse korral 22+0–23+6 GN-i sündinud laste suremuse olulise vähenemisega (57).
Töörühm otsustas, et arvestades GKS-ravist saadavat võimalikku kasu lapse tervisetulemile, tuleb raseduskestuses 22+0–22+6 GN-i GKS-i manustamist loote kopsude ettevalmistamiseks soovitada ja alates 23.+0 GN-ist rakendada.
Tokolüüs. Tõendusmaterjal tokolüütiliste ravimite kasutamise kohta selles gestatsioonivanuses on väga vähene. NICE ravijuhendis ei ole soovitatud tokolüüsi rakendada raseduskestuse korral 22+0–23+6 GN-i (9). RCOG on seisukohal, et kuigi tokolüüs selles gestatsioonivanuses ilmselt neonataalset tervisetulemit ei paranda, on seda mõistlik kasutada üsasisese transpordi või loote kopsude ettevalmistuse ajal (58). Prospektiivses kohortuuringus, kuhu olid kaasatud enne 27.+0 GN-i sündinud lapsed, leiti, et tokolüütilise ravi rakendamine on seotud imikusurma väiksema riskiga (52).
Tõendusmaterjali põhjal soovitas töörühm kasutada tokolüüsi raseduskestuse korral 22+0–23+6 GN-i, kui on vaja võita aega raseda transpordiks kõrgema etapi haiglasse või loote kopsude ettevalmistuseks.
Neuroprotektsioon. Ravijuhendite soovitused on ekstrapoleeritud uuringutest, kuhu olid kaasatud enneaegsed vastsündinud alates 23.+0 GN-ist. Austraalia perinataalabi käsitlevas ravijuhendis on soovitatud neuroprotektsiooni alates 23.+0 GN-ist, kui plaanitakse elu toetavaid sekkumisi. NICE ravijuhendis on soovitatud neuroprotektsiooni alates 24.+0 GN-ist. (9, 49)
Töörühm otsustas, et kui plaanitakse kasutada teisi elu toetavaid sekkumisi, siis soovitatakse raseduskestuse korral 22+0–23+6 GN-i neuroprotektsiooni magneesiumsulfaadiga (vt lisa 3).
Keisrilõige lootepoolsetel näidustustel. Tõendusmaterjal keisrilõike kohta ELGA- laste puhul on väga vähene. Ravijuhendites ei ole soovitatud teha keisrilõiget raseduskestuse korral 22+0–23+6 GN-i lootest tingitud näidustustel (9, 49, 51). Prospektiivse kohortuuringu põhjal ei vähene keisrilõike korral enne 27.+0 GN-i risk surra või haigestuda imikueas, küll aga on vastsündinu surma risk esimese ööpäeva jooksul väiksem (52). Mitmed retrospektiivsed kohortuuringud on näidanud väga varieeruvaid tulemusi elumuse ja IVH kohta (49). Arvesse tuleb võtta keisrilõike tehnilist keerukust vähese raseduskestuse puhul ning sellest tulenevaid riske ema tervisele ja järgnevatele rasedustele. Retrospektiivne kohortuuring näitas, et nendel naistel, kellel oli anamneesis varajases raseduses (22+0–23+6 GN-i) tehtud keisrilõige, oli sagedamini tegemist klassikalise ehk korporaalse emakalõikega ning järgneva raseduse ajal esines rohkem emakaruptuure. Emakaruptuure oli rohkem ka naistel, kellele oli õnnestunud teha emaka madal ristilõige (59).
Tõendusmaterjal ei näita keisrilõike kindlat eelist vaginaalse sünnituse ees raseduskestuse korral 22+0–23+6 GN-i. Kuna keisrilõige on tehniliselt keerukam ning selle risk ema tervisele ja järgnevatele rasedustele on suurem, ei soovita töörühm raseduskestuse korral 22+0–22+6 GN-i lootepoolsetel näidustustel keisrilõiget teha, ning raseduskestuse korral 23+0–23+6 GN-i on see samuti pigem mittesoovitatav.
Proaktiivse ravitaktika kokkuvõte on toodud lisas 2.
Ravijuhendi ajakohastamisel proaktiivse raviga seotud kliinilist küsimust ei avatud, soovitused kehtivad.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K3.
Loote kopsude ettevalmistus
| 16 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 23+0–33+6 GN-i, kasutage antenataalset kopsude ettevalmistust GKS-iga. |
|
| 17 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 22+0–22+6 GN-i, kaaluge antenataalset kopsude ettevalmistust GKS-iga. Nõrk positiivne soovitus, mõõdukas tõendatuse aste |
|
| 18 |
Ähvardava enneaegse sünnituse korral kasutage antenataalseks loote kopsude ettevalmistuseks beetametasooni või deksametasooni. Annustamine: lihasesisesi beetametasooni 12 mg kaks annust 24-tunnise intervalliga või deksametasooni 6 mg neli annust 12-tunnise intervalliga. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 19 |
Rasedal, kes on saanud GKS-i esialgse kuuri seitsme või enama päeva eest, kuid kellel endiselt esineb enneaegse sünnituse risk enne 34.+0 GN-i järgneva seitsme päeva jooksul, kaaluge ühe GKS-i lisaannuse manustamist. |
|
| 20 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 23+0–33+6 GN-i, kaaluge GKS-i manustamist ka juhul, kui sünnitus toimub enne 24 tunni möödumist. |
|
| 21 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 34+0–36+6 GN-i, ärge pigem kasutage rutiinselt GKS-ravi. |
Prospektiivses kohortuuringus leiti, et 23.+0–25.+6 GN-il sündinud vastsündinutel on antenataalse GKS-ravi foonil väiksem suremus ning IVH, PVL-i ja NEK esinemise sagedus; 22.+0–22.+6 GN-il sündinutel esineb GKS-ide foonil vähem surmasid ja NEK-d (56).
Retrospektiivses kohortuuringus leiti, et GKS-i manustamine vähendab oluliselt 22.+0–23.+6 GN-il sündinud laste suremust (57). GKS-ravi gestatsioonivanuses 26+0–34+6 GN-i vähendab RDS-i esinemist ning gestatsioonivanuses 26+0–29+6 GN-i esineb vähem IVH-d ja neonataalsete surmade arv on väiksem (54).
Ravimi valik. Kahes Cochrane’i süstemaatilises ülevaates on võrreldud deksametasooni ja beetametasooni kasutamist. Mõlema ravimi puhul on leitud teisega võrreldes mõningaid soodsamaid toimeid lapse tervisetulemile, kuid tõendusmaterjali põhjal ei saa teha kindlat eelistust ühe ravimi kasuks. Ühe süstemaatilise ülevaate tulemusena leiti, et nii deksametasooni kui ka beetametasooni kasutamine vähendab tuntavalt neonataalsete surmade arvu ning RDS-i ja IVH esinemist (54).
Teine süstemaatiline ülevaade näitas, et deksametasooni kasutamisel vähenes IVH tekke risk rohkem võrreldes beetametasooniga, samas RDS-i ja perinataalsete surmade osas erinevust ei leitud (60).
Antenataalne GKS vähendab neonataalsete surmade arvu isegi siis, kui laps sünnib vähem kui 24 tundi pärast esimese annuse manustamist, mistõttu tuleks ravi alustada isegi juhul, kui eeldatakse, et sünnitus toimub selle aja sees (54). Euroopa mitme keskuse uuringus selgus, et ka mõne tunni ajavahemikuga sünnini on GKS- ravi saanute väga väikeste enneaegsete rühmas väiksem suremus kui nendel, kes üldse ei saanud GKS-ravi (61).
Kaks enim uuritud GKS-i manustamise skeemi on kaks annust 12 mg beetametasooni lihasesisese süstena manustatuna 24-tunnise intervalliga või neli annust 6 mg deksametasooni lihasesisese süstena manustatuna 12-tunnise intervalliga.
Töörühm otsustas, et eeltoodud tõendusmaterjali arvestades ei saa eelistada kindlat GKS-i preparaati, mistõttu võib kasutada nii beetametasooni kui ka deksametasooni. Erandiks on üsasisese kasvupeetuse ja Doppler-uuringul tuvastatud muutustega loode, kelle puhul tuleks pigem eelistada beetametasooni ning mitte kasutada korduvaid ravikuure. Uuringud on näidanud, et neuroloogiline ja kardiovaskulaarne kaugtulem üsasisese kasvupeetusega lapsel võib beetametasooni kasutamisel olla parem (62–64). Üsasisese kasvupeetuse ja Doppler-uuringul tuvastatud muutustega loodete puhul vajab kortikosteroidide kasutamine ja nende ohutus siiski lisauuringuid.
Korduv ravikuur. Süstemaatilises ülevaates leiti, et korduva(te) annus(t)e manustamise korral rasedatele, kellel enneaegse sünnituse risk püsib seitse või enam päeva pärast esialgset GKS-i manustamist, vähenes vastsündinutel RDS-i ja imiku halvema tervisetulemi (uuringutes erinevalt defineeritud; üldiselt kombineerituna neonataalne surm, RDS, III-IV astme IVH, PVL, NEK, BPD) risk võrreldes rühmaga, kellele korduvat annust ei manustatud. Korduv(ad) ravikuur(id) seostus(id) keskmise sünnikaalu vähenemisega, kuid gestatsiooniajaga korreleeritud sünnikaaludes erinevust ei leitud (65).
Beetametasooni korduvaid kuure ja ravimi ühekordset manustamist võrdlevas süstemaatilises ülevaates leiti, et korduva manustamise korral esines vähem RDS-i, vähenes vajadus surfaktantravi ja hingamistoetuse järele ning neonataalne haigestumine oli väiksem. Samas esines seos väiksema sünnikaalu ja väiksema peaümbermõõduga sünnil, samuti esines emadel rohkem koorionamnioniiti (66).
Süstemaatilise ülevaate ja metaanalüüsi tulemusena on leitud, et korduv beetametasooni kuur (nii üks lisaannus kui ka nädalase või kahenädalase intervalliga korratud annused) vähendab RDS-i esinemise sagedust. Üsasisene kasvupeetus esines neil enneaegsetel vastsündinutel, kes olid eksponeeritud
nädalase või kahenädalase intervalliga beetametasooni korduvatele ravikuuridele (67).
Kahe juhuslikustatud kontrolluuringu põhjal vähendab üks täielik korduskuur (beetametasoon 2 × 12 mg 24-tunnise intervalliga või deksametasoon 4 × 6 mg 12-tunnise intervalliga) oluliselt RDS-i esinemise sagedust ja lisahapniku kasutamise vajadust (68, 69).
Austraalias tehtud mitme keskuse uuringu põhjal ei erinenud kordusdoosi saanud FGR-laste puhul neurokognitiivne tulem platseeboravimit saanud lastega (70). Korea mitmekeskuselises retrospektiivses vaatlusuuringus leiti, et täielik GKS-i ravikuur vähendab normaalse sünnikaaluga (AGA) väga madala sünnikaaluga (VLBW) vastsündinute suremust ning tüsistusi nagu respiratoorne distressi sündroom (RDS), raske intraventrikulaarne hemorraagia (IVH) ja nekrotiseeriv enterokoliit (NEC), kuid kasvupeetusega (SGA) vastsündinute puhul mõju ei täheldatud. (71)
Töörühm on GKS-i korduvat manustamist puudutava otsuse tegemisel olnud teadlik, et tõenduspõhine materjal selle teema kohta on halva kvaliteediga ning rutiinse GKS-i lisakuuri korral ei pruugi kõrvaltoimed üles kaaluda sellest saadavat kasu. Seetõttu töörühm rutiinset korduvat ravikuuri ei soovita. Lähtudes kirjeldatud uuringute tulemustest, võib kaaluda ühekordse lisaannuse manustamist, võttes arvesse raseduskestust, aega eelmisest GKS-i manustamisest ning sünnituse tõenäosust järgmise seitsme päeva jooksul. Naisi, kellele plaanitakse manustada korduv annus, tuleb teavitada võimalikest riskidest ja kasust ning sellest, et info kaugtulemi kohta on piiratud.
Ravijuhendi ajakohastamise käigus soovis töörühm täpsustada kliinilises praktikas vastsündinu ravitulemusele tähtsaid küsimusi: kuidas tagada loote kopsude ettevalmistus üsasisese kasvupeetuse, koorionamnioniidi või ema diabeedi korral ning kas alati on vajalik glükokortikosteroidide täieliku skeemi manustamine või annab tulemusi ka osalise skeemi järgimine?
Antenataalne GKS-ravi on näidustatud enneaegse sünnituse korral enne 34.+0 GNi, kui risk enneaegseks sünnituseks on suur järgmise seitsme päeva jooksul. GKS-ravi efekt on maksimaalne kahe kuni seitsme päeva jooksul ravi alustamisest. Metaanalüüsi põhjal saavad enne 28. GN-i sündinud enneaegsed vastsündinud GKS-ravist kõige enam kasu, sh neurolooglise arengu tulemi osas (72). 34.+0–36.+6 GN-il sündinud enneaegsetel vastsündinutel on GKS-raviga väiksem hingamistoetuse vajadus sünni järel, kuid suurem risk hüpoglükeemiaks, hilisemateks neurokognitiivseteks ja -psühhiaatrilisteks probleemideks (72–74).
Vaimse tervise probleemid ja käitumishäired on sagedasemad ka nendel lastel, kes on sündinud ajalisena, kuid looteea perioodil saanud GKS-ravi (75, 76).
Koorionamnioniit, kasvupeetus ja ema diabeet on olnud uuringutes sageli väljaarvamise kriteerium. Histoloogilise koorionamnioniidi puhul selgus kaheksa kohortuuringu põhjal tehtud madala kvaliteediga analüüsist (vastsündinuid 1460), et GKS-ravi puhul väheneb enneaegsete vastsündinute suremus, III-IV astme IVH ja RDS-i haigestumise esinemine. Kliinilise koorionamnioniidi puhul ei olnud risk vastsündinu sepsiseks suurenenud. Kasvupeetusega laste uuringud olid kõik jälgimisuuringud (77). USA-s tehtud jälgimisuuringu põhjal ei leitud erinevust ema diabeedi korral GKS-ravi saanud ja mittesaanud enneaegsete (23+0–33+6 GN-i) vastsündinute neonataalses haigestumuses (78). Kasvupeetuse ja ema diabeedi korral on soovitatav sama raviskeem, mis on näidustatud vastavas gestatsioonieas.
Töörühm leidis, et tõendusmaterjali põhjal aitab ka osaline GKS-ravi skeem ravitulemust parandada. Võib kaaluda lisaannuse tegemist, kui sünnitus toimub seitsme päeva jooksul. Kindlasti tuleb alati vanemaid informeerida.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K4 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 3 TõKo ja SoKo tabelit.
Loote neuroprotektsioon
| 22 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 24+0 –31+6 GN-i, kasutage rasedal loote neuroprotektsiooniks magneesiumsulfaati. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 23 |
Ähvardava enneaegse sünnituse korral, kui rasedus on kestnud 32+0 –33+6 GN-i, kaaluge rasedal loote neuroprotektsiooniks magneesiumsulfaadi kasutamist. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 24 |
Ähvardava enneaegse sünnituse korral, kui sünnitus toimub tõenäoliselt järgmise 24 tunni jooksul, tuleks lootele neuroprotektsiooni alustada vähemalt 4 tundi enne sünnitust. Annustamine: veenisisesi 4–6 g magneesiumsulfaati boolusena 20–30 minuti jooksul ja edasi 1 g tunnis kuni sünnituseni maksimaalselt 24 tunni jooksul (vt lisa 3). Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 25 |
Ähvardava enneaegse sünnituse korral, kui sünnitus ei toimu 24 tunni jooksul pärast ravi alustamist ja enneaegse sünnituse oht tekib uuesti enne 32.+0 GN-i, kaaluge korduvat magneesiumsulfaadi manustamist. Praktiline soovitus |
Magneesiumsulfaadi manustamine neuroprotektsiooni eesmärgil ähvardava enneaegse sünnituse korral on kulutõhususe analüüsi põhjal tervishoiusüsteemile kulutõhus sekkumine (87). Neuroprotektiivne mõju on suurem enneaegsetel, kes on sündinud enne 32.+0 GN-i (84, 84).
Magneesiumsulfaadi kasutamine ei ole seotud raskete kõrvaltoimetega emale ega vastsündinule. Magneesiumsulfaadi kasutamine võib põhjustada emal kergemaid kõrvaltoimeid, nagu kuumahood, iiveldus, higistamine ja lokaalne ärritus infusiooni piirkonnas. Raskeid kõrvaltoimeid, nagu südameseiskus, hingamise pärssumine, kopsuturse, ulatuslik sünnitusjärgne verejooks, nimetatud metaanalüüsidesse kaasatud uuringutes ei täheldatud (80–82). Vähem tõsiste kõrvaltoimete esinemine kahaneb, kui kasutatakse aeglasemat infusioonikiirust (85). Magneesiumsulfaadi infusiooni ajal soovitatakse jälgida raseda vererõhku, pulssi, hingamissagedust, süvareflekse (nt patellaarrefleksid) ja diureesi. Kõrvaltoimete esinemise korral on soovitatav vähendada infusioonikiirust või lõpetada infusioon.
Kui nifedipiini on kasutatud tokolüüsiks või hüpertensiooni raviks, siis puuduvad vastunäidustused magneesiumsulfaadi kasutamiseks neuroprotektsiooni eesmärgil. Kuigi on kirjeldatud üksikuid juhte, kus samaaegsel kasutamisel nifedipiin süvendas magneesiumsulfaadi neuromuskulaarseid kõrvaltoimeid, ei ole siiski täheldatud tõsist ohtu patsiendile ning ravimeid võib samal ajal kasutada (86).
Magneesiumsulfaadi manustamise jälgimise tabel põhineb analüüsitud tõendusmaterjalil ja on toodud lisas 3 (9, 86, 87).
Kuna piisava tõendusmaterjali puudumise tõttu ei ole täpselt teada, milline annus ja režiim on kõige efektiivsemad ning kas magneesiumsulfaadi korduv manustamine on vajalik, otsustas töörühm kohandada rahvusvaheliste juhendite soovitused annuste ja manustamise ajaliste kriteeriumide kohta (9, 11, 86, 87).
Ravijuhendi ajakohastamise käigus soovis töörühm täpsustada, kas magneesiumsulfaati on vaja korduvalt manustada ja milline peaks olema kahe manustamise vaheline ajavahemik. Puudub tõendusmaterjal magneesiumsulfaadi korduva manustamise kohta olukorras, kus enneaegset sünnitust ei toimu, kuid raseduse progresseerudes tekib uuesti oht ähvardavaks enneaegseks sünnituseks. NICE enneaegse sünnituse ning sünni ravijuhendites ei soovitata magneesiumsulfaati manustada üle 24 tunni, kuid juhul, kui tehakse otsus seda korduvalt manustada, tuleks kaaluda vastsündinu jälgimist hüpokaltseemia, hüpermagneseemia ning luutiheduse languse osas (10, 88). Austraalia enneaegse sünnituse ja sünni ravijuhendi (11) järgi võib naistearst otsustada magneesiumsulfaati korduvalt manustada, kui sünnitus ei toimu pärast esmast manustamist ja enneaegse sünnituse oht püsib. Korduv annus tuleb manustada vähemalt 24 tundi pärast eelmist annust.
Töörühma hinnangul ei ole kindlat tõendust, et soovitada magneesiumsulfaadi korduvat manustamist neuroprotektsiooni eesmärgil. Kindlasti peab arvestama ka ravimi võimaliku kumulatiivse toimega.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K5 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 4 SoKo tabelit.
Mikrobioloogilised uuringud rasedale
| 26 |
Ähvardava või käigusoleva enneaegse sünnituse korral kaaluge rasedal uriinikülvi tegemist. Praktiline soovitus |
|
| 27 |
Ähvardava enneaegse sünnituse korral võtke rasedalt B-grupi streptokoki (GBS) külv tupe alumisest kolmandikust ja rektumi piirkonnast; käigusoleva enneaegse sünnituse korral kaaluge kiirtesti Streptococcus agalactiae DNA tupekaapes (Vag-S agalactiae DNA). Tugev positiivne soovitus, madal tõendatuse aste |
|
| 28 |
Ähvardava või käigusoleva enneaegse sünnituse korral ärge tehke rasedal rutiinselt emakakaelakanalist külvi. Praktiline soovitus |
Uriinikülv. Austraalia enneaegse sünnituse ravijuhendis on soovitatud teha ähvardava enneaegse sünnituse korral naisel uriinianalüüs ja -külv, kuigi tõenduspõhiseid uuringuid, mis näitaksid saadavat kasu ema või lapse tervisetulemile, ei leidunud (89).
Töörühm otsustas siiski, et uriinikülv tuleb teha, sest kuseteede nakkus suurendab püelonefriidi, koorionamnioniidi ja enneaegse sünnituse riski ning selle puhul on antibakteriaalne ravi tõhus (87, 90).
GBS-analüüs. GBS on enneaegse sünnituse riskitegur ning enneaegne sünnitus on vastsündinul GBS-infektsiooni väljakujunemise riskitegur. 20 uuringut (kohortuuringud, läbilõikeuuringud ja juhtkontrolluuringud) hõlmava süstemaatilise ülevaate põhjal esineb seos enneaegse sünnituse ja sünnitusaegse GBS-i kolonisatsiooni vahel (91). Euroopa neonatoloogia- ja günekoloogiaeksperdid on soovitanud ähvardava enneaegse sünnituse sümptomite või PPROM-iga naistel, keda pole eelneva viie nädala jooksul GBS-i kandluse suhtes sõeluuritud, võtta GBS-analüüs vatipulgaga tupe alumise kolmandiku ja rektumi piirkonnast (92). GBS-analüüsi ei võeta emakakaelakanalist. Kiirtestimine (GBS-PCR) GBS-i kandluse suhtes enneaegse sünnituse ajal võimaldab otsustada sünnitusaegse antibakteriaalse profülaktika vajalikkuse üle.
Bakteriaalne külv emakakaelakanalist. Puudub kvaliteetne tõendusmaterjal, mille kohaselt parandaks ähvardava enneaegse sünnitusega raseda emakakaelakanalist mikrobioloogilise külvi rutiinne võtmine ema ja lapse tervisetulemit. Külvi võtmine ei aita koorionamnioniidi diagnoosimises ega ravikäsitluses ning see on seletatav koorionamnioniidi polümikroobse etiogeneesiga (93).
Asümptomaatilise bakteriaalse vaginoosi ravi ei vähenda enneaegse sünnituse riski (94). Sümptomaatiline bakteriaalne vaginoos vajab ravi, sest seda seostatakse enneaegse sünnituse ja koorionamnioniidiga (95).
Gonorröasse haigestumine on Eestis madal, seega rasedaid rutiinselt selle suhtes ei testita. Klamüdioosi skriining tehakse Eestis kõigile rasedatele esmasel pöördumisel, kui analüüsi ei ole tehtud viimase kuue kuu jooksul (vt ENS-i raseduse jälgimise juhend, 2018) (96).
Eelnevast lähtudes otsustas töörühm, et rutiinne bakteriaalse külvi võtmine emakakaelakanalist ähvardava või käigusoleva enneaegse sünnituse korral ei ole näidustatud. Analüüsi(de) võtmise vajaduse otsustamisel tuleks lähtuda raseda anamneesist ja tervisekäitumisest.
Rasedal, keda ei ole raseduse jooksul jälgitud, tuleb ähvardava või käigusoleva enneaegse sünnituse korral võtta kõik rasedusaegsed infektsioonide skriininganalüüsid, st HIV, süüfilise, B-hepatiidi ja klamüdioosi analüüs (vt ENS-i raseduse jälgimise juhend, 2018) (96).
Ravijuhendi ajakohastamisel soovis töörühm selgitada, kas ja millal on vajalik ähvardava ja/või käigusoleva enneaegse sünnituse korral rasedal võtta emakakaelakanalist või tupest aeroobne külv, sh määrata B-grupi streptokokki (GBS). Uuemaid aeroobse külvi võtmist käsitlevaid uuringuid ei leidunud ning soovituste tugevus ja sõnastus jäeti töörühma otsusel samaks. Ilmselt ei uurita seda teemat enam aktiivselt, järgitakse riikides kehtivaid juhendeid. Pigem ei soovitata rutiinselt külve teha. Kui lootevesi on puhkenud, tehakse kiirtest, mille tulemuste alusel määratakse antibiootikumravi.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K6 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 5 SoKo tabelit.
Antibakteriaalne ravi rasedale
| 29 |
Lootevee enneaegse puhkemiseta, bakteriaalse infektsiooni kliiniliste tunnusteta ähvardava enneaegse sünnituse korral ärge alustage rasedal antibakteriaalset ravi. Tugev negatiivne soovitus, mõõdukas tõendatuse aste |
|
| 30 |
Lootevee enneaegse puhkemisega ähvardava enneaegse sünnituse korral alustage antibakteriaalset ravi erütromütsiiniga, selle puudumise korral kasutage penitsilliini. Penitsilliiniallergia puhul kasutage klindamütsiini. Tugev positiivne soovitus, kõrge tõendatuse aste [RAKENDUSPIIRANG] |
|
| 31 |
Koorionamnioniidi puhul alustage laia toimespektriga või kombineeritud antibakteriaalset ravi, rasedust prolongeerimata (vt lisa 4). |
|
| 32 |
Vältige rasedal amoksitsilliini-klavulaanhappe kasutamist vastsündinu nekrotiseeriva enterokoliidi suurenenud riski tõttu. Tugev negatiivne soovitus, mõõdukas tõendatuse aste |
|
| 33 |
Enneaegse sünnituse ajal alustage rasedal GBS-i kandluse või teadmata GBS-i staatuse korral veenisisest profülaktilist antibakteriaalset ravi bensüülpenitsilliiniga. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
Antibakteriaalse ravi kasutamise metaanalüüsi tulemused näitasid ähvardava enneaegse sünnituse korral puhkemata looteveega rasedatel infektsiooni esinemise sageduse vähenemist neil, kes olid saanud antibakteriaalset ravi. Samas suurenes antibakteriaalset ravi saanud rasedate rühmas neonataalsete surmade arv (98). Seitsmeaastaste laste kaugtulemi analüüs näitas lastel, kelle emad olid saanud antibakteriaalset ravi puhkemata lootevee korral, enam CP-d võrreldes platseeborühmaga (102). Kui rasedal ei esine kliinilist infektsiooni ja lootevesi ei ole puhkenud, pole antibakteriaalse ravi alustamine näidustatud, kuna puuduvad andmed selle positiivse mõju kohta vastsündinu lähitulemile ja teada on selle ravi negatiivne mõju laste neuroloogilisele arengule (11, 98, 103).
PPROM-i korral pikendab antibakteriaalse ravi alustamine rasedust, vähendab koorionamnioniidi ja neontaalse infektsiooni esinemise sagedust, surfaktant- ja hapnikravi vajadust ning laste arvu, kellel on haiglast väljakirjutamisel patoloogilise leiuga aju ultraheli leid. Antibakteriaalse ravi rühmas võrreldes platseeborühmaga ei esine olulist perinataalsete surmade arvu vähenemist (9, 97, 103, 104) ja laste kaugtulemis funktsionaalsete häirete esinemise sageduse erinevust (101).
Antibiootikumi valik. Ähvardava enneaegse sünnituse korral lootevee enneaegse puhkemisega rasedatel soovitatakse valikravimina kitsa toimespektriga antibiootikumi. Mitmes ravijuhendis on soovitatud valikravimina kasutada erütromütsiini (annus 250 mg × 4), kuna seda on ORACLE uuringus kõige põhjalikumalt testitud. Alternatiivravimina pakutakse penitsilliini (9, 11, 104). Soovitatav antibakteriaalse ravi kestus on maksimaalselt kümme päeva (9, 104).
On tõestatud, et amoksitsilliin-klavulaanhappe kasutamine rasedal on seotud vastsündinul nekrotiseeriva enterokoliidi esinemise suurenemisega, seega soovitatakse selle preparaadi manustamist vältida (9, 97, 98).
Koorionamnioniit. Koorionamnioniit on oluline ema ja vastsündinu surma põhjus. Metaanalüüside tulemused näitavad, et koorionamnioniit on vastsündinul seotud suurema riskiga NEK (105) ja CP (106) tekkeks ning emal metroendometriidi (emakasisekestapõletik ehk emakakestapõletik) ja sepsise tekkeks. Juhuslikustatud uuringute tulemused näitavad, et koorionamnioniidi diagnoosimisel tuleb antibakteriaalset ravi alustada laia toimespektriga antibiootikumiga või kasutada kombineeritud raviskeeme, et vähendada koorionamnioniidiga seotud tüsistuste teket nii emal kui ka vastsündinul (11, 93, 107).
Rahvusvahelistes ravijuhendites (NICE, Queensland) soovitatakse kasutada kombineeritud raviskeeme. Eesti haiglates on siiamaani kasutatud pigem ühte laia toimespektriga antibiootikumi.
Kliinilise koorionamnioniidi diagnoos põhineb mitme tunnuse kombinatsioonil ega tohi toetuda vaid ühele kliinilisele tunnusele (nt CRP sisalduse suurenemine, leukotsütoos või kardiotokogrammi muutused) (9). Koorionamnioniidi kliinilised tunnused (89, 93) on toodud lisas 4.
Kui eelistatakse kasutada ühte laia toimespektiga antibiootikumi (nt ampitsilliin/ sulbaktaam, tsefalosporiin), soovitame lähtuda haiglasisesest ravi- või tegevusjuhendist.
GBS-i profülaktika. Enneaegne sünnitus on vastsündinul varajase ja hilise GBS-infektsiooni väljakujunemise suur riskitegur. Töörühma soovitus GBS-i antibakteriaalse profülaktika kohta tugineb Euroopa neonatoloogia ja günekoloogia eriala ekspertide koostatud protokollile (92), kus on soovitatud GBS-i antibakteriaalset profülaktikat enneaegse sünnituse korral kõigile GBS-i kandlusega ja teadmata GBS-i staatusega rasedatele. Haiglasse saabumisel soovitatakse rasedal, keda pole eelneva viie nädala jooksul GBS-i kandluse suhtes sõeluuritud, võtta GBS-analüüs vatipulgaga tupe alumise kolmandiku ja rektumi piirkonnast (92). GBS-analüüsi ei võeta emakakaelakanalist. Kiirtestimine (GBS-PCR) GBS-i kandluse suhtes enneaegse sünnituse ajal võimaldab otsustada sünnitusaegse antibakteriaalse profülaktika vajalikkuse üle (92, 104, 108, 109).
Ravijuhendi ajakohastamise käigus soovis töörühm selgitada, millise ravimiga alustada antibakteriaalset ravi koorionamnioniidi kliiniliste tunnuste puudumisel ning kas kasutada ühte preparaati või kombineeritud ravi. Leidus kaks metaanalüüsi, kuhu kaasatud uuringud osaliselt kattusid. Esimeses võrreldi kümmet antibiootikumi skeemi. Metaanalüüsi tulemusel leiti, et PPROM-i korral kasutatav profülaktiline antibiootikum võiks eelistatult olla penitsilliin või klindamütsiin koos gentamütsiiniga, kuna nendega on leitud kõige suurem koorionamnioniidi esinemise sageduse langus (110). Teises metaanalüüsis leiti, et koorionamnioniidi ennetamiseks on ilmselt kõige efektiivsem klindamütsiin koos gentamütsiiniga ja neile järgneb penitsilliin. (111) Rahvusvahelistes juhendites soovitatakse ähvardava enneaegse sünnituse korral lootevee enneaegse puhkemisega rasedatel kasutada valikravimina erütromütsiini (112).
Koorionamnioniidi korral on rahvusvaheliste juhendite põhjal efektiivne kolmikravi (penitsilliin, gentamütsiin ja metronidasool või amoksitsilliin, gentamütsiin ja metronidasool), penitsilliiniallergia korral tuleks valida klindamütsiin. Sünnitusabi teenust osutavad haiglad võivad kasutada erinevaid antibiootikumravi skeeme tulenevalt mikrobioloogilisest seirest. Kolmikravi katab küll terve spektri, kuid on naisele raske taluda ning raviga kaasuvalt hakkavad vohama oportunistlikud mikroobid. (104)
Rakenduspiirang
Erütromütsiin oli ravijuhendi ajakohastamise ajal kättesaadav Ravimiameti taotluse alusel. Täpsem info on kirjas rakenduskavas.
Sünnitusviisi valik
| 34 |
Enneaegse sünnituse korra ärge tehke keisrilõiget, kui loode on peaseisus ja keisrilõike ainuke näidustus on enneaegsus. |
|
| 35 |
Enneaegse sünnituse korral, kui rasedus on kestnud vähemalt 24.+0 GN-ini ja kui loode on tuharseisus, kaaluge keisrilõike tegemist. Nõrk positiivne soovitus, väga madal tõendatuse tase
|
|
| 36 |
Enneaegse kaksiksünnituse korral, kui esimene kaksik on peaseisus, eelistage vaginaalset sünnitust. Nõrk positiivne soovitus, väga madal tõendatuse aste
|
|
| 37 |
Enam kui kahe loote korral eelistage keisrilõike tegemist. Praktiline soovitus |
Cochrane’i süstemaatilises ülevaates, mis hõlmas enneaegseid sünnitusi raseduskestuse korral 26+0–33+6 GN-i, leiti, et keisrilõike ja vaginaalsel teel sündinud lastel ei esinenud erinevusi järgmistes näitajates: sünnikahjustus; perinataalne asfüksia; viienda minuti Apgari hinne; hüpoksilis-isheemiline entsefalopaatia, RDS-i, vastsündinu krampide ja perinataalsete surmade esinemise sagedus; vastsündinute invasiivse hingamistoetuse vajaduse kestus ja lisahapniku vajadus (114).
RCOG ülevaate põhjal leiti, et raseduskestuse korral 22+0–24+6 GN-i oli keisrilõike teel sündinud laste neonataalsete surmade arv väiksem, kuid seda vaid esimesel elupäeval. Alla 1500 g kaaluvatel vastsündinutel oli keisrilõige seotud paremate tervisetulemitega, kui enneaegsusega kaasnes koorionamnioniit (58). Sarnased tulemused leiti prospektiivses populatsioonipõhises vaatlusuuringus, kus oli käsitletud eriti enneaegsete (kuni 27+0 GN-i) vastsündinute sünnitusviisi – keisrilõige vähendas vastsündinute surma esimesel elupäeval, kuid mitte hiljem (115).
Suure valimiga retrospektiivses kohortuuringus, kus võrreldi loote peaseisu korral vaginaalset sünnitust keisrilõikega ja kus raseduskestus oli 24+0–27+6 GN-i, ei leitud erinevust vastsündinute tervisetulemis. Raseduskestuse korral 28+0–31+6 nädalat ei leitud keisrilõiget ja vaginaalset sünnitust võrreldes erinevusi neonataalsete surmade arvus, kuid planeeritud vaginaalse sünnituse rühmas esines vähem perinataalset asfüksiat ja RDS-i ning invasiivse hingamistoetuse vajadus oli väiksem; samas suurenes IVH esinemise sagedus (116). IUGR-vastsündinutel raseduskestuse korral 25+0–33+6 nädalat ei ole keisrilõige seotud parema neonataalse tervisetulemiga, kuid on seotud RDS-i tekke suurema riskiga (117).
Ravijuhendites on soovitatud peaseisus loote korral eelistada vaginaalset sünnitust (9, 11, 113, 118).
Ravijuhendi ajakohastamisel tehtud tõendusmaterjali otsingu käigus leiti 2016. aastal ilmunud metaanalüüs (119), kus ei leitud alla 1500 g enneaegsete vastsündinute puhul statistiliselt olulist suremuse erinevust vaginaalse sünnituse ja keisrilõike võrdluses. Samuti ei leitud erinevust III-IV astme IVH ega neuroloogilise puude esinemises, kuid IVH-d üldiselt esines enam vaginaalselt sündinud enneaegsete laste (alla 1500 g) seas. Teises, süstemaatilises ülevaates ja metaanalüüsis leiti, et suremus 22.–27.+6 GN-il sündinud enneaegsete vastsündinute seas oli väiksem keisrilõike teel sündinud laste rühmas (120).
Sünnitusviisi valik tuharseisu korral. Tuharseisu korral, kui rasedus on kestnud 26+0–36+6 GN-i, võib kaaluda sünnitust keisrilõike teel, teavitades ema, et selle teema kohta tõenduspõhised uuringud puuduvad (9, 89).
The Consortium on Safe Labori uuringus leiti, et tuharseisu korral, kui rasedus oli kestnud 24+0–27+6 GN-i, oli planeeritud vaginaalne sünnitus võrreldes planeeritud keisrilõikega seotud neonataalsete surmade suurema arvuga, kuid samas esines selles rühmas vähem neonataalset sepsist ja invasiivse hingamistoetuse vajadust. Planeeritud vaginaalsetest sünnitustest tuharseisu korral, kui rasedus oli kestnud 28+0–31+6 GN-i, õnnestus vaid 17,2% ja üldine neonataalsete surmade osakaal selles rühmas oli 2,9%. Planeeritud vaginaalne sünnitus tuharseisu korral võrreldes planeeritud keisrilõikega oli seotud rohkemate neonataalsete surmadega (116).
Prospektiivses populatsioonipõhises vaatlusuuringus leiti, et tuharseisu korral, kui rasedus oli kestnud kuni 27+0 GN-i, on vaginaalne sünnitus seotud neonataalsete surmade suurema arvuga ning neuroloogilise arengu suurema mahajäämusega 2,5 aasta vanuselt (115).
Ravijuhendi ajakohastamisel leiti mitmeid hiljuti avaldatud uuringuid, kuid enamasti oli tegemist madala tõendatuse astmega, sest puuduvad juhuslikustatud uuringud.
RCOG tuharseisu käsitleva ravijuhendi alusel ei ole spontaanselt alanud sünnituse korral rutiinne keisrilõige näidustatud. Soovitatakse individuaalset lähenemist, arvestades naise soovi, tuharseisu tüüpi, loote seisundit ja arsti oskusi võtta vastu vaginaalset tuharseisus sünnitust. Spontaanselt alanud sünnituse korral keisrilõige raseduse suuruses 22–25+6 GN-i ei ole soovitatud. (121)
Kui raseduse lõpetamine on vajalik ema ja/või lootepoolsetel näidustustel ja sünnitustegevus pole vallandunud, siis on soovitatav plaaniline keisrilõige, mitte sünnituse indutseerimine (121).
Retrospektiivses uuringus, kus uuriti 413 tuharseisus enneaegset sünnitust, leiti, et vaginaalselt sündinud lastel on suurem risk viienda minuti Apgariks alla 7, võrreldes keisrilõike teel sündinud lastega, eriti vanuserühmas 28–37 GN-i. Enne 28. GN-i sündinud enneaegsetel vastsündinutel olulist erinevust ei olnud (122). Teises retrospektiivses uuringus väga enneaegsetel (23–25+6 GN-i) tuharseisus sündinutel leiti neonataalset suremust rohkem vaginaalse sünnituse rühmas. Samas oli ka gestatsioonivanus selles rühmas väiksem. Neuroloogilise patoloogia (IVH, PVL), Apgari hinnete ja nabaväädi pH väärtuste osas erinevusi ei olnud. (123)
Soome 2004.–2017. aasta retrospektiivne uuring, milles võrreldi vaginaalset sünnitust ja plaanitud keisrilõiget 32.–36.+6 GN-il sündinud enneaegsetel vastsündinutel, leiti, et vaginaalse sünnitusega on oluliselt suurem tõenäosus madalamaks Apgari hindeks. Samas vaginaalselt sündinud lapsed vajasid vähem antibakteriaalset ravi, sattusid harvem intensiivravisse ning neil esines vähem RDS-i. Vastsündinute intubatsioonivajadus rühmade vahel ei erinenud. (124)
Euroopa kohortuuringus (24–31 GN tuharseisus sünnitused), kus osales ka Eesti, leiti, et vaginaalse sünnitusega on suurem risk vastsündinu surmaks, madalaks Apgari hindeks ja neuroloogiliseks kahjustuseks. Erinevus oli eriti suur 24.–25.+6 GN-il sündinud enneaegsete vastsündinute seas. Samas oli vaginaalse sünnituse rühmas väiksem gestatsioonivanus ja rohkem vastsündinuid, kes ei olnud saanud loote kopsude ettevalmistust. (125)
Prantsusmaal tehtud kohortuuringus, milles võrreldi planeeritud vaginaalset sünnitust planeeritud keisrilõikega (26–34 GN) enneaegsetel tuharseisus üksikloodete puhul, ei leitud keisrilõike rühmas elumuse paranemist ega haigestumise vähenemist. (126)
Mahukas kohortuuringus (8356 tuharseisus enneaegset sünnitust, 26+0–36+6), milles võrreldi planeeritud vaginaalset sünnitust planeeritud keisrilõikega, leiti, et keisrilõike rühmas on haigestumus väiksem kui vaginaalse sünnituse rühmas. Suremus oli väiksem keisrilõike rühmas, eriti 28+0–31+6 (vaginaalse sünnituse rühmas 4,1% ja plaanitud keisrilõike rühmas 1,7%) (127).
Viimaste aastate jooksul on sel teemal tõendusmaterjali lisandunud. Töörühm otsustas ajakohastada olemasolevat soovitust ja sõnastada see nõrga positiivse soovitusena.
Emade tervisetulem. Keisrilõige enneaegse sünnituse korral on tehniliselt raskem ega ole lapsele täiesti ohutu. Vajalikuks võib osutuda klassikaline ehk korporaalne keisrilõige, mida seostatakse ema terviseriskide (armi dehistsents, emaka rebend, platsenta peetumine, ema surm) suurenemisega järgnevate raseduste ajal (89). Puudub info emade hospitaliseerimise kohta intensiivravi osakonda, kuid erakorralise keisrilõike rühmas on kirjeldatud tunduvalt rohkem sünnitusjärgseid komplikatsioone (haava dehistsents, süvaveenitromboos, endotoksiline šokk, sepsis). Sünnitusjärgse verejooksu puhul erinevusi ei leitud (114). Emade rahulolu kohta info puudub.
Töörühm otsustas tõendusmaterjali põhjal soovitada teha sünnitusviisi valik raseduskestuse korral 22+0–23+6 GN-i, lähtudes sünnitusabi ja emapoolsetest näidustustest (nt platsenta irdumine, raske preeklampsia, eklampsia), mitte niivõrd lootepoolsetest põhjustest, ning keisrilõiget rutiinselt mitte soovitada. Keisrilõiget võib kaaluda, kui rasedus on kestnud üle 24 nädala ja loode on tuharseisus.
Ravijuhendi ajakohastamise käigus leiti kolm uuemat allikat. Süstemaatilises ülevaates ja metaanalüüsis leiti, et enne 26. GN-i tehtud keisrilõike puhul on emade raske haigestumise risk palju suurem kui pärast 26. GN-i tehtud keisrilõike korral (128). Samuti on keisrilõike rühmas rohkem ema near-miss-juhtumeid ja emade intensiivravi vajadust (129). Värskes retrospektiivses Soome uuringus, milles uuriti enneaegse tuharseisus loote sünnitamise viisi (vaginaalne või keisrilõige) mõju järgmisele sünnitusele, leiti, et naistel, kes on eelmise enneaegse tuharseisus lapse sünnitanud keisrilõike teel, on suurem tõenäosus nii plaaniliseks kui erakorraliseks keisrilõikeks ja instrumentaalseks sünnituseks ka järgmise sünnituse ajal. Samuti oli nendel lastel suurem tõenäosus sattuda intensiivravisse. Enneaegse sünnituse risk järgmisel sünnitusel ei erinenud. (130)
Tõendusmaterjali põhjal (väga madal tõendatuse aste) ei ole võimalik soovitada kindlalt ühte või teist sekkumist. Enneaegse tuharseisus sünnituse korral võib keisrilõige vähendada vastsündinu suremust ja haigestumust.
Sünnitusviisi valik mitmikraseduse korral. ACOG praktilises juhendis on mitmikute sünnitusviisi valiku kohta kirjas, et kaksikrasedus üksi ei ole keisrilõike näidustus ning otsuse tegemisel tuleb lähtuda amniaalsusest/koriaalsusest, loodete seisust, raseduskestusest ja abiosutaja pädevusest. ACOG ekspertide konsensusliku arvamuse põhjal tuleks raseduskestuse korral 32+0 või rohkem esimese loote peaseisu puhul eelistada vaginaalset sünnitust. Algse juhendi koostamise ajal puudusid uuringud sünnitusviisi kohta rohkem kui kahe lootega raseduse korral, kuid nimetatud juhendis ei ole ka siis välistatud vaginaalset sünnitust (113).
Kanada Sünnitusabiarstide ja Günekoloogide Ühingu (SOGC) soovituse (131) kohaselt tuleks plaaniline keisrilõige teha kaksikraseduse korral (loodete prognooskaal üle 2500 g) monoamniaalsete kaksikute ja Siiami kaksikute puhul ning samadel põhjustel, mis üksikloote puhul.
Vaginaalne sünnitus on näidustatud esimese loote peaseisu ja teise loote tuharseisu (loodete prognooskaal 1500–4000 g) korral, kui naistearst on võimeline vastu võtma tuharseisus sünnitust. Puudub tõenduspõhisus sünnitusviisi eelistamise kohta esimese loote peaseisu ja teise loote tuharseisu korral, kui loodete prognooskaal on 500–1500 g (131).
Süstemaatilises ülevaates ja metaanalüüsis, kus käsitleti sünnitusviisi kaksikraseduse korral, leiti, et plaaniline keisrilõige esimese loote tuharseisu korral võib parandada viienda minuti Apgari hinnet, kuid muu kohta puudub tõendusmaterjal, mis toetaks plaanilise keisrilõike tegemist kaksikraseduse korral (132).
Ravijuhendi ajakohastamisel vaadati üle rahvusvahelised juhendid ning tehti süstemaatiline tõendusmaterjali otsing. NICE ravijuhendis soovitatakse sünnituse lõpetamist keisrilõike teel, kui esimene loode ei ole peaseisus ja tegemist on dikoriaalsete diamniaalsete või monokoriaalsete diamniaalsete kaksikutega. Monokoriaalsed monoamniaalsed kaksikud peaksid sündima keisrilõike teel ka siis, kui mõlemad looted on peaseisus. Kolmikute korral soovitatakse raseduse plaanilist lõpetamist keisrilõike teel raseduskestuses 35 GN-i. Keisrilõiget soovitatakse kolmikute korral ka igas raseduse varasemas järgus, kui on lootust eluvõimeliste laste sünniks. (89)
RCOG juhendis soovitatakse esimese loote tuharseisu korral plaanilist keisrilõiget. Kui sünnitustegevus on juba käigus, siis rutiinne erakorraline keisrilõige esimese loote tuharseisu korral pole soovitatav. Arvestama peaks emakakaela avatuse, eesasetseva osa kaugust, tuharseisu tüüpi (liht- vs. segatuharseis), loote seisundit ja sünnitusabi arsti oskusi. Rutiinset keisrilõiget teise loote tuharseisu tõttu ei soovitata (121).
Retrospektiivses kohortuuringus, kus uuriti 1655 rasedat (212 naisel planeeritud keisrilõige ja 1443 naisel planeeritud vaginaalne sünnitus) 26.–32. GN-il, leiti, et perinataalne suremus ja haigestumus on suuremad keisrilõike rühmas olenemata esimese loote seisust. Emade haigestumus oli tunduvalt suurem keisrilõike rühmas. Alarühmade uuringus, kus võrreldi planeeritud keisrilõiget tegeliku sünnitusviisiga (mõlema loote vaginaalset sünnitust ja erakorralist keisrilõiget mõlemal lootel ja erakorralist keisrilõiget teisel lootel), ei leitud vaginaalse sünnituse ja erakorralise keisrilõike rühmas olulisi erinevusi (nii ühe kui ka mõlema loote tõttu). (133)
Kanadas tehtud retrospektiivses kohortuuringus võrreldi kaksiksünnitusi nii sünnitusviisi (mõlemad looted vaginaalne n = 1934 vs. kombineeritud n = 418 vs. mõlemad keisrilõikega n = 4284) kui ka loodete asetuse osas. Vaginaalse sünnituse rühmas oli suurem tõenäosus IVH ja PVL-i kujunemiseks. Vaginaalse sünnituse ja kombineeritud lähenemise rühmas statistiliselt olulist erinevust ei olnud. Keisrilõike rühmas oli rohkem RDS-i kui vaginaalse sünnituse rühmas. Vaginaalse sünnituse ja kombineeritud sünnituse vahel olulist erinevust ei olnud. Loodete asetusest lähtuvalt selgus, et vastsündinu surmaks on suurenenud risk, kui esimene loode on tuharseisus ja teine loode peaseisus. Selliseid sünnitusi oli 476 ja nendest naistest 92% sünnitas keisrilõike teel. (134)
Kanadas tehtud kohortuuringus (135) (peaseis/mittepeaseis) ei leitud väga enneaegsetel (24+0–27+6) erinevusi neonataalse suremuse ja haigestumise osas vaginaalse sünnituse katse ja keisrilõike vahel. See tuleneb ilmselt sellest, et sügav enneaegsus on põhiline faktor, mis otsustab tulemuse. Sama kinnitab ka 2017. aasta metaanalüüs (136).
USA-s tehtud retrospektiivses kolmikute sünnitusuuringus võrreldi vaginaalse sünnituse katset ja plaanitud keisrilõiget. Vaginaalse sünnituse katse oli seotud suurema vereülekande riskiga emale ja suurema mehaanilise ventilatsiooni vajadusega lastele. Asfüksia esinemises erinevusi ei olnud. Ainult 16,7% vaginaalse sünnituse katsetest lõppes vaginaalse sünnitusega (neli kolmikute komplekti, 12 vastsündinut). (137)
Töörühma arvamusel on tuharseisus esimese kaksiku korral võimalik vaginaalne sünnitus, kuid arvestama peab emakakaela avatust, eesasetseva osa kaugust, tuharseisu tüüpi (liht- vs. segatuharseis), loote seisundit ja sünnitusviisi valikul sünnitusabi arsti oskusi.
Võttes arvesse võimalikke komplikatsioone ning raskendatud jälgimist sünnituse ajal, on töörühma hea tava suunis enam kui kahe loote korral sünnitus keisrilõike teel.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K8 ning ajakohastatud ravijuhendi kliiniliste küsimuste nr 7, 8, 9 TõKo ja SoKo tabeleid.
Episiotoomia
| 38 |
Enneaegse sünnituse korral ärge tehke rutiinselt episiotoomiat. Praktiline soovitus |
Selle teema kohta on uuringuid vähe ja need on madala tõendatuse astmega (kolm ülevaateartiklit), kuid nendest ilmneb, et episiotoomia rutiinne kasutamine enneaegsete vastsündinute tervisetulemit ei paranda (138, 139).
Kuna teema kohta puudub tõenduspõhine materjal, mis pooldaks episiotoomia tegemist, otsustas töörühm pärast 37. täisrasedusnädalat tehtud süstemaatilise ülevaate põhjal, et rutiinne episiotoomia ei ole näidustatud ning episiotoomia tuleb teha vaid sünnitusabist lähtuvatel näidustustel (140).
Ravijuhendi ajakohastamisel vastavat kliinilist küsimust ei avatud ja uut teaduskirjanduse otsingut ei tehtud. Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K9.
Raseduse prolongeerimine
39 |
Ähvardava enneaegse sünnituse korral, kui lootevesi on enneaegselt puhkenud ja raseduse kestus on lühem kui 34+0 GN-i, eelistage raseduse prolongeerimist, kui ei esine vastunäidustust (vt lisa 5). |
|
| 40 |
Lootevee enneaegse puhkemisega spontaanselt alanud sünnituse korral, kui raseduse kestus on 34+0–36+6 GN-i, ärge kasutage tokolüüsi. |
|
| 41 |
Ähvardava enneaegse sünnituse korral, kui lootevesi on enneaegselt puhkenud ja raseduse kestus on 34+0–36+6 GN-i, kaaluge induktsiooni. |
Puuduvad uued juhuslikustatud uuringud, milles oleks võrreldud prolongeerimise taktikat kohese sünnituse taktikaga PPROM-i ravi (profülaktiline antibakteriaalne ravi, loote kopsude ettevalmistus) tingimustes. Viimased uuringud sel teemal pärinevad 1990. aastatest (143–145). Nende uuringute põhjal koostatud süstemaatilistes ülevaadetes on soovitatud PPROM-i korral rasedust pikendada 34.+0 GN-ini, kuna varajasem sünnitus suurendab neonataalsete surmade ja keisrilõigete arvu (146, 147). Raseduse pikendamine vähendab vastsündinul sünni järel RDS-i esinemise sagedust, kuid rasedat tuleb teavitada võimalikust koorionamnioniidi riskist ja sellest tulenevatest ohtudest lapsele (147, 148). Raseduse prolongeerimise kestus ja koorionamnioniit on olulised PVL-i riskitegurid (142), kuna 60–100%-l lastest areneb PVL-i korral välja CP. Koorionamnioniidi diagnoos on keeruline, sest selle kulg on sageli subkliiniline ning haiguse algfaasis esineb palavikku ja põletikunäitajate sisalduse suurenemist harva.
Juhuslikustatud kontrolluuringus käsitleti antenataalset lootevee puhkemist raseduskestuse korral 34+0 –36+6 GN-i. Kahe rühma – induktsioon vs prolongeerimine – võrdlemisel ei leitud erinevusi neonataalse sepsise, RDS-i, hüpoglükeemia ega hüperbilirubineemia esinemise sageduses. Keisrilõigete arv oli mõlemas rühmas sarnane. Autorid järeldasid, et raseduse pikendamine 37+0 GN-ini võib olla põhjendatud juhul, kui ei esine GBS-i kandlust (149–152).
Ravijuhendi ajakohastamisel soovis töörühm täpsustada raseduse prolongeerimist väga enneaegse sünnituse korral (kuni 31+6 GN-i vs. üle 32 GN-i). Lisaks soovitakse selgitada, kui kaua prolongeerida rasedust juhul, kus lootevesi on puhkenud (juhtudel, kui lootevett on alles või on tekkinud anhüdramnion).
Rahvusvahelistes ravijuhendites raseduse prolongeerimist PPROM-i puhul ei käsitletud. Cochrane’i 12 uuringut haaranud süstemaatilises ülevaates, mis hõlmas patsiente enneaegse sünnituseelse lootevee puhkemisega raseduse kestuses 25–36+6 rasedusnädalat, ei leitud statistiliselt olulist erinevust raseduse prolongeerimise ja sünnituse indutseerimise vahel järgmistes tulemusnäitajates: vastsündinu infektsioon/sepsis, perinataalsuremus ning periventrikulaarse leukomalaatsia (PVL-i), ajusisese verejooksu ja nekrotiseeriva enterokoliidi (NEK) esinemine. Raseduse varase lõpetamise rühmas oli suurem respiratoorse distressi sündroomi (RDS-i) esinemissagedus, hingamistoetuse vajadus, vastsündinute suremus, keisrilõigete osakaal, väiksem koorionamnioniidi ja suurem metroendometriidi esinemissagedus ning lühem ema haiglaravi kestus. Eraldi tehti alaanalüüs osale tulemusnäitajatele, eristades rasedusi alla ning üle 34 GNi. Üle 34 GN-i kestnud raseduste puhul esines raseduse prolongeerimise rühmas vähem RDS-i ja rohkem koorionamnioniiti, alla 34 nädala kestnud raseduste puhul olulist erinevust nende tulemusnäitajate puhul ei esinenud. (153)
Töörühm arutas, et üldiselt püütakse vastunäidustuste puudumisel rasedust prolongeerida. RCOG vastavas ravijuhendis soovitatakse prolongeerida kuni 34 GN-ini. Praktikas, kui ei esine vastunäidustusi, püütakse prolongeerida kuni 34+6 GN-ini – kui siis algab sünnitus, edasi ei prolongeerita. Igal juhul on lähenemine iga raseduse korral individuaalne, mõni rase ei soovi sekkumist. Ähvardava enneaegse sünnitusega rasedad 34+6–37 GN-i on aktiivsel jälgimisel.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K10 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 10 TõKo ja SoKo tabelit.
Raseduse prolongeerimine (tokolüüs)
42 |
Ähvardava enneaegse sünnituse korral kasutage tokolüüsi kuni 48 tundi loote kopsude ettevalmistuse, neuroprotektsiooni ja transpordi eesmärgil. Tugev positiivne soovitus, kõrge tõendatuse aste |
|
| 43 |
Ähvardava enneaegse sünnituse korral ärge kasutage tokolüüsi üle 48 tunni. Tugev negatiivne soovitus, kõrge tõendatuse aste |
|
| 44 |
Ähvardava enneaegse sünnituse korral ärge kasutage tokolüüsi järgmistes olukordades, kus raseduse prolongeerimine ei ole soovitatav: • surnud loode; • loote eluks sobimatu väärarend; • loote hüpoksia, mis vajab kohest sekkumist; • äge verejooks ja/või ema ebastabiilne hemodünaamika; • raske preeklampsia; • platsenta irdumine; • koorionamnioniit. Tugev negatiivne soovitus, kõrge tõendatuse aste |
|
| 45 |
Ähvardava enneaegse sünnituse korral kasutage tokolüüsiks valikravimina nifedipiini, kui puuduvad vastunäidustused selle ravimi kasutamiseks (vt lisa 5). Tugev positiivne soovitus, kõrge tõendatuse aste |
|
| 46 |
Ähvardava enneaegse sünnituse korral, kui tokolüüsiks on nifedipiini kasutamine vastunäidustatud, võib kasutada beetamimeetikumi (heksoprenaliin), oksütotsiini retseptori antagonisti (atosibaan), tsüklooksügenaasi inhibiitorit (indometatsiin). |
Ei leidu tugevat tõenduspõhisust selle kohta, et tokolüütilised ravimid parandavad perinataalset tulemit. Tokolüütiliste ravimite ja platseebo võrdluses ei ole leitud erinevusi raseduse jätkumise kestuses, neonataalses haigestumises (RDS, IVH), perinataalsete surmade arvus (156–158) ega laste tervise kaugtulemis (9, 24, 89, 155).
Süstemaatilised ülevaated on näidanud, et säilitav tokolüüs (kestusega üle 48 tunni) ei ole kasulik ema ega lapse tervisele ja seetõttu seda ei soovitata. Tokolüüs on vastunäidustatud, kui see võib emale või lapsele kahju teha (9, 89, 155).
Tokolüütiliste ravimitena on kasutusel kaltsiumikanali blokaatorid (nifedipiin), beetamimeetikumid (heksoprenaliin), oksütotsiini retseptorite antagonist (atosibaan) ja tsüklooksügenaasi inhibiitorid (indometatsiin).
Preparaadi valik
Beetamimeetikumid (heksoprenaliin). Praegu kasutatakse Eestis tokolüütiliseks raviks enim beetamimeetikume. Süstemaatiliste uuringute põhjal on leitud, et võrreldes platseeboga on beetamimeetikumid efektiivsemad raseduse pikendamises 48 tunni võrra, kuid ei vähenda RDS-i, perinataalsete ja neonataalsete surmade arvu. Beetamimeetikumidel esineb palju kõrvaltoimeid: valu rindkeres, kopsuturse, ema ja loote tahhükardia, treemor, peavalu. On kirjeldatud raskest kopsutursest tingitud ema surmasid. Beetamimeetikume tuleb kasutada ettevaatusega ja pigem mitte esmavaliku preparaadina (9, 89, 155).
Oksütotsiiniretseptorite antagonistid (atosibaan). Oksütotsiiniretseptorite antagonistid on kõige uuem tokolüütiliste ravimite rühm. Nifedipiiniga võrreldes on leitud raseduse prolongeerimises paremaid tulemusi nifedipiinirühmas, samas on emapoolseid kõrvaltoimeid vähem kirjeldatud atosibaanirühmas (159, 161, 162). Ravijuhendites on soovitatud atosibaani teise valiku preparaadina, kuna tal on kõige vähem kõrvaltoimeid (9, 155). Eestis ei ole atosibaan praegu kättesaadav, seda eelkõige oma kõrge hinna tõttu.
Tsüklooksügenaasi inhibiitorid (indometatsiin). Uuringutega on tõestatud tsüklooksügenaasi inhibiitorite efektiivne tokolüütiline toime võrreldes platseebo ja beetamimeetikumidega. Indometatsiinil on nifedipiiniga analoogne positiivne toime, kuid indometatsiini kasutamine on piiratud, sest põhjustab lootel arterioosjuha sulgumist (163). Lühiajaline kasutamine on ilmselt pöörduva toimega, kuid pikaajaline manustamine võib põhjustada loote ja vastsündinu pulmonaalset hüpertensiooni, loote neerufunktsiooni häireid ja sellest tingitud oligohüdramnioni ning sünni järel NEK-d. Indometatsiini on seetõttu lubatud kasutada vaid lühiajaliselt, enne 28.+0 GN-i, kui teised tokolüütilised ravimid on vastunäidustatud (nt ema südamehaigus) (89).
Ravimite kombinatsioone ei ole soovitatav kasutada, sest kõrvaltoimed võivad kumuleeruda, samuti ei saada paremat ravitulemust (164). Soovituslik raviskeem on toodud lisas 5 (89, 155).
Ravijuhendi ajakohastamisel soovis töörühm täpsustada, kas tokolüüsi vajava ähvardava enneaegse sünnitusega rasedal kasutada ema ja vastsündinu parema ravitulemuse saavutamiseks atosibaani või nifedipiini.
Cochrane’i süstemaatilise ülevaate alusel on kõik tokolüütikumide rühmad (beetamimeetikumid, tsüklooksügenaasi inhibiitorid, kaltsiumkanali blokaatorid, oksütotsiiniretseptorite antagonistid, magneesiumsulfaat, lämmastikoksiidi doonorid) sünnituse edasilükkamises efektiivsemad kui platseebo ja mitteravimine. Neonataalse suremuse osas 28 päeva jooksul ei olnud ükski tokolüütikumide rühm parem kui platseebo. Kõrvaltoimeid esines kõige rohkem beetamimeetikumide ja tokolüütikumide kombinatsioonide rühmas (165).
Nii 2022. aastal avaldatud metaanalüüs kui ka mitmekeskuseline juhuslikustatud kontrolluuring (APOSTEL III) on näidanud, et nifedipiin ja atosibaan on võrdselt efektiivsed 48 tunni tokolüüsiks. Laste tervisenäitajate osas (IVH vähemalt III aste; nekrotiseeriv enterokoliit vähemalt II aste; RDS, mis vajab surfaktanti; laboratoorselt kinnitatud sepsis) erinevust ei leitud. Intensiivravi vajasid vähem need vastsündinud, kelle ema sai tokolüüsi nifedipiiniga. Vastsündinute ravitulemustes olulist erinevust ei leitud. (166, 167)
APOSTEL III uuringu andmetel on tehtud mitu sekundaarset analüüsi. Ajukahjustuste esinemise osas vastsündinutel ei leitud ravimite kasutamisel erinevust (kõrge tõendatuse aste) (168). Samuti ei leitud erinevust laste tervislikus seisundis 2,5–5,5 aasta vanuses (mõõdukas tõendatuse aste) (169).
Kulutõhususe analüüsi põhjal on ravikulu tokolüüsil nifedipiiniga oluliselt tunduvalt väiksem võrreldes atosibaaniga. Ravi maksumus on seotud nii preparaadi enda hinnaga kui ka sellega, et atosibaani kasutamisel satub rohkem vastsündinuid intensiivravisse. (170)
Töörühma hinnangul kasutatakse haiglates tokolüüsiks erinevaid ravimeid. Nifedipiinil on mitmeid kõrvaltoimeid, ka ei sobi ravim juhul, kui sünnitaja on väga hüpotooniline. Tsentraliseerimisel peaks olema võimalik kasutada atosibaani. Indometatsiini kasutamine on tüsistuste ohu tõttu piiratud.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K11 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 11 TõKo ja SoKo tabelit.
Nabaväädi sulgemine
| 47 |
Enneaegse vastsündinu sünni järel oodake nabaväädi sulgemisega võimaluse korral vähemalt 60 sekundit. |
|
| 48 |
Enneaegse vastsündinu nabaväädi sulgemisega ärge oodake, kui vastsündinu või ema vajab kohe elupäästvaid tegevusi. |
|
| 49 |
Enneaegsel vastsündinul, kes on sündinud pärast 28. GN-i, kaaluge nabaväädi lüpsmist kolm-neli korda, kui nabaväädi hiline sulgemine ei ole võimalik. |
|
| 50 |
Enneaegsel vastsündinul kaaluge hilist nabaväädi sulgemist ka juhul, kui ta vajab kohe sünni järel hingamistoetust (kui mõlemat saab teha samal ajal). |
Kui ema on lapse sünni hetkel saanud oksütotsiini, ei ole juhul, kui laps paikneb ema kõhul, platsentaarse transfusiooni mahus erinevust. Lihasesisesi manustatud uterotoonilised ravimid suure tõenäosusega platsentaarset transfusiooni ei mõjuta (177).
Kui ei ole võimalik rakendada nabaväädi hilist sulgemist, võiks alternatiivina kaaluda üle 28+0 GN-i umbes 20 cm pikkuse nabaväädi segmendi lüpsmist lapse suunas kolm-neli korda. Alla 28 GN-i on nabaväädi lüpsmine seotud suurema IVH tekke riskiga (9, 175, 177). Nabaväädi lüpsmine annab sarnaseid tulemusi nabaväädi hilise sulgemisega. Nabaväädi lüpsmine vajab siiski lisauuringuid, et hinnata võimalikku kasu ja kahju täpsemalt (174, 178–180). Emade tervisetulemi kohta andmed peaaegu puuduvad, küll on aga paaris uuringus mainitud, et nabaväädi hilise sulgemise või nabaväädi lüpsmise puhul ei ole komplikatsioonide suurenemist emadel täheldatud (173, 174).
Ravijuhendi ajakohastamisel soovis töörühm täpsustada, kas kõikidel enneaegsetel vastsündinutel võiks kasutada ravitulemuse parandamiseks esmase stabiliseerimise käigus hilist nabaväädi sulgemist ning kas esmase stabiliseerimise käigus tuleks kasutada nabaväädi lüpsmist, kui sulgemisega viivitamine ei ole võimalik.
Rahvusvahelistes juhendites soovitatakse oodata nabaväädi sulgemisega vähemalt 60 sekundit (10, 11, 39).
Hiljuti avaldatud mahukas süstemaatilises ülevaates ja võrgustik-metaanalüüsis leiti, et võrreldes varajase nabaväädi sulgemisega vähendas nabaväädi sulgemine ≥ 120 sekundi vastsündinu suremust enne väljakirjutamist. Samas nii nabaväädi sulgemine 45 kuni < 120 sekundi möödudes ega 15 kuni < 45 sekundi möödudes ei näidanud erinevust ka võrreldes kohese nabaväädi klõmmimisega (esimesel võimalusel või < 15 sekundit). Nabaväädi lüpsmise korral ei leitud samuti erinevust võrreldes varajase nabaväädi sulgemisega. Uurijad arvutasid erinevate sekkumiste tõenäosusliku pingerea. Selle alusel oli ≥ 120 sekundi nabaväädi sulgemine 91% tõenäosusega parim ravi suremuse ennetamiseks enne haiglast väljakirjutamist, lühiajaline, mõõdukas hiline nabaväädi sulgemine ja nabaväädi lüpsmine olid vastavalt suure tõenäosusega paremuselt teine, kolmas ja neljas sekkumine. Varajane nabaväädi sulgemine oli 1% tõenäosusega parim sekkumine ja 53% tõenäosusega halvim sekkumine. Ei leitud märkimisväärseid erinevusi uuritavate karakteristikute lõikes, nagu gestatsioonivanus. Intraventrikulaarse hemorraagia (kõik astmed) osas ei leitud selget erinevust erinevate ravitaktikate võrdlemisel, samuti ei ole selge, kas üks taktika võiks olla teistest oluliselt parem või halvem. (181)
Cochrane’i süstemaatilises ülevaates (182), kus võrreldi hilist nabaväädi sulgemist varase sulgemisega, leiti, et hiline nabaväädi sulgemine tõenäoliselt vähendab vastsündinu surma riski. Ei leitud erinevust raske IVH, PVL-i, kroonilise kopsuhaiguse, RDS-i esinemisel. Hiline nabaväädi sulgemine on tõenäoliselt vähesel määral efektiivne NEK tekkimise vähendamisel. Võrreldes nabaväädi lüpsmist ja varajast nabaväädi sulgemist enneaegsetel vastsündinutel ei leitud tulemusnäitajate vahel erinevust (182).
Töörühm arutas, et võimalusel tuleb oodata nabaväädi sulgemisega nii kaua, kui laps on teinud esimesed hingetõmbed. Samal ajal peab vältima lapse maha jahtumist. Kuigi viimati avaldatud metaanalüüsis leiti, et võrreldes varajase nabaväädi sulgemisega vähendas pikk hiline nabaväädi sulgemine (≥ 120 sekundit) vastsündinu suremust enne väljakirjutamist, siis mitmes uuringus olid kaasatud rohkem kui 30. GN-il sündinud vastsündinud. Nabaväädi hiline sulgemine eeldab elustamislaudade olemasolu sünnitustoas. Otsustati täpsustada olemasoleva soovituse sõnastust selliselt, et nabaväädi sulgemisega oodata võimalusel vähemalt 60 sekundit. Lisaks sõnastati täpsustav soovitus.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K12 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 12 ja 13 TõKo ja SoKo tabeleid.
Kehatemperatuuri kontroll
| 51 |
Enneaegsel vastsündinul tagage seisundi esmase stabiliseerimise käigus normotermia. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
Normotermia tagamine vähendab neonataalsete surmade ja haigestumiste arvu (IVH, PDA sulgemise vajadus, kopsuverejooks, hiline sepsis), eriti sügavalt enneaegsete laste hulgas (183–185). Kõikidel vastsündinutel tuleks tagada kehatemperatuur vahemikus 36,5–37,5 °C (24).
Kehatemperatuuri peab korrektselt jälgima seisundi esmase stabiliseerimise ja protseduuride (surfaktandi manustamine, intubatsioon, veenitee rajamine) tegemise ajal, et vältida hüpertermiat (24). Iatrogeense hüpertermia kaugtulemi kohta andmed puuduvad ning vajalikud on põhjalikumad sellekohased uuringud.
Elustamisjuhendites (176, 186) on normotermia tagamine tugev soovitus. Normotermia tagamiseks tuleb kasutada soojendatud ja niisutatud hingamisgaase, tõsta toatemperatuuri, kasutada radiatsioonsoojendust (lamp, madrats), plastkotte või kinnikatvaid kilesid ning vältida lapse eelnevat kuivatamist (171, 50, 176, 186).
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K13.
Esmane hingamistoetus
| 52 |
Enneaegsel vastsündinul, kes on sündinud enne 30.+0 GN-i ja kellel on respiratoorse distressi sündroomi (RDS-i) kujunemise risk, kasutage seisundi esmasel stabiliseerimisel mitteinvasiivset hingamistoetust (CPAP, NIV). Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 53 |
Enneaegse vastsündinu seisundi esmasel stabiliseerimisel kasutage võimaluse korral kontrollitud rõhuga hingamistoetust (Neopuff või muu T-kontuur või muu CPAP või NIV aparatuur). |
|
| 54 |
Spontaanhingamisel oleva enneaegse vastsündinu seisundi esmasel stabiliseerimisel kasutage CPAP-ravi korral hingamisteedes pidevat positiivset ekspiratoorset lõpprõhku vähemalt 5–6 cm H2O. |
|
| 55 |
Enneaegse vastsündinu seisundi esmasel stabiliseerimisel kontrollitud rõhuga ventileerimisel eelistage inspiratoorset tipprõhku (PIP) 20–25 cm H2O. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 56 |
Enneaegse vastsündinu seisundi esmasel stabiliseerimisel vältige pikendatud sissehingamisaja kasutamist. Nõrk negatiivne soovitus, madal tõendatuse aste |
|
| 57 |
Suurema gestatsioonivanusega enneaegsel vastsündinul võite individuaalse otsusena esmase hingamistoetusena kaaluda HF-i kasutamist. |
Euroopa vastsündinute elustamise juhendis (186) on soovitatud enneaegsete vastsündinute seisundi esmasel stabiliseerimisel pigem kasutada kontrollitud rõhuga ventilatsiooni. Juhuslikustatud uuringus (189) võrreldi kontrollitud rõhuga (T-piece resuscitator, Neopuff ) ja kontrollimata rõhuga (self-inflating bag, Ambu) ventilatsiooni kasutamist. Uuringu tulemusena leiti, et kontrollitud rõhuga ventilatsiooni (Neopuff ) puhul oli väiksem hilisema intubatsiooni vajadus ning alarühma (VLBW-laste) analüüsist selgus BPD esinemise väiksem sagedus kontrollitud rõhuga ventilatsiooni rühmas.
Kopsude avanemiseks, kopsukoe kahjustuse ja alveoolide korduva kollabeerumise vältimiseks on vaja hoiduda suure mahuga (lubatud maht maksimaalselt 4–8 ml/ kg) ventilatsioonist ja vältida kopsude ülevenitust. Tagada tuleb stabiilne PEEP 5–6 cm H2O (176), millega paraneb kopsude venitatavus ja gaasivahetus. Soovitatav inspiratoorne tipprõhk on 20–25 cm H2O.
Uuemates uuringutes, kus on käsitletud pikendatud sissehingamisaja kasutamist esimestel hingetõmmetel (192, 193), on leitud, et pikendatud sissehingamisaja (sissehingamisrõhu hoidmine 15–22 sekundit) kasutamine vastsündinu seisundi sünnijärgsel stabiliseerimisel on efektiivne hingamistoetuse lühiajalisel rakendamisel, vähendades invasiivse ventilatsiooni vajadust esimese 72 elutunni jooksul. Samas ei ole leitud statistiliselt olulist erinevust laste hilistulemites (BPD, surm). Pikendatud sissehingamisaja rühmas esines statistiliselt olulisel määral enam avatud arterioosjuha, mida oli vaja medikamentoosselt või kirurgiliselt sulgeda (193), ja statistiliselt mitteoluliselt rohkem õhktüsistusi (192). Praegu on pikendatud sissehingamisaja kasutamise kohta uuringuid ebapiisavalt, mistõttu ei soovitata seda rutiinselt kasutada.
Ravijuhendi ajakohastamisel soovis töörühm täpsustada, kas enneaegsete vastsündinute esmasel stabiliseerimisel peaks eelistama CPAP-ravi (mitteinvasiivse positiivse ekspiratoorse lõpprõhu kasutamine ilma täiendava sissehingamise toetuseta), kui võrrelda mitteinvasiivse ventilatsiooni või sünkroniseeritud mitteinvasiivse ventilatsiooniga.
Enneaegse vastsündinu esmase hingamistoetuse valikul lähtuti kolmest rahvusvahelisest juhendist (39, 196, 197) ja ühest kohalikust vastsündinu esmase adapatatsiooni toetamist käsitlevast juhendist (198), lisaks viiest süstemaatilisest ülevaatest ja/või metaanalüüsist ning kolmest RCT-st. Rahvusvahelistes ravijuhendites rõhutatakse CPAP tähtsust esmase hingamistoetuse rakendamisel enneaegsetel lastel, kellel on suur risk RDS-i kujunemiseks (s.o alla 30 GN-i), ning positiivse rõhuga ventilatsiooni tuleks kasutada ainult siis, kui on tegemist bradükardia või apnoega. NICE ravijuhendis soovitatakse esmase hingamistoetuse valikuna CPAP-d või HF-i (196). RDS-i juhendis soovitatakse esmase valikuna CPAP-toetust (39), HF-i õnnestumine sõltub kogemusest ja vilumusest. Hõlpsamat ja säästlikumat üleminekut CPAP-lt HF-ile on võimalik rakendada hübriidvormiga aparatuuriga, kus mõlemad funktsioonid on olemas.
Mitteinvasiivsete hingamistoetuse meetoditest võrreldi uuringutes erinevaid meetodeid: CPAP, HF, BiPAP, NIPPV, NIV NAVA, NHFOV. Võrdlus oli keeruline nii seadmete põhimõtete kui ka nende rakendamise heterogeensuse tõttu.
Erinevaid mitteinvasiivseid hingamistoetuse võimalusi omavahel võrreldes (HF, CPAP, BiPAP, NIPPV) oli suremus väikseim HF-i hingamistoetuse korral (201). Samas on erakordselt väikeste enneaegsete puhul eduka ventilatsiooni saavutamine HF-iga esmase hingamistoetusena vähem tõenäoline, kui võrrelda hilisemas gestatsioonivanuses sündinud enneaegsete vastsündinutega (196, 39).
Mitteinvasiivse hingamistoetuse üks eesmärkidest on vältida intubatsiooni ja invasiivset ventilatsiooni, mis omakorda mõjutab BPD esinemissagedust (187, 188). BPD-d esines NIPPV meetodi puhul vähem võrreldes CPAP-ga (199). NIVNAVA vs. NCPAP ja NHFOV vs. NCPAP korral BPD esinemissagedus ei erinenud (200, 201). Samuti ei erinenud BPD esinemissagedus HF-i ja CPAP võrdlemisel (202). BPD esinemissagedus ei erinenud ka BiPAP ja CPAP meetodi vahel (199). NIPPV puhul oli mitteinvasiivse ravi ebaõnnestumise tõenäosus väiksem, õhkrinda ja BPD-d esines vähem kui CPAP puhul (203).
Metaanalüüsis, mis kaasas 22 RCT-d, ei erinenud hingamistoetuse ebaõnnestumine või invasiivse ventilatsiooni vajadus HF-i ja CPAP võrdlusel (204), kuid samas 10 RCT-d käsitleva metaanalüüsi põhjal oli risk ravi ebaõnnestumiseks suurem HF-i puhul võrreldes CPAP-ga (202). Seejuures ei erinenud intubatsiooni vajadus HF-i ja CPAP meetodi puhul (202). HF-i eelis CPAP meetodi ees on väiksem ninakahjustuse ja õhkrinna esinemissagedus. (203, 204) Kasutegur HF-i puhul võrreldes CPAP-ga on vanemate suurem rahulolu lapsega vastastikuse kontakti loomisel (196). HF-i puhul on vanematel kergem last sülle võtta ja parem lapse nägu näha. Lisaks on HF ka hõlpsamini käsitletav, kuid siinkohal on oluline keskuse vilumus ja kogemus HF-i meetodi kasutamisel.
NIPPV-l oli väiksem ravi ebaõnnestumise sagedus ja lühem invasiivse ventilatsiooni vajadus võrreldes CPAP-ga (199, 203). Ka BiPAP-l oli ravi ebaõnnestumine tõenäosus väiksem, kui võrrelda CPAP-raviga (203).
NIV NAVA vs. NCPAP uuringud esmasel hingamistoetusel on olnud väikesed. Vahetult sünni järel rakendatud NIV NAVA meetodit on rakendatud väga väikeses RCT-s (N = 20) (205) esmase stabiliseerimise käigus, kahes teises RCT-s esimese kahe ööpäeva jooksul. NIV NAVA vs. NCPAP meetodeid käsitlevates uuringutes ei olnud erinevust intubatsiooni vajaduse osas, samuti ei erinenud nende meetodite puhul õhkrinna esinemine (200, 206).
NHFOV režiimil olnud vastsündinutel oli esimese 72 tunni jooksul intubatsiooni vajadus väiksem kui CPAP-ravil olnud vastsündinutel. Õhkrinna või NEK esinemises NHFOV ja NCPAP meetodite vahel erinevust ei olnud (207).
Erakordselt väikeste enneaegsete puhul oleks seega esmase hingamistoetusena ravi õnnestumisel suurem tõenäosus NIPPV-l ja suuremate enneaegsete puhul on spetsialiseeritud keskustes eelistatud HF-i hingamistoetus. Rahvusvaheliste juhendite põhjal on aga CPAP jätkuvalt esmane valik väga väikese enneaegse esmase hingamistoetuse rakendamisel.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K14 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 14 TõKo ja SoKo tabelit.
Esmane hingamistoetus (hapniku kontsentratsioon, FiO2)
| 58 |
Enneaegse vastsündinu esmasel stabiliseerimisel hingamistoetuse rakendamisel valige hapniku osakaalu algväärtus sissehingatavas õhus sõltuvalt gestatsiooninädalast sünnil: - alates 32+0 GN-i 21% hapnikku; - 28+0–31+6 GN-i 21–30% hapnikku; - enne 28 GN-i 30% hapnikku. |
|
| 59 |
Enneaegsel vastsündinul, kellel puudub efektiivne vereringe ja kui rakendatakse kaudset südamemassaaži, eelistage hapniku osakaalu sissehingatavas õhus 100%. |
Metaanalüüsides ei leitud hapniku väiksema kontsentratsiooniga rühma ja hapniku suurema kontsentratsiooniga rühma võrdlemisel statistilist erinevust suremuses ega haigestumuses (BPD, IVH, ROP) (208, 209). 2014. aastal avaldatud juhuslikustatud kontrolluuringus ei leitud enneaegsetel vastsündinutel, keda oli esmase hingamistoetuse käigus abistatud 30% või 65% hapnikuga, BPD esinemise sageduse ja oksüdatiivse stressi markerite erinevusi. Järeldati, et FiO2 0,3 on niisama ohutu kui FiO2 0,65 (210). 2015. aastal avaldatud juhuslikustatud kontrolluuringus uuriti ruumiõhuga või 100% hapnikuga elustatud enneaegsetel vastsündinutel oksüdatiivse stressi markerite erinevusi ning leiti, et ruumiõhuga elustatud vastsündinutel esines 12 tunni vanuselt väiksem oksüdatiivse stressi markerite suurenemine seerumis (211).
2015. aastal avaldatud Euroopa elustamisjuhendis on soovitatud FiO2 tiitrida, et saavutada preduktaalne saturatsiooninäit, mis vastab ajaliste tervete vastsündinute varajase sünnijärgse saturatsiooni väärtuse 25. tsentiilile. Vt joonist 1 (212).
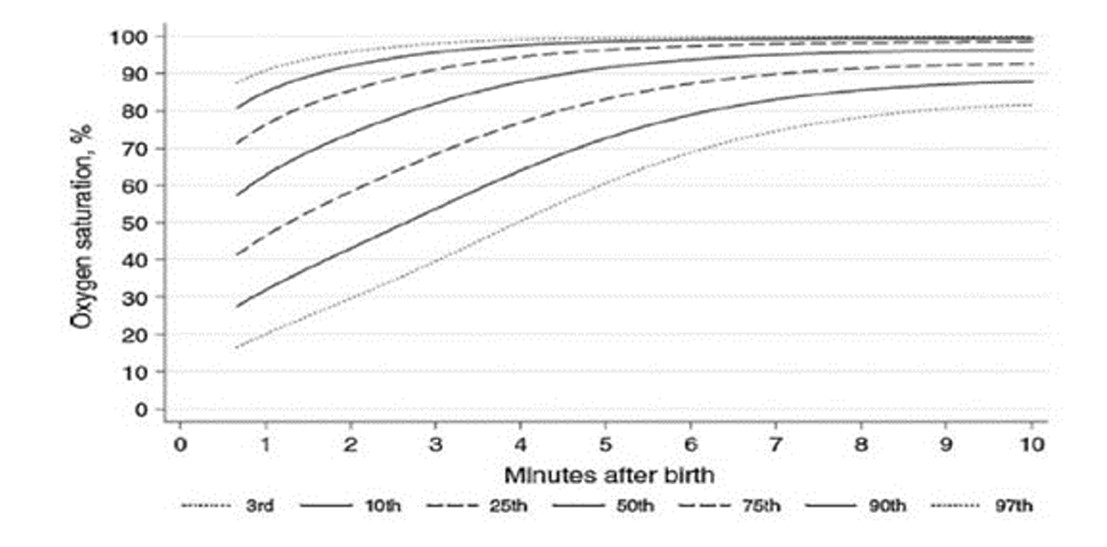
Ravijuhendi ajakohastamisel avati algne kliiniline küsimus, et analüüsida uuemat tõendusmaterjali. Leidus mitmeid metaanalüüse ja juhuslikustatud uuringuid.
Enneaegsena sündinud laste haiglasuremus ei ole erinev, kui võrrelda madalama (< 0,4) ja kõrgema (> 0,4) hapnikufraktsiooniga esmaselt stabiliseeritud rühmasid (213). Kolmel juhuslikustatud uuringul põhinevas metaanalüüsis, mis hõlmas 543 enne 32. GN-i sündinud enneaegset vastsündinut, ei leitud seost esmasel stabiliseerimisel kasutatud FiO2 ja kahe aasta suremuse ja/või neuroloogilise puude esinemise vahel (214). Samale tulemusele on jõutud ka teistes juhuslikustatud uuringutes (215, 216).
Kaheksal juhuslikustatud uuringul põhinevas metaanalüüsis ei leitud erinevust BPD, IVH, ROP, PDA ega NEK esinemissageduses enne 29. GN-i sündinud enneaegsete vastsündinute seas, keda esmasel stabiliseerimisel abistati madalama kuni 30% või kõrgema üle 60% hapniku kontsentratsiooniga (217). Enneaegsete vastsündinute esmane abistamine õhuga võrrelduna 100% hapnikuga on seotud väiksema oksüdatiivse stressi molekulaarsete muutustega 12 esimese elutunni jooksul (218).
Hiljutises Euroopa konsensusdokumendis soovitatakse enne 28. GN-i sündinud enneaegsete vastsündinute esmasel stabiliseerimisel kasutada 30% hapnikku, 28.–31. nädalal sündinud enneaegsetele 21–30% hapnikku ja üle 32 nädala sündinud enneaegsetele 21% hapnikku (39). Hapniku kontsentratsiooni tuleks tiitrida, et saavutada pulseoksümeetriga mõõdetav preduktaalne SpO₂ > 80% viiendaks eluminutiks, kuna madalamate saturatsioonide korral on ravitulemused halvemad (214).
Vereringeseiskuse korral, kui on vajalik kõikide elustamisvõtete, sh kaudse südamemassaaži rakendamine, peaks kasutama 100% hapnikku, et tagada hapniku jõudmine kudedesse. Eetilistel kaalutlustel ei saa teha vastsündinutel juhuslikustatud kontrolluuringuid elustamissituatsioonis erineva hapniku kontsentratsiooni kasutamisega. Loomkatsete tulemused, kus võrreldakse kõrge ja madala hapniku kontsentratsiooni kasutamist kaudset südamemassaaži vajavatel vastsündinutel, toetavad pigem madalama hapniku kontsentratsiooni kasutamist (197, 219). Loommudelil on näidatud ka pulssoksümeetria ebausaldusväärsust kaudse südamemassaaži tingimustes (220).
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K15 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 15 TõKo ja SoKo tabelit.
Esmane hingamistoetus (saturatsioonipiirid, SpO2)
| 60 |
Enneaegsel vastsündinul, kes on sündinud enne 32.+0 GN-i, tiitrige hapniku kontsentratsioon sissehingatavas õhus, et pulssoksümeetril mõõdetuna parema käe randmel tõuseks saturatsioon (SpO2) viie minuti jooksul pärast sündi järkjärgult üle 80%. |
|
| 61 |
Enneaegsel vastsündinul hoidke hapnikravi kasutamisel SpO2 väärtused 90–95% juures. |
|
| 62 |
Enneaegse vastsündinu saturatsiooniväärtuse jälgimiseks võib kasutada FiO2-SpO2 automaatse korrigeerimise aparatuuri. Praktiline soovitus |
Enneaegsete vastsündinute jaoks ei ole optimaalne hapniku saturatsioon teada. Varajane hapnikravi on otseselt seotud ROP ja vähemal määral BPD tekkega. Sünnijärgses üleminekufaasis peaks pulssoksümeetrial mõõdetud SpO2 paremal randmel tõusma järk-järgult 60%-lt 80%-ni umbes viie minuti jooksul pärast sündi ning umbes kümnendaks eluminutiks jõudma > 85%-ni. SpO2 väärtuste kõikumised on samuti seotud ROP tekke suurenenud riskiga, mistõttu on Euroopa neonataalse RDS-i ravijuhendis soovitatud pärast surfaktantravi vältida hüperoksilisi SpO2 tõuse (171).
Euroopa RDS-i ravijuhendi ja metaanalüüside alusel tuleks eelistada enneaegsetel vastsündinutel kõrgemat saturatsioonipiiri (SpO2 90 –95%). Madalama saturatsioonipiiri (85–89%) kasutamisel esines oluliselt vähem rasket ROP-d (221, 222), kuid võrreldes kõrgema saturatsioonipiiri kasutamisega suurenes oluliselt suremus ja NEK esinemise sagedus (171, 223). 2015. aasta alguses avaldatud metaanalüüsist (224) selgus, et kõrgema saturatsioonivahemiku rühma suremus oli kojukirjutamise hetkel väiksem, kuid tulemuse tõenduspõhisus GRADE- süsteemi alusel on madal. Samuti esines suurema saturatsioonivahemiku rühmas vähem NEK-d. Kaugtulemites (surm/puue, BPD, kuulmislangus, psühhomotoorne areng, ROP 24 elukuu vanuses) kahe rühma vahel erinevust ei olnud. Seega jääb nimetatud metaanalüüsile tuginedes ebaselgeks, milline on optimaalne SpO2 vahemik hapnikravil olevate enneaegsete laste jaoks.
Rutiinselt jälgib lisahapnikku vajavatel vastsündinutel saturatsiooniväärtust õenduspersonal ning selle hoidmiseks etteantud piirides kas vähendatakse või suurendatakse hapniku kontsentratsiooni sissehingatavas õhus. Et parandada kinnipidamist etteantud saturatsiooniväärtustest ning vähendada õenduspersonali töökoormust, on loodud automaatsed SpO2-FiO2 korrigeerimise süsteemid. FiO2- SpO2 automaatse korrigeerimise süsteemi efektiivsuse ja ohutuse kohta võrreldes FiO2 manuaalse reguleerimisega ei ole suuri juhuslikustatud kontrolluuringuid ega metaanalüüse avaldatud. Väikestes uuringutes on näidatud, et FiO2 korrigeerimise automaatne süsteem pikendab oluliselt aega, mil saturatsiooniväärtus püsib etteantud piirides, ning lühendab hüperoksia aega, samas esines SpO2- FiO2 automaatse kontrolli ajal enam hüpoksilisi episoode. Sekkumise mõju neuroloogilisele kaugtulemile uuringutes seni hinnatud ei ole. Automaatsed SpO2- FiO2 korrigeerimise süsteemid võivad potentsiaalselt vähendada suure riskiga enneaegsete haigestumist ning oluliselt vähendada õenduspersonali töökoormust. (225–229)
Ravijuhendi ajakohastamisel avati algne kliiniline küsimus, et analüüsida uuemat tõendusmaterjali. Enneaegsete vastsündinute esmaseks stabiliseerimiseks erineva FiO2 kasutamist võrdlevatest uuringutest on leitud, et viienda eluminuti SpO2 > 80% ennustab väiksemat suremust, väiksemat puude esinemissagedust ja paremat kognitiivset võimekust. See seos on tulnud välja teisele uurimisküsimusele suunatud uuringutest, mistõttu peab tõendust hindama kaudseks ja mitte kaalukaks. (214, 215)
Enneaegsete vastsündinute edasises ravis on leitud, et väiksemad SpO2 eesmärkväärtused (85–89%) võrreldes suurematega (91–95%) ei mõjutanud suremuse või raske puude komposiittulemit ega raske puude esinemist kogu enneaegsete populatsioonis, küll aga suurendasid suremust ja NEKi esinemissagedust väga väikestel enneaegsetel vastsündinutel (230). Erinevad SpO2 eesmärkväärtused 85% ja 95% vahel ei mõjutanud enneaegsete laste kasvukiirust ega kasvus mahajäämust (231). Enneaegsete vastsündinute hulgas, kes olid SGA, mõjutas SpO2 eesmärkväärtus suremust tuntavalt – suremus oli rohkem kui kaks korda suurem väiksema (85–89%) SpO2 eesmärkväärtuse rühmas (232).
Väiksemate SpO2 eesmärkväärtuste korral on enneaegsete vastsündinute suremus suurem, aga ravi vajavat retinopaatiat esineb vähem (214). Arvestades, et madalamad SpO2 eesmärkväärtused on seotud väga väikeste ja SGA enneaegsete gruppides kõrgema suremusega, soovitatakse kasutada suuremaid SpO2 eesmärkväärtusi (90–95%).
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K16 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 16 TõKo ja SoKo tabelit.
Surfaktant
Profülaktiline surfaktantravi
| 63 |
Kõikidel enneaegsetel vastsündinutel ärge kasutage profülaktilist surfaktantravi. Tugev negatiivne soovitus, mõõdukas tõendatuse aste |
|
| 64 |
Kõikidele enne 30.+0 GN-i sündinud enneaegsetele vastsündinutele, kes vajavad esmase stabiliseerimise käigus intubatsiooni, manustage surfaktanti. |
Euroopa RDS-i ravijuhend 2013 (171), Ameerika surfaktantravi juhend 2013 (175) ja Ameerika Pediaatrite Akadeemia kliiniline juhend (235) annavad soovitused nii profülaktilise kui ka selektiivse surfaktantravi kasutamiseks enneaegsetel vastsündinutel, kellel on RDS või selle kujunemise risk. Varajane selektiivne surfaktantravi võiks olla standard.
Enne rutiinse CPAP-toetuse ajastut tehtud uuringud on näidanud väiksemat suremust ja õhulekete esinemise riski enneaegsetel vastsündinutel, kellele manustati profülaktilist surfaktanti, võrreldes ravi eesmärgil surfaktanti saanud lastega (242). 2012. aasta metaanalüüsis, mis hõlmas uuringuid, kus CPAP-toetust kasutati rutiinselt, ei ilmnenud enam profülaktilise surfaktantravi mõju suremuse ja õhulekkesündroomide vähenemisele. Lisaks oli profülaktilist surfaktantravi saanud vastsündinutel BPD esinemise sagedus ja suremus suurem võrreldes lastega, kelle seisundi stabiliseerimiseks kasutati CPAP-toetust. Profülaktilise surfaktantraviga vähenes IVH ja raske IVH esinemise risk, kuid ROP, PDA ja PVL-i haigestumuses olulisi erinevusi ei esinenud (243).
Algses ravijuhendis soovitati kasutada profülaktilist surfaktanti teatud juhtudel (sh erakordselt enneaegsel lapsel, kelle emale ei ole manustatud enne sünnitust GKS-i ja/või kes vajab esmase seisundi stabiliseerimise käigus intubatsiooni (171, 234, 235). Samuti soovitati enneaegsetel vastsündinutel vahetult sünni järel alustada CPAP-toetust koos edasise selektiivse surfaktantraviga alternatiivina tavapärasele intubatsioonile ja profülaktilisele või varajasele surfaktantravile (243–246).
Ravijuhendi ajakohastamisel avati algne kliiniline küsimus, et analüüsida uuemat tõendusmaterjali. Uue RDS-i juhendi (39) alusel soovitatakse enneaegsel vastsündinul alla 30+0 GN-i kasutada surfaktanti, kui ta vajab intubatsiooni esmase stabiliseerimise käigus. Ravijuhendi soovitused on viidud vastavusse RDS-i juhendiga.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K19 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 19 TõKo ja SoKo tabelit.
Varajane CPAP-ravi ja varajane surfaktantravi
| 65 |
Kuni 30.+0 GN-il sündinud enneaegsel vastsündinul, kellel on hingamishäire ja kes ei vaja invasiivset hingamistoetust, alustage varast CPAP-ravi. Tugev positiivne soovitus, kõrge tõendatuse aste |
SUPPORT-uuringus võrreldi esimesel elutunnil rakendatud CPAP-toetust profülaktilise surfaktandi ja KKV-ga raseduskestuse korral 24+0–27+6 GN-i sündinud enneaegsetel. Gestatsioonivanuses 24+0–25+6 GN-i sündinud vastsündinute suremus oli CPAP rühmas väiksem kui profülaktilise surfaktandi rühmas. Kaks kolmandikku CPAP rühma lastest vajas hiljem surfaktanti, kuid nende KKV aeg oli lühem ja nad vajasid vähem postnataalseid steroide võrreldes profülaktilise surfaktandi rühmaga. Õhulekete ega BPD tekkimise erinevust ei olnud (246). Kuigi Colombian Networki uuringus (244) oli CPAP rühmas pneumotooraksi risk suurem kui INSURE rühmas (9% vs. 2%), näitasid SUPPORT ja teised uuringud, et CPAP, alustatuna kiiresti pärast sündi, on efektiivne ja ohutu alternatiiv profülaktilisele või varajasele surfaktantravile (246, 248). Varajane CPAP ja selektiivne INSURE vähendasid KKV ja surfaktandi vajadust (249). Raseduskestuse korral kuni 30+0 GN-i sündinud enneaegsetel, kes ei saanud invasiivset hingamistoetust, oli metaanalüüsi alusel väiksem risk surra või haigestuda BPD-sse, ilma et suureneks raske IVH risk (187).
Kuna RDS-iga enneaegsed vastsündinud erinevad küpsusastmelt ja RDS-i raskusastmelt, on vaja patsientide käsitlus individualiseerida. CPAP-toetus kohe pärast sündi koos vajaduse korral selektiivse surfaktantraviga INSURE meetodil või LISA meetodil võiks olla rutiinne alternatiiv intubatsioonile ja profülaktilise surfaktandi manustamisele. See vähendab surfaktantravi vajadust ja KKV kestust väga väikese sünnikaaluga enneaegsetel vastsündinutel, suurendamata haigestumise ja surma riski (187, 243, 249–252).
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K21.
Surfaktantravi
| 66 |
Enneaegsel vastsündinul, kellel süvenevad RDS-i kliinilised tunnused ja FiO2 on > 0,3 CPAP hingamistoetusel rõhuga ≥ 6 cm H2O või kopsu ultraheliuuringu leid ennustabsurfaktandi vajadust, kasutage varast surfaktantravi. |
|
| 67 |
Mitteinvasiivsel hingamistoetusel oleval enneaegsel vastsündinul manustage surfaktanti peenikese kateetri teel. |
|
| 68 |
Enneaegsel vastsündinul kaaluga üle 1 kg võib alternatiivina manustada surfaktanti kõrimaski kaudu. |
|
| 69 |
RDS-iga enneaegsel vastsündinul kasutage eelistatult naturaalset surfaktanti (vt lisa 6). Tugev positiivne soovitus, kõrge tõendatuse aste |
|
| 70 |
RDS-iga enneaegsel vastsündinul kasutage võimalikult kontsentreeritud surfaktandipreparaati (poraktant alfa). Annustamine: poraktant alfa algannus 200 mg/kg, korduv annus 100 mg/kg. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 71 |
Enneaegsel vastsündinul, kelle RDS on raske kuluga ning püsib oluline lisahapniku ja/või invasiivse hingamistoetuse vajadus, on näidustatud surfaktandi korduv manustamine intervalliga vähemalt kuus tundi, kokku mitte rohkem kui kolm annust. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
Ravijuhendi ajakohastamisel vaadati üle tõendusmaterjal enneaegse vastsündinu kopsu ultraheliuuringu kohta. Kopsu ultraheli skoorid ennustavad hästi enneaegsete vastsündinute surfaktandi vajadust ning ultraheli skooride järgi surfaktandi manustamine on varasem kui hingamistoetuse vajaduse järgi surfaktandi manustamine. (253, 254)
Paljudes varasemates uuringutes on surfaktanti manustatud klassikalisel meetodil ehk intubatsioonitoru kaudu, mille puhul vastsündinu on invasiivsel hingamistoetusel. Pikemaajalist invasiivset ventilatsiooni saab vältida, kasutades INSURE või LISA meetodit. Juhuslikustatud uuringutes on näidatud, et INSURE meetodi rakendamine vähendab pikemaajalise invasiivse hingamistoetuse vajadust ja edaspidi BPD esinemise sagedust (255, 256). Mida varem on tehtud otsus kasutada INSURE meetodit, seda suurem on võimalus KKV-d vältida, kuigi kulub rohkem surfaktanti (248).
Ravijuhendi ajakohastamisel vaadati üle uuem tõendusmaterjal INSURE ja LISA meetodi kohta. Intubatsiooni vältimiseks on soovitatav kasutada minimaalselt invasiivseid meetodeid, nagu INSURE või LISA. Viimastel aastatel on LISA meetodi eeliseid INSURE ees kinnitanud mitmed uuringud. 2017. aasta metaanalüüsis (257), kuhu kaasati kuus RCT-d (n = 895), leiti, et LISA meetodi puhul oli väiksem mehaanilise ventilatsiooni vajadus esimese 72 tunni jooksul pärast sündi ning vähem esines BPD-d ja suremus oli väiksem kui INSURE meetodiga ravitud lastel. Hilisemas, 2024. aasta metaanalüüsis (258) (16 RCT-d, n = 1944) leiti, et LISA meetodi eelisteks on lisaks lühemale mehaanilisele ventilatsiooni vajadusele ja BPD ning suremuse vähenemisele väiksem pneumotooraksi ja periventrikulaarse-intraventrikulaarse hemorraagia (PIVH) esinemissagedus võrreldes nende lastega, keda raviti INSURE meetodiga.
Kuue juhuslikustatud uuringu metaanalüüs ja üks hilisem juhuslikustatud uuring (259, 260) näitasid, et kõrimaski kaudu surfaktandi manustamine on mehaanilise ventilatsiooni vajaduse ärahoidmiseks sama efektiivne kui standardmeetodil (INSURE) surfaktandi manustamine.
Uuringute järgi on naturaalsel surfaktandil parem pindaktiivsus ja jaotuvus alveoolide pinnal kui sünteetilisel proteiinivabal surfaktandil (242). Võrdlevates juhuslikustatud kontrolluuringutes on naturaalse surfaktandiga ravimisel väiksem hapnikuvajadus ning pneumotooraksi, BPD ja surma risk (171, 234, 135, 261–264). Naturaalse surfaktandiga on väike võimalus mõne haiguse ülekandmiseks, võivad esineda religioossed ja kultuurilised vastuolud (265).
Euroopas 2013. aastal litsentseeritud surfaktandi preparaadid ja nende annused (171) on toodud lisas 6.
Enneaegse vastsündinu hingamispuudulikkuse raviks vajalik fosfolipiidi annus on 100 mg/kg, aga on farmakokineetilisi ja kliinilisi uuringuid, mis näitavad, et annusel 200 mg/kg on pikem poolestusaeg ning kiirem ja efektiivsem kliiniline vastus (171, 234). Enneaegsete vastsündinute ravis tuleb väiksema mahu tõttu eelistada võimalikult kontsentreeritud preparaati (praegu poraktant alfat).
Kolme ravijuhendi alusel võib korduv surfaktandi manustamine teatud juhtudel olla vajalik (171, 50, 239). Kliiniliselt raske kuluga RDS-i korral on kahe annuse surfaktandi manustamisel olnud parem mõju kui ühe annuse kasutamisel – täheldati oksügenatsiooni paranemist, vähenesid ventilatsiooni vajadus, NEK- sse haigestumise risk ja suremus (239). Kuni kolme annuse poraktant alfa manustamine võrreldes ühekordse annusega vähendas raske kuluga RDS-iga enneaegsete vastsündinute suremust ja õhulekete esinemise sagedust (266). Surfaktantravi Ameerika juhendi järgi võiks surfaktandi manustamise intervall olla 6–24 tundi (134). Rootsi ravijuhendis on soovitatud surfaktandi kordusannust 8–12 tundi pärast eelmise surfaktandi manustamist juhul, kui püsib kopsuhaigusest tingitud oluline lisahapniku vajadus (50). RDS-i Euroopa ravijuhendis on peetud otstarbekaks surfaktanti korduvalt manustada paindliku skeemi alusel, lähtudes lapse seisundist ja lisahapniku vajadusest; seda seisukohta toetavad ka tänapäevased farmakokineetilised andmed (171, 267, 268).
Ravijuhendi ajakohastamisel soovis töörühm täpsustada, kas hingamishäiretega enneaegsel vastsündinul kasutada parema ravitulemuse saavutamiseks varast surfaktantravi võrreldes hilise surfaktantraviga. Üks juhuslikustatud uuring 305 enneaegse vastsündinuga, kellel võrreldi INSURE meetodil surfaktandi varast manustamist hilisema manustamisega, ei näidanud olulist erinevust reintubatsioonivajaduse ja 36. postmenstruaalnädalal hapniksõltuvuse osas. (269)
Surfaktantravi ajakohastatud soovitused on sõnastatud 2022. aastal uuendatud Euroopa RDS-i ravijuhendi järgi (39).
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtteid EvSu K20-1 ja K20-2 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 20 TõKo ja SoKo tabelit.
Kofeiinravi
| 72 |
Enneaegsel vastsündinul kasutage kofeiinravi, et apnoed ennetada ja ravida ning invasiivsest hingamistoetusest võõrutada. |
|
| 73 |
Kõikidel enneaegsetel vastsündinutel, kes on sündinud enne 30.+0 GN-i, kasutage rutiinselt kofeiinravi. Alustage kofeiinravi nii vara kui võimalik, enne kolmandat elupäeva. |
|
| 74 |
Kõikidel enneaegsetel vastsündinutel, kellel esineb apnoe, kaaluge kofeiinravi kasutamist. |
|
| 75 |
Kõikidel enneaegsetel vastsündinutel annustage kofeiintsitraati järgmiselt: veeni või suu kaudu on soovituslik küllastusannus 20 mg/kg ööpäevas; säilitusannus 5–10 mg/ kg ööpäevas, mida võib suurendada apnoede püsimisel kuni 20 mg/kg-ni ööpäevas ühekordse annusena. [AJAKOHASTATUD 2026] Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 76 |
Enneaegsel vastsündinul postmenstruaalvanuses 33–35 nädalat kaaluge kofeiinravi lõpetamist, kui vastsündinu on kliiniliselt stabiilne. |
Metüülksantiine (kofeiintsitraat, aminofülliin, teofülliin) on kasutatud 1970. aastatest enneaegsete laste apnoede ennetamiseks ja raviks ning invasiivsest hingamistoetusest võõrutamiseks (270).
Kofeiinravi parandab võrreldes platseeboga enneaegsete laste varast ravitulemust. Kaks metaanalüüsi näitavad, et metüülksantiinide kasutamine vähendab apnoede esinemise sagedust, ekstubatsioonide ebaõnnestumist ning invasiivse hingamistoetuse vajadust kahe kuni seitsme päeva jooksul pärast ravi alustamist (270, 271). Kofeiinravi rakendamisel võrreldes mitterakendamisega väheneb PDA ligeerimise vajadus ning postmenstruaalvanus, mil viimati esineb lisahapniku, intubatsiooni ja invasiivse ventilatsiooni vajadus (270, 272).
Selle valdkonna olulisimas juhuslikustatud kontrolluuringus, mis hõlmas 500–1250 g sünnikaaluga lapsi, esines kofeiintsitraati saanud lastel võrreldes kontrollrühmaga oluliselt vähem BPD-d ning positiivse rõhuga ventilatsioon lõpetati nädal varem. Küll aga esines kofeiinravirühmas võrreldes kontrollrühmaga väiksem positiivne kaaluiive esimesel kahel elunädalal (272). Kofeiini manustamist seisundi esmase stabiliseerimise käigus on käsitletud vaid ühes uuringus, kus uuriti 21 gestatsionivanusega alla 29+0 GN-i sündinud last. Leiti, et varajase (< 2 tunni vanuses) ja hilise/rutiinse (12 tunni vanuses) kofeiini manustamise vahel ei esine hilisema intubatsiooni vajaduses erinevust. Samas oli varajasemal kofeiini manustamisel positiivne mõju hemodünaamikale (273).
Juhuslikustatud kontrolluuringutes on näidatud, et kofeiiniravi saanud lastel esines 18–21 kuu vanuses vähem CP-d ja kognitiivse arengu defitsiiti kui kofeiinravi mittesaanud lastel (171, 274). Viie aasta vanuses see erinevus küll kadus, kuid võib järeldada, et kofeiinravi on ohutu ega põhjusta olulisi elukvaliteeti mõjutavaid kesknärvisüsteemi kõrvaltoimeid (275). Kofeiinravist saavad enam neuroprotektiivset kasu hingamistoetust vajavad vastsündinud (276). Kofeiinravi toimemehhanism neuroloogilisele kaugtulemile on ebaselge. Kofeiini saanud laste ajus esinesid difusioonimuutused, mis viitavad paremale valgeaine mikrostruktuursele arengule, ning need muutused ei ole vahendatud ainult BPD esinemise vähenemise kaudu (277).
Esmavalikuna soovitatakse kasutada kofeiintsitraati, mis on teofülliini ja aminofülliiniga võrreldes vähem toksiline ning mille kõrvaltoimete profiil on parem (270). Kofeiintsitraadi farmakokineetlised uuringud jäävad 1970.–1980. aastatesse. Traditsiooniliselt alustatakse ravi küllastusannuses 20 mg/kg ööpäevas (vastab kofeiinalusele 10 mg/kg ööpäevas) ning jätkatakse säilitusannuses 5–10 mg/kg ööpäevas veeni või suu kaudu. Kofeiini biosaadavus suukaudsel manustamisel on 100%, seega võib esimesel võimalusel minna üle suukaudsele ravimivormile (278). Suurem kofeiintsitraadi annus periekstubatsiooni perioodis (küllastusannus 40–80 mg/kg ööpäevas ning säilitusannus 20 mg/kg ööpäevas) võrreldes tavaannusega vähendab oluliselt ebaõnnestunud ekstubatsioonide ja enne 28 GN-i sündinud lastel oluliselt invasiivse hingamistoetuse päevade arvu (279), apnoede esinemise sagedust ning apnoepäevade arvu (280). Suurema annuse rühmas esines oluliselt rohkem tahhükardiat, kuid oluliste kõrvaltoimete (surm, oluline neonataalne haigestumine, surm või raske puue 12 kuu vanuses) esinemise sagedus ei suurenenud (280).
Kofeiini kontsentratsiooni jälgimine raviefekti olemasolu ja toksiliste sümptomite puudumise korral ei ole otstarbekas (278–281).
Ravijuhendi ajakohastamisel avati algse juhendi kliiniline küsimus, et analüüsida uuemat tõendusmaterjali. CAP uuringus, mis on kofeiinravi nurgakivi enneaegsete apnoe ravis ja kus võrreldi kofeiintsitraatravi platseeboga, selgus, et varem kui 31. GN-il sündinud enneaegsetel vastsündinutel vähenes kofeiinravi puhul BPD esinemissagedus, tserebraalparalüüsi esinemine 18–21 kuu vanuses ning motoorsete häirete esinemine 11 aasta vanuses, kui võrrelda platseeborühmas olnud lastega. (282)
Kofeiinravi varajase vs. hilise alustamise osas keskenduvad uuringud peamiselt kofeiinravi alustamisele enne kahe-kolme päeva vanust võrreldes ravi alustamisega peale teist-kolmandat elupäeva. BPD ja hiliste neuroloogiliste arengunäitajate mõttes oli varajase ravi alustamisel eelis hilise alustamise ees (10; 283, 284).
18–24 kuu korrigeeritud vanuses esines vähem rasket neuroloogilist arenguhäiret enneaegsetel alla 29. GN-i esimese kahe päeva jooksul alustatud rühmas võrreldes nende lastega, kellel alustati ravi peale kaht päeva (285).
IVH ja PVL esines varajase kofeiinravi alustamisel vähem võrreldes hilise kofeiinravi alustamisega (286). Nii PDA esinemissagedus kui ka kirurgilist ravi vajav PDA esinemissagedus oli väiksem varajase kofeiinravi alustamise puhul, kui võrrelda hilise kofeiinravi alustamisega (286). ROP-d esines samuti vähem varajase kofeiinravi alustamisel võrreldes hilise kofeiinravi alustamisega (286). Varajane kofeiinravi alustamine ei suurendanud NEK esinemissagedust (286). Eri kofeiiniannuste vahel ei olnud erinevust NEK esinemises (10, 287, 283), kuid NEK-d esines vähem neil alla 30 GN-i enneaegsetel, kes said kofeiinravi pikemalt (üle 30 päeva), võrreldes alla 15 päeva kestnud raviga (10).
Nii RDS-i kui ka NICE ravijuhendi koostajate töörühm soovitab kliinilise kogemuse ja esialgse CAP uuringu põhjal kofeiinravi alustada võimalikult varakult, juba intensiivravi osakonda hospitaliseerimisel (10, 39).
Kofeiintsitraatravi annustamise aluseks on jätkuvalt CAP uuring, kus kofeiintsitraadi küllastusdoos oli annuses 20 mg/kg ja säilitusdoos 5–10 mg/kg ööpäevas (272, 282). Erinevaid skeeme võrdlevad uuringud (suur vs. väike annus) varieeruvad uuringuti nii küllastudoosi kui säilitusannuse osas (varieeruvus 20–80 mg/kg ööpäevas ja 5–20 mg/kg ööpäevas vahel) (287, 288, 289).
Ekstubatsiooni õnnestumise ja apnoehoogude vähenemise osas on suurem eelis kofeiini suurel annusel võrreldes väikse annusega. BPD risk on samuti väiksem suurema kofeiiniannuse puhul võrreldes väikse annusega (283, 287, 288).
Kuivõrd metaanalüüsides kofeiinravi suure ja väikse annuse vahel IVH või PVLi puhul erinevust ei esinenud (287, 288), siis suure annuse ja standardannusega üksikuuringus oli suurem tserebellaarse verevalumi sagedus suure annuse puhul
(289) ning suurem krambivalmidus (290).
Tserebraalparalüüsi esinemisel ei olnud kahe aasta vanuses erinevust suures doosis kofeiinravi saanute ja standardannuses kofeiinravi saanute vahel. Kaugtulemis ei olnud viie aasta vanuses suure ja standardannuse kofeiinravi vahel neuroloogilistes arenguhäiretes erinevusi (289).
Kofeiintsitraatravi kõrvaltoimetest esineb tahhükardiat suurema annuse puhul rohkem, kui võrrelda väikse annusega. Teistes kõrvaltoimetes (elektrolüütide kõrvalekalded, toitmisraskused, hüpertensioon, hüperglükeemia, rahutus) ei olnud kofeiinravi suure ja väikse annuse vahel erinevust (287).
Kui ravitulem ei ole saavutatud 10 mg/kg ööpäevas säilitusdoosis, võib vajadusel suurendada kofeiintsitraatravi säilitusannust kuni 20 mg/kg-ni ööpäevas. Erandjuhtudel võib kaaluda doseerimist üle 20 mg/kg ööpäevas säilitusannuses, kuid sellisel juhul on näidustatud ravimi kontsentratsiooni määramine veres. Kofeiintsitraatravi puhul rutiinne ravimi monitooring veres ei ole vajalik. Tänu pikale poolestusajale ei ole doosi vaja jagada päevas kahte annusesse.
Töörühma hinnangul on analüüsitud tõendusmaterjali alusel kofeiinravil väga väikestele enneaegsetele vastsündinutele neuroprotektiivne toime. Uuringute põhjal on leitud nii varajane kui hiline positiivne ravitulem (vähem IVH-d, PVLi, kaugtulemina vähem rasket neuroloogilist puuet 18–24 kuu vanuses). CAP uuringu tulemuste põhjal esines 18 kuu vanuses kofeiinravi rühmas (vs. platseebo) vähem tserebraalparalüüsi ja kognitiivse arengu hilinemist ning 11 aasta vanuses vähem motoorset kahjustust võrreldes platseeborühmaga (282). Töörühm otsustas ajakohastada kahe algse soovituse sõnastust ning muuta ühe soovituse tugevust, tuginedes uuemale tõendusmaterjalile.
Tahhükardia esinemisel kõrvaltoimena võib olla vajalik annuse muutmine või ravipaus. Ravimi kumuleerumise risk on suurem sügava enneaegsuse korral.
Kofeiinravi võib kasutada kõikidel enneaegsetel vastsündinutel, kes on mitteinvasiivsel hingamistoetusel või kellel on suurenenud risk invasiivse hingamistoetuse vajaduse tekkeks. Kofeiinravi säilitusannusena on kasutatud ka suuremaid annuseid ning pikem ravi on soositud, sest annab kaitsva efekti. Kofeiinravi lõpetamisel vajab vastsündinu jälgimist viis kuni kümme päeva. (291)
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K25 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 24 TõKo ja SoKo tabelit.
Hemodünaamika hindamise kriteeriumid
| 77 |
Enneaegse vastsündinu vereringet hinnake kompleksselt järgmiste koeperfusiooni näitajate alusel: jume, kapillaartäitumus, südamelöögisagedus, keskmine vererõhk, ajukoe regionaalne saturatsioon, diurees, happe-aluse tasakaal, laktaat. Ärge ravige enneaegse vastsündinu hüpotensiooni ainult vererõhu lävendist lähtudes. |
Uuringutes oli „ravitud hüpotensioon“ VLBW-lastel seotud haigestumise ja kuulmislangusega ning ebasoodsa kaugtulemiga (295, 297). Ühes uuringus leiti, et ravi võib olla seotud IVH tekkega (298).
Paljud normatiivsed vererõhu referentsväärtused rajanevad sellistel kriteeriumitel nagu sünnikaal, gestatsiooni- ja postnataalne vanus (293–295) ning varieeruvad märkimisväärselt, sest nende aluseks on puudulike andmetega retrospektiivsed uuringud, mis on tehtud väikestel kohortidel ja vastsündinutel, kes sündisid enne perinataalabi parandavate ravivõtete (nt GKS) kasutuselevõttu (294, 295).
Joint Working Group of the British Association of Perinatal Medicine on soovitanud, et keskmine arteriaalne vererõhk (mm Hg) peaks olema kõrgem sündinud lapse gestatsioonivanusest nädalates (299). Vaatamata vähesele tõenduspõhisusele on see kõige sagedasem ja tihti ainuke ravi alustamise kriteerium, mida on kasutatud mitmes juhuslikustatud uuringus (171, 292, 294, 295, 297).
Vererõhk ei pruugi korreleeruda perfusiooniga. Uuringus hinnati kombineeritud parameetrite efektiivsust hüpotensiooni ravi alustamisel VLGA-lastel, kelle vererõhk stabiliseerus spontaanselt esimese 24 tunni jooksul. Vastsündinud, kes olid hüpotensiivsed gestatsiooninädala kriteeriumite järgi, kuid kellel ei olnud kliiniliselt perfusioonihäiret, olid niisama hea kaugtulemiga nagu normotensiivsed patsiendid. Ravitud hüpotensioon oli seotud ebasoodsa kaugtulemiga (294, 300).
Neonataalmeditsiini praktikas kasutatakse hüpotensiooni määratlemiseks tavaliselt kaht vererõhu väärtust: kolmel esimesel elupäeval keskmine arteriaalne rõhk (MAP) alla 30 mm Hg või MAP väiksem vastsündinu gestatsioonivanusest nädalates. Neid väärtusi käsitletakse ka ravi alustamise näidustusena. Uuringud ei ole nende kriteeriumide tõenduspõhisust kinnitanud. Tõendite järgi on rohkem kui 90%-l gestatsioonivanusega 23+0–26+6 GN-i sündinud vastsündinutest MAP pärast kolmandat elupäeva üle 30 mm/Hg. Ravijuhendi soovitus on jälgida vererõhku regulaarselt, et säilitada normaalne kudede perfusioon. Hüpotensiooni ravi tuleb rakendada, kui esineb kudede perfusiooni häire (171). Õige ravi määramise alus on hüpotensiooni põhjuse väljaselgitamine. Ei ole valideeritud kliinilist skoorisüsteemi, millega oleks võimalik diagnoosida šokki või süsteemse perfusiooni puudulikkust, mis on enneaegsetel vastsündinutel seotud madala vererõhuga. Vastsündinu hemodünaamika hindamisel ja hüpotensiooni ravi alustamisel VLGA-lastel on soovitatav hinnata vereringet kompleksselt, kasutada kaudseid kliinilisi parameetreid (jume, kapillaartäitumus, südamelöögisagedus, keskmine vererõhk, diurees, happe-aluse tasakaal, laktaat) (297). Ükski nendest näitajatest ei ole isoleeritult spetsiifiline perfusiooni hindamiseks. Paljud neist parameetritest on subjektiivsed, kuid koos vererõhu jälgimisega annavad paremat infot perfusiooni kohta ja täiendavad vererõhu näitude usaldusväärsust (292, 294, 295, 297, 301, 302).
Kirjanduses avaldatud CRT väärtused on esitatud ajaliste vastsündinute kohta, enneaegsetele kohandatud väärtused puuduvad. Uuringute järgi esineb nõrk seos CRT ja süsteemse verevoolu vahel (295, 302). CRT mõõdetakse eelistatult rinnaku keskosas, otsmikul, suurel varbal (avaldada kerget survet viie sekundi jooksul, siis vabastada survest ja mõõta aeg, mis läheb värvuse taastumiseks). Pikenenud CRT-ks peetakse aega üle nelja sekundi (302).
Ühes varasemas uuringus, milles võrreldi seerumi laktaadi ja perfusiooni hindamise seost, ei leitud hüpotensiivsetel ja normotensiivsetel enneaegsetel vastsündinutel perifeerse oksügenisatsiooni hindamisel laktaadi taseme erinevust (303). Prospektiivses VLGA-laste vaatlusuuringus leiti, et laktaadi väärtusel rohkem kui 4 mmol/l ja pikenenud CRT-l üle nelja sekundi on positiivne ennustav väärtus 80% ja negatiivne ennustav väärtus 88% aeglase süsteemse voolu leidmiseks. Uuringus on rõhutatud kliiniliste ja biokeemiliste parameetrite kombineerimise vajadust (295, 302). Laktaadi tase on informatiivne kudede oksügenisatsiooni näitaja. Esimesel elupäeval korduva laktaadisisalduse määramine võib prognoosida kaugtulemit. Tulem on halvem, kui kopsude invasiivsel ventilatsioonil oleval gestatsioonivanusega 23–40 GN-i sündinud vastsündinul on laktaadi väärtus püsivalt suurenenud. Kui kaks laktaadi väärtust olid suuremad kui 5,6 mmol/l, ulatus suremus 57%-ni (292).
Südamelöögisagedus varieerub gestatsiooniaja ja lapse postnataalse vanusega ning korreleerub hapniku tarbimisega. Vahetult sünni järel on südame löögisagedus aeglasem ja kiireneb esimese viie eluminuti jooksul (304). Sealjuures on löögisageduse tõus aeglasem enneaegsetel vs. ajalistel, keisrilõike teel vs. vaginaalselt sündinud lastel ning juhul, kui emale on manustatud valuvaigisteid (304). Kapadia jt tehtud kaheksa uuringu individuaalsete patsiendiandmete metaanalüüsis (305) leiti, et enne 32. GN-i sündinud enneaegsetel, kellel esineb kestev bradükardia (SL < 100 bpm >= 2 min), on suurem risk haiglas surra. Samuti oli sünnitustoas bradükardilistel vastsündinutel viiendal eluminutil sagedamini SpO2 < 80%. Bradükardia pikem kestus oli seotud suurema IVH ja BPD esinemissageduse ning haiglasuremusega (305). Oliguuria on elundite vähenenud perfusiooni üks näitajatest. Invasiivne vererõhu mõõtmine on nn kuldne standard.
Ravijuhendi ajakohastamisel soovis töörühm täpsustada, kas seni soovitatud parameetrid hemodünaamika kompleksseks hindamiseks ja raviotsuste tegemiseks on kehtivad.
Üks juhuslikustatud uuring, kus planeeriti uurida, kas madala vererõhu korral esimesel 72 elutunnil parandab inotroopse ravi piiramine enne 28. GN-i sündinud enneaegsete vastsündinute elumust ilma olulise ajukahjustuseta 36. postmenstruaalseks nädalaks, kukkus läbi. Uuringusse õnnestus juhuslikustada ainult 7,7% planeeritud populatsioonist, mistõttu selle uuringu tulemusi ei saa tõendusmaterjalina kasutada (306). Samasse uuringusse juhuslikustamiseks skriinitud 89 enneaegsel vastsündinul leiti jälgimisuuringus seos IVH esinemise ja ajukoe hüpoksia kestuse vahel, mis peale gestatsioonivanusega korrigeerimist muutus ebaoluliseks (307).
Enneaegsete vastsündinute optimaalse vererõhuväärtuse leidmiseks on kasutatud ajukoe regionaalse saturatsiooni mõõtmisel põhinevat aju verevoolu autoregulatsiooni hindamist. 44 vastsündinuga (mediaangestatsioonivanuses 25 (23–27) nädalat) uuringus on leitud vererõhu väärtused, mille juures aju verevool sõltub kõige vähem vererõhust. Nii positiivse kui ka negatiivse tulemiga enneaegsete vastsündinute kohordile on hinnatud optimaalseks keskmiseks arteriaalseks vererõhuks 31,3 +/– 4,7 mm Hg. Enneaegsetel vastsündinutel, kellel tekkis IVH või kes surid, olid vererõhu kõikumised alla optimaalse vererõhu suuremad kui ilma IVH-ta ellujääjatel. (308)
103 enneaegse vastsündinu (keskmise gestatsioonivanusega 26 nädalat) vaatlusuuringus, kus 21 (20%) suri või sai tõsise neuroloogilise tüsistuse, oli halva tulemiga vastsündinutel oluliselt madalam ajukoe hapnikusaturatsioon 67 ± 9% vs. 72 ± 7%. Ajukoe saturatsioon < 50% oli läviväärtuseks halvale prognoosile. Vastsündinutel, kes surid või said raske neuroloogilise kahjustuse, esines rohkem olulist positiivset või negatiivset korrelatsiooni ajukoe saturatsiooni ja keskmise arteriaalse vererõhu vahel, aju autoregulatsiooni puudumise tunnusena. (309)
Süstemaatilistes ülevaadetes on kokku võetud tõendusmaterjal ülemise õõnesveeni verevoolu ja ajuarterite verevoolu alusel ajukahjustuse või halva pikaaegse neuroloogilise tulemi ennustamiseks, aga kummalgi juhul ei olnud olemasolevad uuringud selliselt tehtud, et oleks saanud teha metaanalüüsi. Kvalitatiivsetes ülevaadetes on esile tõstetud, et uuringutulemuste mittevastavuse tõttu ei saa soovitusi anda. (310)
43 vastsündinul (mediaangestatsioonivanusega (ulatus) 25 + 5 (23 + 3–31) nädalat) esimesel kahel elupäeval tehtud uuringus mõõdeti ehhokardiograafial südame minutimahtu ja lähipuna spektroskoopiaga ajukoe oksügenisatsiooni. Tulemused näitasid, et enneaegsetel vastsündinutel, kellel tekkis IVH, sõltus aju verevool südame minutimahust. Selle uuringu suur puudus oli palju puuduolevaid ehhokardiograafia mõõtmisandmeid. (311)
Tõendusmaterjali puudumise või väga madala kvaliteedi tõttu ei saa anda kindlaid soovitusi vererõhu ja verevoolu hindamisel kindlate parameetrite ja eesmärkväärtuste kasutamiseks. Ravi eesmärk on koeperfusiooni ja hapnikuga varustatuse tagamine, mistõttu soovitame jälgida mitmeid erinevaid vereringet iseloomustavaid parameetreid.
Vahetul sünnijärgsel stabiliseerimisel jälgige südame löögisagedust, kuna südamesageduse tõus on kõige kiirem adekvaatse ventilatsiooni ja oksügenisatsiooni saavutamise tunnus. Sealjuures annab südame löögisageduse hindamine EKG elektroodidega võrreldes pulssoksümeetrial mõõdetuga kiiremini usaldusväärse lugemi.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K17 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 17 TõKo ja SoKo tabelit.
Hüpotensiooni, hüpoperfusiooni ravimeetodid
| 78 |
Vereringehäirega enneaegsele vastsündinule kaaluge südame- ja vereringepuudulikkuse põhjuse täpsustamiseks südame ultraheliuuringu tegemist. |
|
| 79 |
Enneaegsel vastsündinul ärge kasutage rutiinselt ringleva veremahu asendust ega vasoaktiivset ravi. |
|
| 80 |
Enneaegsel vastsündinul kaaluge hüpotensiooni ravi sõltuvalt põhjusest, kui ilmnevad hüpoperfusiooni tunnused: oliguuria, atsidoos, halb kapillaarne täituvus (vt lisa 7). |
|
| 81 |
Enneaegse vastsündinu hüpotensiooni/hüpoperfusiooni, mille põhjus on verekaotus või hüpovoleemia, ravige esmalt ringleva veremahu täitmisega 10 ml/kg, vajaduse järgi võib sama annust korrata. Massiivse verekaotuse korral jätkake esimesel võimalusel erütrotsüütide suspensiooni ja teiste verekomponentide ülekannetega massiivse transfusiooni põhimõtete alusel. |
Enneaegsete laste hüpotensiooni ravi kohta ei leidu piisavalt tõenduspõhist materjali. Seetõttu jääb ebaselgeks, millal tuleks selles populatsioonis hüpotensiooni ravida ja missugune peaks olema ravistrateegia. Siiski on kõikides hüpotensiooni/hüpoperfusiooni käsitlevates ravijuhendites rõhutatud, et kontrollitud vererõhu raviks on vaja lähtuda hüpotensiooni etioloogiast (171, 297, 312–314).
Cochrane’i 2009. aasta metaanalüüsis järeldati, et kardiovaskulaarsete häireteta enneaegsetel vastsündinutel tuleks rutiinset veremahu täitmist vältida. Samuti ei ole tõendatud, et veremahu täitmine oleks hüpotensiooniga enneaegsetele vastsündinutele kasulik. Andmed veremahu täitmiseks kasutatavate vedelikutüüpide eelistamise kohta on samuti ebapiisavad (297, 315, 316). Enamik hüpotensiooniga VLBW-vastsündinutest ei ole hüpovoleemilised ja neil on normaalne ringleva vere maht (312, 313). Varajase hüpovoleemia esinemist saab vähendada nabaväädi hilise sulgemisega. Kui hüpovoleemia on tõendatud ehhokardiograafilise uuringuga või hüpotensiooni põhjus ei ole täpselt teada, võib kaaluda vedelikuboolusena naatriumi suhtes isotoonilise kristalloidlahuse (eelistatud kolloidlahuste ees) manustamist 10 (kuni 20) ml/kg (171, 315, 317).
Cochrane’i 2009. aasta metaanalüüsile tuginedes jääb ebaselgeks, kas ja millal tuleks hüpotensiivsetel enneaegsetel vastsündinutel kasutada veremahu täitmist või vasoaktiivset/kardiotoonilist ravi (316).
Dopamiin on enneaegsel vastsündinul enim uuritud ja kasutatud vasoaktiivne aine (318). Varased uuringud on näidanud, et dopamiin tõstab vererõhku efektiivsemalt kui dobutamiin, aga see ei korreleeru alati süsteemse verevoolu paranemisega (319). Uuemates analüüsides ja uuringutes on tähelepanu pööratud dopamiini mitteselektiivse vasokonstriktoorse toime võimalikele negatiivsetele mõjudele, eriti pulmonaalhüpertensiooni korral (320). Loomeksperimentides on leitud, et normaalse kopsuarteri rõhu korral on dopamiinil toime eeskätt süsteemsele vereringele, põhjustades vasokonstriktsiooni – süsteemse vererõhu ja kopsuringe rõhu suhe pigem suureneb. Kõrgenenud kopsuringerõhu korral (nt hüpoksiast vm tingituna) on dopamiini mõju kopsuarteri rõhule võrreldav mõjuga süsteemses vereringes (321). Sarnast efekti on kirjeldatud ka vastsündinutel, sh enneaegsetel tehtud vähestes vaatlusuuringutes (süsteemse vererõhu ja kopsuringe rõhu suhe pigem väheneb, seega efekt kopsuarteri rõhule enam väljendunud; PDA šunt, mis enne ravi ühesuunaline, muutub kahesuunaliseks) (322).
Dobutamiini soovitatakse kasutada enneaegsetel vastsündinutel müokardi düsfunktsioonist ja/või perifeerse vaskulaarse resistentsuse suurenemisest tingitud hüpotensiooni või hüpoperfusiooni ning aeglase süsteemse verevoolu puhul. Kui vererõhk pärast dobutamiinravi alustamist langeb, võiks lisaks kasutada väikeses annuses dopamiini. Kolmanda valikuna võib kasutada hoolikalt tiitritud annuses adrenaliini (171, 297, 323, 324). Dobutamiinil on otsene positiivne inotroopne toime ja retseptorite tundlikkusest sõltuv mõju perifeersele vasodilatatsioonile. Olukorras, kus VLBW-vastsündinu südame minutimaht on mõjutatud äkiliselt suurenenud perifeersest vaskulaarsest resistentsusest, mis kaasneb väikese resistentsusega platsenta eemaldamisega, arvavad eksperdid, et dobutamiini ettevaatliku astmelise annustamisega võib vasodilatatsiooni ja süsteemse verevoolu parandamisega suurendada südame minutimahtu. Samas ei ole tõendeid, et ühepäevasel VLBW-lapsel põhjustaks dobutamiin süsteemset vasodilatatsiooni (319, 325).
Hüdrokortisooni võib hüpotensiooni raviks kasutada, kuid andmed kortikosteroidide pikaajalise ohutuse kohta on puudulikud. Seetõttu tuleks hüdrokortisooni kasutada vaid refraktaarse hüpotensiooni korral (326).
Praegu ei ole tõendeid, mis toetaksid milrinooni kasutamist hüpotensiooni raviks VLBW-vastsündinutel. Ühes topeltpimedas juhuslikustatud kontrolluuringus, kus võrreldi milrinooni ja platseebo efektiivsust aeglase süsteemse verevooluga VLBW-vastsündinutel, näidati, et milrinoon ei hoidnud ära aeglast süsteemset verevoolu (327). Enneaegsetel vastsündinutel on milrinooni kasutatud hilisemas vanuses avatud arterioosjuha sulgemise järgse südame väikse minutimahu sündroomi ennetamiseks (328, 329).
Terlipressiini ja levosimendaani ei soovitata enneaegsetel vastsündinutel hüpotensiooni raviks kasutada, kuna piisava kvaliteediga uuringud selle populatsiooni kohta puuduvad (323, 324). Viimastel aastatel on vastsündinutel soovitatud vasopressiini kasutada, kui on vaja hoida adekvaatset diastoolset vererõhku, näiteks tagamaks adekvaatset koronaarperfusiooni.
VLBW-vastsündinute hüpotensiooni ravi algoritm esimestel elupäevadel (297) ja enneaegse vastsündinu hüpotensiooni raviks kasutatavad ravimid (171) on toodud lisas 7.
Ravijuhendi ajakohastamisel soovis töörühm täpsustada, kas enneaegse vastsündinu esmasel stabiliseerimisel peaks kasutama parema ravitulemust saavutamiseks kindlat hüpotensiooni/hüpoperfusiooni ravimeetodit.
Prospektiivsetes juhuslikustatud uuringutes ei ole õnnestunud näidata inotroopsete või vasopressoorsete ravimite pikaaegseid toimeid, kuna nendesse uuringutesse ei ole õnnestunud piisavat arvu vastsündinuid kaasata. Kuna selliseid uuringuid ei ole võimalik teha, peame tõenduspõhist teadmist nende ravimite toimete kohta saama teistsuguse disainiga uuringutest, nagu näiteks farmakokineetika- faramkodünaamika mudelid ja füsioloogial baseeruvad mudelid.
Kui enneaegsel vastsündinul on hüpoperfusiooni tunnused, tuleks ravi valikul lähtuda vereringehäire eeldatavast või leitud põhjusest ning teha inotroopsete ja vasopressoorste ravimite valik nende farmakodünaamiliste omaduste alusel. Täpsemalt vt lisa 7.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K18 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 18 TõKo ja SoKo tabelit.
Parenteraalne toitmine (vt lisa 8)
| 82 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g, keda ei ole võimalik toita piisavas mahus enteraalselt, eelistage parenteraalse toitmisega alustamist esimesel elupäeval, soovitatavalt esimestel elutundidel. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 83 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g eelistage glükoosi infusiooni alustada 4–8 mg/kg minutis (5,8–11,5 g/kg päevas) ja edaspidi juhinduge vere glükoosisisalduse jälgimisest. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 84 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g ärge kasutage hüperglükeemia ennetamiseks insuliini. Tugev negatiivne soovitus, madal tõendatuse aste |
|
| 85 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g eelistage alustada aminohapete lahuste manustamist võimalikult kiiresti sünni järel, hiljemalt 24 tunni vanuselt. Ohutu on alustada aminohapete pakkumist 2–2,5 g/kg päevas, suurendades järgnevatel päevadel valgukogust kuni annuseni 3,5 g/kg päevas. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 86 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g eelistage alustada lipiidide manustamist esimesel elupäeval. Soovitatav algannus on 1,0 g/kg päevas, edaspidi suurendada taluvuse korral lipiidide kogust annuseni 3,0 g/kg päevas. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 87 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g eelistage niisutatud kuvöösi tingimustes alustada vedeliku pakkumisega 70–80 ml/kg päevas, suurendades vedeliku pakkumist järk-järgult füsioloogiliselt. Enne 28.+0 GN-i sündinud enneaegsed vastsündinud võivad vajada rohkem vedelikku. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 88 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g korrigeerige vedeliku pakkumist individuaalselt, arvestades seerumi naatriumi kontsentratsiooni ja kaalulangust. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 89 |
Enneaegsel vastsündinul sünnikaaluga alla 1500 g pigem piirake esimestel elupäevadel naatriumi pakkumist, alustades sellega pärast diureesi vallandumist ning jälgides vedelikubilanssi ja elektrolüütide taset. Nõrk positiivne soovitus, madal tõendatuse aste |
Ravijuhendites, metaanalüüsides (v.a Cochrane’i selleteemaline 2013. aasta metaanalüüs) ja süstemaatilistes ülevaadetes on soovitatud enneaegsetel vastsündinutel (sh enneaegsed VLBW-vastsündinud), kellel on sünni järel enteraalse toitmise mahud piiratud, alustada parenteraalset toitmist esimesel elupäeval (171, 50, 330–334). Varajase parenteraalse toitmise eesmärk on tagada vastsündinule piisavalt energiat ja aminohappeid, suurendades valgusünteesi ja lämmastiku säilitamist, sest see vähendab sünnijärgset kaalulangust ning pikemaajalist sünnijärgset kasvupeetust. Varajase parenteraalse toitmisega ei suurene suremus ega haigestumine NEK-sse, sepsisesse, CLD-sse, IVH-sse või kolestaasi (331) ega kaasne halvem neuroloogiline kaugtulem lapse kahe aasta vanuses (335). Parenteraalse toitmise alustamise edasilükkamine kuni tsentraalse veenitee rajamiseni ei ole vajalik. Puuduvad tõendid, et osmolaarsuse/glükoosi suure kontsentratsiooniga kaasnevad riskid kaaluksid üle parenteraalsest toitmisest saadava kasu.
Glükoosi infusiooni tuleks alustada pakkumisega 4–8 mg/kg minutis (5,8–11,5 g/ kg päevas). Maksimaalne glükoosi oksüdatsioon enneaegsetel vastsündinutel sünni järel on 8,3 mg/kg minutis (12 g/kg päevas) (330). Liigne glükoosi pakkumine võib põhjustada hüperglükeemiat ja soodustada põletikuliste kahjustuste ning maksa, südame ja teiste elundite rasvinfiltratsiooni teket.
Metaanalüüsi tulemuste põhjal järeldati, et insuliini rutiinne kasutamine hüperglükeemia ennetamiseks ja kasvamise soodustamiseks võib olla kahjulik (333, 334, 336). Insuliini võib hüperglükeemiaga VLBW-lastel parenteraalse toitmise ajal kasutada, kuid ohutus ja toime kliinilisele tulemile ei ole teada (330).
Aminohapete varajase ja hilise pakkumise võrdluse metaanalüüsis (337) järeldati, et ei ole piisavalt andmeid parenteraalsel toitmisel varajase aminohapete pakkumisega kaasneva soodsa toime kohta enneaegsete vastsündinute varajasele ja hilisele kasvule, neuroloogilisele arengule ning suremusele. Minimaalne aminohapete pakkumine peaks olema vähemalt 1,5 g/kg päevas, et ennetada negatiivset lämmastikubilanssi. Suurem pakkumine on vajalik, et saavutada füsioloogiline valgu talletamine (330). Esmane ohutu aminohapete pakkumine on vähemalt 2–2,5 g/kg päevas, edaspidi tuleb annust astmeliselt suurendada kuni 3,5–4 g/kg päevas (vt lisa 8). Selleks et tagada enneaegse lapse positiivne kaaluiive, ei tohiks parenteraalset aminohapete pakkumist vähendada enne, kui enteraalse toitmise maht ületab 75 ml/kg päevas.
Parenteraalse toitmise puhul on soovitatav kaloraaž esimesel elupäeval 50–60 kcal/kg päevas, edaspidi täieliku parenteraalse toitmise puhul 90–115 kcal/kg päevas (vt lisa 8). Puuduvad tõendid suurema energiapakkumise soodsa mõju kohta neuroloogilisele tulemile, kasvutempole ja kehakoostisele. Enneaegsetel vastsündinutel võib suurema energiapakkumise tulemusena tekkida rasva ladestumine (334).
Vastsündinutel, keda ei ole võimalik enteraalselt piisavalt toita, tuleb alustada lipiidemulsioonide parenteraalset manustamist hiljemalt kolmandal elupäeval (330). Metaanalüüsis (332) järeldati, et VLBW-lapsele lipiidide manustamise alustamine kahel esimesel elupäeval on turvaline ja hästi talutav. Lisaks leiti, et mittetäielikult sojaoaõlil baseeruvate lipiidemulsioonide kasutamine võib olla seotud sepsise esinemise väiksema sagedusega selles populatsioonis (332). Kliinilises praktikas on soovitatav lipiidide manustamist alustada esimese 24 elutunni jooksul, algannusena 1,0 g/kg päevas, suurendades seda astmeliselt 0,5– 1,0 g/kg päevas, lipiidide taluvuse korral kuni annuseni 3,0 g/kg päevas (50, 330, 334). Lipiidemulsioone tuleks manustada 24-tunnise infusioonina. Vaja on jälgida triglütseriidide taset (330). Enneaegsetel vastsündinutel on soovitatav kasutada 20%-lisi lipiidemulsioone. Keskmise ja pika ahelaga triglütseriide sisaldavatel lipiidlahustel on eelis ainult pika ahelaga triglütseriide sisaldavate lipiidlahuste ees (330, 334).
Vedeliku ja elektrolüütide kontrollitud tasakaal on vajalik selleks, et vältida dehüdratatsiooni, ülehüdratatsiooni, elektrolüütide häireid ja metaboolse atsidoosi teket, mis omakorda võivad suurendada suremust ja haigestumust. Kolmel esimesel elupäeval peab vedeliku ja naatriumkloriidi pakkumine olema piiratud (vt lisa 8) (50, 338).
Soovitused toitainete ja vedelikuvajaduse kohta sügavalt enneaegsel vastsündinul on toodud lisas 8.
Ravijuhendi ajakohastamisel antud kliinilist küsimust ei avatud. Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K23.
Enteraalne toitmine (vt lisa 8)
| 90 |
Enneaegsel vastsündinul alustage enteraalset toitmist võimaluse korral oma ema rinnapiimaga, selle puudumisel doonoripiimaga, ema rinnapiima ja doonoripiima puudumisel enneaegsete piimaseguga. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 91 |
Enneaegsel vastsündinul, kes on sündinud enne 28.+0 GN-i, alustage minimaalset enteraalset toitmist esimesel elupäeval võimalikult vara, soovitatavalt esimestel elutundidel. Sobiv kogus ühel toidukorral on 1 ml/kg iga kahe-kolme tunni järel. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 92 |
Enneaegse vastsündinu enteraalse toitmise taluvuse korral suurendage toidu kogust 10–30 ml/kg ööpäevas. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 93 |
Enneaegse vastsündinu boolusena toitmise korral suurendage toidukogust 1 ml/kg 8–12 tunni järel. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 94 |
Enneaegse vastsündinu pideva toitmise korral suurendage toidukogust 0,5–1,0 ml/kg 8–12 tunni järel. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 95 |
Enneaegse vastsündinu rinnapiima rikastamist kaaluge alates toidukogusest 100 ml/kg ööpäevas. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 96 |
Enneaegsel vastsündinul, kes on sündinud enne 32.+0 GN- i, tagage täisenteraalsel toitmisel energiavajadus 110–130 kcal/kg ööpäevas ja valguvajadus 3,0–4,5 g/kg ööpäevas. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
Oma ema rinnapiim ei vaja pastöriseerimist ja on tavaliselt doonoripiimast suurema valgusisaldusega. Doonoripiima sagedasim valgusisaldus on 1 g/dl, sest doonoriteks on tavaliselt ajaliselt sünnitanud naised. Enneaegsete laste emade rinnapiima valgusisaldus on neljandal kuni kuuendal nädalal pärast sünnitust 1,2–1,5 g/dl, mille tõttu on vaja doonoripiima rikastada. Pastöriseerimine kaitseb bakteriaalsete ja viirushaiguste eest, kuid rinnapiimas sisalduvad unikaalsed põletikuvastased komponendid inaktiveeruvad pastöriseerimisel. Sekretoorse lgA tase väheneb 28–60%, laktoferriini ja lüsosüümi aktiivsus vähenevad vastavalt 80% ja 60%. Enamik uuringuid näitab, et pastöriseerimine ei mõjuta rinnapiima valgu-, rasva- ega süsivesikusisldust, kuid asendamatute pika süsinikuahelaga polüküllastamata rasvhapete sisaldus väheneb. Enamiku vitamiinide ja mineraalide sisaldus püsib endine, kuid piima antioksüdantne toime väheneb oluliselt. (339– 342)
Varajane toitmine rinnapiimaga vähendab NEK riski ja ebaküpse seedetrakti permeaablust, stimuleerib rakkude proliferatsiooni, soodustab mao tühjenemist ja kiirendab jõudmist täisenteraalse toitmiseni. Hilinenud või vähene enteraalne toitmine võib nõrgendada seedetrakti funktsionaalset adaptatsiooni ja häirida mikroobide kolonisatsiooni. Seedetrakti düsmotoorika võib põhjustada toidutalumatust ja enteraalse toitmise hilinemist ning seetõttu pikendab parenteraalse toitmise vajadust, mis omakorda võib luua soodsamad tingimused hilise sepsise tekkeks. (340, 343, 344)
Troofilise toitmise ehk minimaalse enteraalse toitmise kogus on 10–15 ml/kg ööpäevas. Soovitatav alustamise aeg on esimese 24 tunni jooksul. Ettevaatlikumalt tuleb suhtuda ELBW- ja IUGR-vastsündinutesse. Kui ei esine olulisi kliinilisi sümptomeid ja maojääk on alla 4 ml/kg või alla 50% viimasest toidukorrast kolme tunni jooksul, siis ei ole vajadust toidukogust vähendada ega toitmist katkestada (345).
Toitmine boolustena on füsioloogilisem kui pidev toitmisviis, soodustades seedetrakti hormoonide tsüklilist vabanemist, mida on näidatud ajalistel vastsündinutel. See võib olla tähtis seedetrakti arengule. Samas võib boolustoitmine olla ebaküpsele seedetraktile koormav, soodustada toidutalumatuse ja toitmisega seostatud apnoede teket. Süstemaatilise ülevaate põhjal ei leitud erinevust täisenteraalse toitmiseni jõudmises, lapse kasvamises ja NEK esinemise sageduses, kui võrreldi pideval ja boolustena toitmisel olevaid lapsi (344, 346, 347). Pidev enteraalne toitmine võib parandada energia tasakaalu, suurendades toitainete absorptsiooni ja vähendades selle kulutamist, soodustada kasvu ja toidutaluvust. Samas on võimalik, et pidev toitmine mõjutab negatiivselt seedetrakti hormoonide tsüklilist vabanemist (gastriin, gastriini inhibiitor peptiid ja enteroglükagoon) ja metaboolset homeostaasi ning häirib alumise söögitoru sfinkteri funktsiooni, soodustades gastroösofageaalse refluksi arengut (344, 346, 347).
Täisenteraalse toitmise korral on toidukogus 150 ml/kg ööpäevas 72 tundi järjest (345). Rinnapiima rikastamine on individuaalne, näidustatud alates toidukogusest 100 ml/kg ööpäevas (340, 346, 348).
Enneaegsetel vastsündinutel on piisava kaaluiibe saavutamiseks valgu- ja energiavajadus palju suurem kui ajalisena sündinud lastel. Life Sciences Research Office on soovitanud, et valguvajadus alla 1200 g sünnikaaluga enneaegsetel on 3,4–4,3 g/kg ööpäevas. European Society for Paediatric Gastroenterology, Hepatology and Nutrition (349) on soovitanud enteraalseks piimakoguseks 135– 200 ml/kg ööpäevas (tavaliselt 150–180 ml/kg ööpäevas) ning valguvajaduseks 4,0–4,5 g/kg ööpäevas alla 1000 g sünnikaaluga lastel ja 3,5–4,0 g/kg ööpäevas 1000–1800 g sünnikaaluga lastel (349, 350). Kui laps saab energiat või valku ööpäevasest vajadusest vähem, on vaja rinnapiima rikastada.
Ravijuhendi ajakohastamisel antud kliinilist küsimust ei avatud. Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K24.
Probiootikumid
| 97 |
Enneaegsel vastsündinul, kes on sündinud enne 34.+0 GN-i ja/või sünnikaaluga alla 1500 g, kasutage probiootikumi kohe koos toitmise alustamisega. |
|
| 98 |
Enneaegsel vastsündinul sünnikaaluga alla 1000 g kaaluge probiootikumi kasutamist. |
|
| 99 |
Kriitiliselt haigetel enneaegsetel vastsündinutel (baktersepsis, NEK) ärge kasutage probiootikumi. |
|
| 100 |
Enneaegsel vastsündinul lõpetage probiootikumi kasutamine pärast kuut nädalat või kojuminekul. |
|
| 101 |
Enneaegsel vastsündinul kaaluge kombineeritud probiootikumide preparaadi kasutamist, eelistatult B infantis Bb-02, B lactis Bb-12 ja Str thermophilus TH-4 annuses 3,0–3,5 × 108 pesa moodustavat ühikut (iga tüve kohta). |
On leitud, et probiootikumide kasutamisel võib olla positiivne efekt lapse ravitulemusele. Cochrane’i süstemaatilises ülevaates järeldati, et probiootikumid võivad vähendada NEK esinemist väga enneaegsetel või väga väikse sünnikaaluga imikutel, kuid ei leitud olulist mõju NEK esinemisele erakordselt enneaegsetel või erakordselt väikse sünnikaaluga imikutel. (351)
Samuti leiti, et probiootikumid vähendavad tõenäoliselt suremust väga enneaegsetel või väga väikse sünnikaaluga imikutel, kuid ei leitud olulist mõju suremusele äärmiselt enneaegsetel või äärmiselt väikse sünnikaaluga imikutel (351). 2017. aasta metaanalüüsis on alarühmade võrdlusel kirjeldatud olulisemat suremuse vähenemist probiootikumide kasutamisel just enne 29. GN-i sündinud enneaegsetel, kui võrrelda pärast 29. GN-i sündinud enneaegsetega (352).
Mitmed metaanalüüsid näitavad väiksemat hilise algusega sepsise kujunemist probiootikumide kasutamisel väga enneaegsetel või väga väikse sünnikaaluga imikutel (351–354). Lisaks on leitud, et hilise algusega sepsist esineb vähem imikutel, keda lisaks probiootikumi manustamisele toideti rinnapiimaga (353).
2017. aasta metaanalüüs näitas statistiliselt olulist haiglaravi kestuse lühenemist probiootikumide kasutamisel, kusjuures haiglaravi kestus lühenes probiootikumide kasutamisel rohkem enne 29. GN-i sündinud enneaegsetel, kui võrrelda pärast 29. GN-i sündinud enneaegsetega (352).
Metaanalüüsides ei leitud märgatavat mõju intraventrikulaarsele hemorraagiale, neuroloogilise arengu kaugtulemile, nägemis- ja kuulmislangusele ega kasvukiirusele olenemata gestatsiooonivanusest ja sünnikaalust (351, 352).
Probiootikumi valik ja manustamisviis
Euroopa Lastegastroenteroloogia, Hepatoloogia ja Toitmise Ühingu (ESPGHAN) 2020. aasta soovitus on kasutada probiootikumide preparaate, mille täpne koostis on teada ning mille kasutamine on turvaline. Soovitus hõlmab Lactobacillus rhamnosus GG ATCC53103 kasutamist või alternatiivina kombinatsiooni Bifidobacterium infantis Bb-02, Bifidobacterium lactis Bb-12 ja Streptococcus thermophilus TH-4, kus iga tüve päevane annus on 3,0–3,5 × 108 pesa moodustavat ühikut (PMÜ). Samas seisukohadokumendis on välja toodud ka soovitus mitte kasutada B breve BBG-001, et vähendada suremust, 2. või
3. staadiumi NEK-d ning sepsist. Samuti ei soovitata turvalisuse kaalutlustel kasutada S. boulardii’d, sest selle kasutamine tsentraalveenikateetriga, kriitiliselt haigetel ning langenud immuunsusega patsientidel on vastunäidustatud Euroopa Meditsiiniagentuuri poolt ja lisaks puudub S. boulardii kasutamise efektiivsusel tõenduspõhisus. (356)
2017. aasta metaanalüüsis soovitatakse probiootikumi manustamist alustada koos esimese enteraalse toitmisega (354). Teise 2017. aasta metaanalüüsi tulemuste kohaselt on probiootikumid kõige efektiivsemad manustatult koos rinnapiimaga (352).
Kindlaid soovitusi probiootikumide kasutamise kestuse kohta ei ole antud, kuid suuremas osas ESPGHAN-i 2020. aasta seisukohadokumendi aluseks olevates uuringutes kestis probiootikumi manustamine neli kuni kuus nädalat või kuni haiglaravi lõpuni. (356)
Töörühma arvamusel on tähtis, et kasutatakse kvaliteetseid probiootikume, seega sõnastati vastav soovitus probiootikumide preparaatide kombinatsioonide kohta. Eri allikates on toodud soovitatav või optimaalne probiootikumide kasutamise kestus erinevalt, aga üldjuhul on see alla kuue nädala.
Vaata lisaks ajakohastatud ravijuhendi kliinilise küsimuse nr 22 TõKo ja SoKo tabelit.
A-vitamiin
| 102 |
Enneaegsele vastsündinule kaaluge A-vitamiini manustamist alates neljandast elupäevast suu kaudu või parenteraalse toitmise osana. |
ESPGHAN-i 2022. aasta seisukohtades enneaegsete vastsündinute enteraalse toitmise kohta soovitatakse kättesaadavatele andmetele tuginedes A-vitamiini ööpäevaseks koguseks 1,333–3,300 RÜ/kg kehakaalu kohta (400–1000 µg
retinoolestrit kg/p) (357).
Suures annuses intramuskulaarse A-vitamiini kasulikku rolli BPD ennetamisel enneaegsetel vastsündinutel on näidatud Cochrane’i süstemaatilises ülevaates (358). Ebamugavustunde tõttu pole selline manustamisviis tavapärane praktika. Uuringud suuremate suukaudsete doosidega (5000 RÜ päevas) on näidanud vastuolulist/ebaühtlast mõju (359).
Üks juhuslikustatud kontrolluuring, milles hinnati suures annuses rasvlahustuva suukaudse A-vitamiini manustamist (5000 RÜ päevas vs. platseebo 28 päeva jooksul) 154 enneaegsel imikul, ei näidanud kroonilise kopsuhaiguse olulist vähenemist (360). Teises uuringus, mis hõlmas 196 enneaegset imikut, hinnati seevastu suuremas annuses enteraalset A-vitamiini manustamist (10 000 RÜ vahelduvatel päevadel 28 päeva jooksul) ja see näitas positiivset efekti peamisele tulemusnäitajale, milleks oli suremus ja hapnikuvajadus 28 päeva jooksul ilma suuremate kõrvalmõjudeta (361). Järgmises juhuslikustatud kontrolluuringus hinnati veeslahustuva A-vitamiini 5000 RÜ päevas manustamise mõju 188 eriti enneaegsel imikul (< 28 nädalat GN). Selles uuringus parandas A-vitamiini manustamine plasma retinooli taset, kuid ei mõjutanud BPD esinemissagedust ega muid kliinilisi tulemusnäitajaid võrreldes platseeboga (362).
Võrreldes kontrollrühmaga selgus, et VLBW-imikutele A-vitamiini manustamisel on väike kasu, vähendades suremuse riski või hapnikuvajadust ühe kuu vanuselt ning BPD (hapnikuvajadus) riski PMV-s 36 nädalat (358). Allikad viitavad A-vitamiini kasulikule toimele BPD riski vähendamisel PMV-s 36 nädalat (mõõduka tõendatusega). Alarühmade analüüs näitas, et kasulik toime piirdus imikutega, kelle A-vitamiini baastarbimine oli vähem kui 1500 RÜ/kg päevas. Nii enteraalne kui ka parenteraalne manustamisviis olid tõhusad. (361)
A-vitamiini suukaudne manustamine enneaegsetele vastsündinutele ei mõjutanud invasiivse hingamistoetuse kestust, hapnikuvajadust, mõõduka kuni raske BPD esinemist ega suremust PMV-s 36 nädalat. Suukaudse A-vitamiini manustamine võib veidi vähendada mitteinvasiivse hingamistoetuse kestust. (363)
Uuringutes on kasutatud erinevaid A-vitamiini manustamise skeeme ja annuseid, 1500–10 000 RÜ päevas suukaudu alates 24 tunni vanusest kuni 28 päeva vanuseni (359, 364, 365).
Praegu ei manustata Eestis enneaegsetele vastsündinutele regulaarselt A-vitamiini. Tõendusmaterjali põhjal võib A-vitamiini manustamisest olla kasu, kuid tõendusmaterjal on madala tõendatuse astmega. Uuringutes on alustatud A-vitamiini manustamist alates neljandast elupäevast. Ei ole leitud, et A-vitamiini manustamisel oleks olulisi kõrvaltoimeid. Soovituslikud annused on leitavad lisast 8.
Vaata lisaks ajakohastatud ravijuhendi kliinilise küsimuse nr 23 TõKo ja SoKo tabelit.
Avatud arterioosjuha (vt lisa 9 ja 10)
| 103 |
Enneaegsel vastsündinul ärge kasutage avatud arterioosjuha ennetamiseks mittesteroidset põletikuvastast ravi (ibuprofeen, indometatsiin) ega paratsetamooli. |
|
| 104 |
Enneaegsel vastsündinul ärge forsseerige avatud arterioosjuha ennetamiseks diureesi (furosemiid, teofülliin). Tugev negatiivne soovitus, madal tõendatuse aste |
|
| 105 |
Enneaegsel vastsündinul vältige avatud arterioosjuha ennetamiseks liiga liberaalset vedeliku manustamist. |
|
| 106 |
Enneaegsel vastsündinul, kes on sündinud enne 28.+0 GN- i, kasutage sümptomaatilise ja/või hemodünaamiliselt olulise avatud arterioosjuha sulgemiseks ravi kõrges doosis ibuprofeeni (veeni või suu kaudu) või paratsetamooliga (vt annused lisas 9). Paratsetamooli eelistada patsientidel, kellel on vastunäidustus ibuprofeeni kasutamiseks (trombotsütopeenia, neerupuudulikkus). |
|
| 107 |
Enneaegsele vastsündinule tehke ehhokardiograafia, kui objektiivsete tunnuste alusel jääb hemodünaamiliselt olulise avatud arterioosjuha kahtlus. |
Juhuslikustatud kontrolluuringute andmetel on spontaanne PDA sulgumine sage. TIPP uuringus (367) (Trial of Indomethacin Prophylaxis in Preterms, 2001), mis hõlmas vastsündinuid sünnikaaluga 500–999 g, ei kujunenud 50%- l platseeborühma lastest kliiniliselt PDA sümptomeid. Uuringus, kus võrreldi raseduskestuse 26+0–31+6 GN-i korral sündinuil varajase ja hilise indometatsiinravi mõju, leiti, et lastel, kellel esines ehhoKG PDA kolmandal elupäeval, sulgus see hilisema sekkumise rühmas spontaanselt üheksandaks elupäevaks 78%-l juhtudest 350. Retrospektiivses uuringus hinnati enne 29. GN-i sündinud lastel PDA spontaanset sulgumist. Enne 26. GN-i sündinutest 90%-l oli PDA spontaanselt sulgunud enne 40 nädalat PMV. (368)
PDA ravi võimalused:
- ennetav ravi (tavaliselt esimese 24 elutunni jooksul);
- varajane eesmärgistatud ravi ehhoKG leiust lähtudes (hemodünaamiliselt oluline, kuid asümptomaatiline PDA);
- sümptomaatiline ravi (tavaliselt pärast 72. elutundi), mille aluseks on hemodünaamiliselt oluline PDA ning kliiniliste sümptomite esinemine.
Samuti ei ole näidustatud diureetikumide (furosemiid, teofülliin) manustamine. Furosemiidi manustamisel tuleks kaaluda kahju ja kasu suhet ning arvestada hüpovoleemia riski (50, 371). Vedeliku piiramine vähendab PDA ja NEK esinemise sagedust, kuid suurendab oluliselt sünnijärgset kaalulangust. Vedeliku pakkumine peaks jääma füsioloogilise vajaduse piiridesse, et vältida dehüdratatsiooni ja oliguuriat (338). 24 tundi pärast vedeliku restriktsiooni aeglustus oluliselt verevool alumises õõnesveenis ja ülemises mesenteriaalarteris ning diurees vähenes 60%, kuid puudus mõju respiratoorsetele näitajatele ja PDA sulgumisele (372).
Mitteinvasiivse ventilatsiooni rolli kohta PDA ennetamisel on tõendusmaterjali vähe. INSURE meetodi puhul on näidatud KKV ja hapnikravi vajaduse ning PDA ja IVH esinemise vähenemist võrreldes konventsionaalse invasiivse ventilatsiooni rühmaga (373). Metaanalüüsis, milles võrreldi varast surfaktandi manustamist ning lühiajalist ventilatsiooni selektiivse surfaktandi manustamise ja konventsionaalse ventilatsiooniga, leiti, et lastel, kellele manustati surfaktanti väiksema FiO2 (< 0,4) juures, esines vähem PDA-d (371). Jälgimisuuringutel põhineval metaanalüüsil esines kofeiinravi varajasel alustamisel (enne 3. elupäeva) PDA-d vähem võrreldes nende lastega, kellel kofeiinravi alustati kolmandal elupäeval või hiljem. Samuti oli PDA kirurgilise ravi vajadus väiksem nende enneaegsete puhul, kellel alustati kofeiinravi varakult (enne 3. elupäeva) (285).
Enne 28.+0 GN-i sündinud enneaegsetel võib kaaluda varast eesmärgistatud ravi, lähtudes ehhoKG leiust (369, 370). PDA ravi võib olla medikamentoosne või kirurgiline, kuid ravi vajadus on küsitav, kuna spontaanne hiline sulgumine on suhteliselt sage (50). Hemodünaamiliselt olulise PDA sulgemiseks on indometatsiin ja ibuprofeen võrdselt efektiivsed, kuid ibuprofeeni kasutusel on väiksem risk NEK ja transitoorse neerupuudulikkuse tekkeks (171, 50). Tõenduspõhisus PDA parima diagnostika ja ravi aja kohta on ebaselge. Diagnoos põhineb ehhoKG leiul, kuid puuduvad ühtsed kriteeriumid, millal PDA muutub hemodünaamiliselt oluliseks ning näidustatud on ravi. Pimeuuringutes, kus võrreldi PDA kliiniliste sümptomite (vt lisa 9 ja 10) ja ehhoKG markerite esinemist, on näidatud, et hemodünaamiliselt oluline PDA ei anna tavapäraselt esimese kahe-kolme elupäeva jooksul kliinilist sümptomaatikat. Alates neljandast elupäevast kujunevad kliinilised sümptomid, eriti kahina esinemine, kuid need ei pruugi olla diagnostiliselt piisavad seitsmenda elupäevani. Seega põhineb hemodünaamiliselt olulise PDA varajane diagnoosimine eeskätt ehhoKG-l (374).
Puudub ühtne seisukoht, millal peaks tegema esimese ehhoKG – sel teemal tehtud uuringuid ei leidunud, samuti ei olnud seda käsitletud ravijuhendites. Austraalia 2014. aasta ravijuhendis on soovitatud enne 28.+0 GN-i sündinud lastel teha uuring esimese kolme kuni kuue elutunni, kuid hiljemalt 12 tunni jooksul, ja pärast 28.+0 GN-i sündinuil vastavalt kliinilisele leiule (374). Rootsi 2014. aasta ravijuhendis on konsensuslik soovitus teha ehhoKG ühe kuni kolme päeva vanuses (50). Viimaste aastate metaanalüüsid ja juhuslikustatud kontrolluuringud on näidanud, et varajane PDA ravi võrreldes hilisega ei paranda enneaegsete laste ravi kaugtulemit. On ka seisukohti, et PDA üleravimise vältimiseks tuleks ehhoKG teha PDA kliiniliste sümptomite ilmnedes (374–377).
PDA (varast) ravi tuleks kaaluda ühe või mitme ehhoKG kriteeriumi ja kliinilise sümptomi esinemise korral. Esmavalik on medikamentoosne ravi ibuprofeeniga. Kirurgilist ravi tuleks kasutada juhul, kui medikamentoosne ravi ebaõnnestub või on vastunäidustatud (50, 171). Enne ravi tuleb alati välistada ductus’est sõltuvad kaasasündinud südamerikked.
Ravijuhendi ajakohastamisel avati algse ravijuhendi kliiniline küsimus, et analüüsida uuemat tõendusmaterjali. Lisaks koostati kaks uut kliinilist küsimust. Töörühm soovis selgitada, kas enneaegsel vastsündinul tuleb hemodünaamiliselt olulise arterioosjuha õigeaegseks diagnoosimiseks ja ravitulemuse parandamiseks teha südame ultraheliuuring enne 72. elutundi või hiljem. Samuti sooviti teada, kas enneaegsel vastsündinul peaks kasutama parema ravitulemuse saavutamiseks hemodünaamiliselt oluliselt avatud arterioosjuha korral konservatiivset ravi või kirurgilist ravi.
Rahvusvahelistest juhenditest kaasati kolm juhendit (39, 196, 378). NICE ravijuhendis (196) ei soovitata avatud arterioosjuha ravida, kui see ei põhjusta olulisi kliinilisi probleeme (kasvava hingamistoetuse vajadus, kopsuverejooks, seedetrakti ja/või neerude hüpoperfusiooni tunnused vmt) (vt lisa 10). RDS-i juhendis soovitatakse ravi vajava hemodünaamiliselt olulise arterioosjuha farmakoloogiliseks sulgemiseks kasutada indometatsiini, ibuprofeeni või paratsetamooli. Paratsetamool on eelistatud trombotsütopeenia või neerufunktsiooni häirete korral. (39)
Kanada Lastearstide Seltsi juhendis soovitatakse kaaluda selektiivset profülaktikat veenisiseselt indometatsiiniga erakordselt väikese sünnikaaluga vastsündinutel (ELBW), kellel on suur risk saada III-IV astme IVH (378). Indometatsiini profülaktikat toetab Saksamaal tehtud mitmekeskuse jälgimisuuring, kus koorionamnioniidiga kulgenud raseduse puhul enne 26. GN-i sündinud vastsündinutest oli IVH esinemine väiksem nendel, kes said PDA profülaktikat indometatsiiniga, võrreldes nendega, kes seda ei saanud (379). Samas, enne 25. GN-i sündinud lastel tehtud jälgimisuuringus ei leitud erinevust olulistes tulemusnäitajates (surm või BPD, surm, BPD mõõdukas/raske või IVH III-IV a, NEK või SIP) nende laste vahel, kes said alla 24 tunni vanuses indometatsiini, võrreldes nendega, kellel rakendati ootamistaktikat (380). Seetõttu ei ole rutiinne PDA profülaktika enneaegsetel vastsündinutel põhjendatud/näidustatud.
Kanada lastearstide juhend lubab sünnijärgse nädala või paari jooksul valida PDA ravis konservatiivse lähenemise, eriti kliiniliselt stabiilsete enneaegsete puhul (378). AAP soovituse kohaselt peaks eesmärgistatud varajane ennetamine indometatsiiniga olema soovitatud ainult nendes üksustes, kus on väike spontaanse sulgumise arv, ja ainult väga hoolikalt valitud patsientidel (< 26 GN, < 750 g). Paratsetamoolil on vähem kõrvaltoimed kui indometatsiinil või ibuprofeenil, kuid selle mõjust neuroloogilisele arengule on liiga vähe andmeid, et soovitada seda ennetava ravina. (381)
Varasemast indometatsiini profülaktilise ravi uuringust erakordselt enneaegsetel vastsündinutel teame, et elumus ilma neurosensoorse arengu kahjustuseta ei erinenud profülaktilise ravi ja platseeborühma vahel. (382)
PDA varajane eesmärgistatud farmakoloogiline ravi on soovitatav enne 28. GN-i sündinutel, kes on vähem kui kuue päeva vanused, ja kui tegemist on mõõduka kuni suure/laia hemodünaamiliselt olulise šundiga ja suurema kui minimaalse hingamistoetusega (nt > 2L vooluga HF toetusel, > 0,25 FiO2). See soovitus annab näidustuse ehhokardiograafiliseks skriininguks kõigil enne 28. GN-i sündinud lastel, kes vajavad hingamistoetust enne kuue päeva vanust. Nendel vastsündinutel, kes hingamistoetust ei vaja (asümptomaatilised vastsündinud) või kellel on väike PDA šunt, võib olla õigustatud konservatiivne lähenemine. (381)
Ravi vs. ootav taktika
Konservatiivse ravi (vedeliku piiramine, diureetikumid ja hingamistoetus) ja farmakoloogilise ravi ja/või kirurgilise ravi võrdlust käsitleti metaanalüüsis, kuhu oli kaasatud 12 kohortuuringut (N = 41 804) ja neli juhuslikustatud kontrolluuringut (N = 720). Juhuslikustatud kontrolluuringute põhjal ei olnud vahet suremuses, BPD-s, NEK ja IVH, ROP esinemises konservatiivset ravi vs. farmakoloogilist või kirurgilist ravi saanute vahel. Kohortuuringute põhjal oli suremus suurem konservatiivset ravi saanute seas, kui võrrelda farmakoloogilist või kirurgilist ravi saanutega. Samas esines konservatiivse ravi rühmas vähem BPD-d, NEK-d, IVH-d ja ROP-d. (384)
Kahe aasta vanuses ei olnud CP esinemise osas erinevust 6–12 tunni vanuses eesmärgistatud ibuprofeenravi saanute ja platseeborühma vahel. (385)
PDA ravi pööre ootava taktika suunas on ajendatud 2023. aastal avaldatud mitmekeskuse juhuslikustatud uuringu põhjal, kus enne 28. GN-i sündinud enneaegsed juhuslikustati ootava taktika või varajase ibuprofeenravi rühma (mediaanvanus 63 h). Ootava taktikaga lastel oli väiksem risk komposiittulemiks NEK, mõõdukas/raske BPD/surm ning eraldi mõõduka/raske BPD kujunemiseks. Suremuse ja NEK esinemissageduses/riskis erinevust ei olnud. (386)
Loomkatsetest on esile kerkinud mure paratsetamooli mõjust aju arengule, kuna on kirjeldatud kognitiivseid ja käitumuslikke häireid. Inimestel tehtud uuringutes on täheldatud seost prenataalse paratsetamooli ekspositsiooni ja kõne hilinemise ning aktiivsus- ja tähelepanuhäirega. (387, 388)
PDA farmakoloogilise ravi doosid on toodud lisas 9.
Ibuprofeeni standarddoos PDA puhul on 10 mg/kg esimese doosina, järgnedes 5 mg/kg 24 tunni järel ja 48 tunni järel esimesest doosist. 2020. aasta Cochrane’i analüüsis käsitleti kolme uuringut väga väikese sünnikaaluga või enneaegsetel lastel, võrreldi omavahel suures doosis ibuprofeenravi (15–20 mg/kg esimene doos ja 7,5–10 mg/kg 24 h ning 48 h järel esimesest doosist veenisisesi või suukaudselt) ja standarddoosis ibuprofeenravi veenisisesi või suukaudselt PDA sulgemisel. Suures doosis ibuprofeenravi saanutel oli PDA sulgemisel vähem ebaõnnestumisi võrreldes standarddoosiga. Seejuures NEK või gastrointestinaaltrakti verejooksude esinemises kahe rühma vahel erinevust ei olnud. (389)
Seetõttu võib teisese ravivalikuna või vajadusel esmase valikuna kaaluda PDA farmakoloogilist sulgemist ibuprofeeniga suuremas doosis (vt lisa 10).
Kokkuvõttes: nii indometatsiin, ibuprofeen kui ka paratsetamool on efektiivsed sümptomaatilise PDA ravis võrreldes mitteravimisega (kõrge tõendatuse aste indometatsiinil, mõõdukas tõendus ibuprofeenil ja madal tõendatuse aste paratsetamoolil). Suures doosis ibuprofeen on PDA sulgemisel tõhusam kui standarddoosis ibuprofeen (383, 389). Samas võib PDA puhul ootava taktika korral olla väiksem risk enneaegsusega seotud probleemideks komposiittulemina (surm, NEK, BPD) või eraldi BPD-na (386).
Töörühma hinnangul hakatakse oluliselt avatud arterioosjuha ravi arutama neljandal kuni viiendal elupäeval. Südame ultraheliuuring tehakse kliiniliste probleemide korral. Töörühm pidas tähtsaks sõnastada selle jaoks uus praktiline soovitus.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K26 ning ajakohastatud ravijuhendi kliiniliste küsimuste nr 25 ja 27 TõKo ja SoKo tabeleid.
Antibakteriaalne ravi vastsündinule
| 108 |
Infektsiooni riskiteguritega enneaegsel vastsündinul kaaluge profülaktilist antibakteriaalset ravi (vt lisa 11). Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 109 |
Enneaegsel vastsündinul kasutage empiirilise antibakteriaalse ravi esmavalikuna penitsilliini (bensüülpenitsilliin või ampitsilliin) ja gentamütsiini kombinatsiooni (vt lisa 12). |
|
| 110 |
Enneaegse vastsündinu empiiriline antibakteriaalne ravi lõpetage 48–72 tunni pärast, kui puudub infektsioonile viitav kliiniline ja laboratoorne leid ning bakteriaalsed külvid on negatiivsed. Tugev positiivne soovitus, madal tõendatuse aste |
NICE ravijuhendis (390, 391) on soovitatud vastsündinu puhul, kellel esineb mõni oluline riskitegur või kaks ja enam riskitegurit või kliinilist sümptomit (vt lisa 11), teha verest CRP analüüs ja teha verekülv ning alustada empiirilist antibakteriaalset ravi. Empiirilist antibakteriaalset ravi tuleks alustada kohe, enne analüüsi tulemuste saabumist. Kui vastsündinul ei ole suurt riski, on ainult üks riskitegur või üks kliiniline sümptom, tuleks otsus teha tema üldseisundi põhjal individuaalselt. Kui empiirilist antibakteriaalset ravi ei alustata, tuleks last jälgida vähemalt 12 tundi (pidev monitooring 0–2 elutunni vanuses, edasi 2 tunni tagant 10 tunni jooksul). Hemogrammi 5-osalise leukogrammiga, vereäige mikroskoopia ja prokaltsitoniini tundlikkust vastsündinu varajase algusega infektsiooni välistamiseks hinnatakse ebapiisavaks.
Enne 37.+0 GN-i sündinud heas üldseisundis vastsündinul, kelle veeta periood on 18 või enam tundi, soovitatakse rakendada sepsise osalist diagnostilist hindamist (verekülv sünnil, hemogramm 5-osalise leukogrammiga, vereäige mikroskoopia, trombotsüütide arv sünnil ja/või 6–12 tunni vanuses) koos jälgimisega ≥ 48 tundi. Kui dünaamikas ilmnevad sepsise kliinilised sümptomid, on vajalik sepsise täielik diagnostika ja antibakteriaalse ravi alustamine (398, 399).
Ravijuhendis on soovitatud ema koorionamnioniidi kahtluse korral alustada empiirilist antibakteriaalset ravi heas üldseisundis vastsündinul pärast sepsise osalist diagnostikat laia toimespektriga antibiootikumiga kuni verekülvide kohta vastuste saabumiseni (398). Liikvori analüüs ja röntgeniülesvõte rindkerest rutiinselt vajalikud ei ole. Uus-Meremaa konsensusjuhises, Šveitsi neonatoloogiaühingu ja Šveitsi pediaatrilise infektsioonhaiguste grupi 2013. aastal muudetud juhendis on soovitatud vastaval juhul rakendada hoolikat jälgimist esimesed 48 tundi, uuringud ja antibakteriaalne ravi on vajalikud ainult sepsise sümptomite ilmnemisel (392). Vastsündinul, kellel esinevad sepsise sümptomid, tuleb teha täielik diagnostiline hindamine (hemogramm 5-osalise leukogrammiga, vereäige mikroskoopia, verekülv, liikvorikülv, näidustusel röntgeniülesvõte rindkerest) ning alustada laia toimespektriga antibakteriaalset ravi, oodates külvide vastuseid (398, 400). Vaatamata väikesele spetsiifilisusele on sepsisele viitavate kliiniliste sümptomite tundlikkus suur, nende alusel leitakse enamik antibakteriaalset ravi vajavatest vastsündinutest (392, 401) (vt lisa 14).
Antibakteriaalse ravi kestus
Korduv CRP soovitatakse määrata 18–24 tunni jooksul pärast antibakteriaalse ravi alustamist. Korduvat CRP kontsentratsiooni määramist võib kasutada antibakteriaalse ravi juhtimiseks varajase algusega infektsiooni riskiteguritega VLBW-vastsündinutel. Seerumi prokaltsitoniini määramine olulist lisainfot ei anna (391).
Uuringutes, kus võrreldi varajase sepsise kahtluse tõttu alustatud kolme- või viiepäevase empiirilise antibakteriaalse ravi ebaõnnestumist kaaluga üle 1500 g ja/või vanusega alla 34 GN-i enneaegsetel ja ajalistel vastsündinutel, ei leitud erinevust ravi ebaõnnestumises (404).
Antibakteriaalset ravi soovitatakse jätkata, kui vastsündinu verekülv on positiivne, püsib sepsise kahtlus kliiniliste sümptomite alusel ja/või ravivastus on halb. Positiivse verekülviga vastsündinutel on näidustatud lumbaalpunktsioon. Antibakteriaalset ravi soovitatakse jätkata ka juhtudel, kui verekülv on negatiivne ja lapse üldseisund hea, aga laboratoorsed analüüsid ei ole normis ja ema sai sünnituse ajal antibakteriaalset ravi (394).
Antibakteriaalse ravi valik
Töörühma tugev soovitus ravi alustamisel eelistada esmavalikuna gentamütsiini kombinatsiooni penitsilliiniga põhineb kliinilistel uuringutel, NICE ravijuhendi soovitustel ja teadaoleval vastsündinu varajase sepsise tekitajate struktuuril. Tuleb möönda, et kõik juhendis esitatud juhuslikustatud kontrolluuringute tõendid olid madala kvaliteediga; erinevate gestatsioonivanuste kohta ei olnud tõendid võrdselt kättesaadavad (391, 392). Tõendid, mis tulenevad seireandmetest ja kliinilisest praktikast, näitavad, et penitsilliini ja aminoglükosiidi kombinatsiooniga saab edukalt ravida enamikku varajase algusega neonataalse infektsiooni juhtudest. Ühendkuningriigi andmetel toimib bensüülpenitsilliini ja gentamütsiini kombinatsioon 95–97% vastsündinu varajase infektsiooni tekitajate puhul. Kombinatsiooni eeliseks on võrreldes ampitsilliini ja amoksitsilliiniga kitsam toimespekter, mis võiks vähendada antibiootikumiresistentsuse kujunemist (378). Samas on mitmes uuringus leitud, et VLBW-vastsündinute sagedasimaks varajase sepsise tekitajaks on enterobakterid (eeskätt Escherichia coli), mille vastu bensüülpenitsilliini ja gentamütsiini kombinatsiooni kasutamisel toimiks efektiivselt ainult aminoglükosiid (378, 402, 405–407). Aminoglükosiid- monoteraapia efektiivsuse kohta kliiniliste uuringute andmed puuduvad.
Eestis tehtud juhuslikustatud kontrolluuringus ei esinenud kliiniliselt olulistes ravitulemites, nagu varajane surm ja antibakteriaalse ravi vahetamise vajadus, aga ka kolonisatsioon ampitsilliiniresistentsete mikroorganismidega, statistiliselt märkimisväärset erinevust penitsilliini- vs. ampitsilliini-gentamütsiini kombinatsiooni vahel (406). Uuringu andmetel oli enne 26.+0 GN-i sündinud enneaegsete suremus intensiivravi osakonnas väiksem ampitsilliini-gentamütsiini rühmas. Samas oli viimati nimetatud kombinatsioon seotud suurema Klebsiella pneumoniae kolonisatsiooniga, sisaldades ampitsilliiniresistentseid tüvesid. Tuleb märkida, et uuringu võimsus ei olnud piisav alarühma analüüside tegemiseks.
Kui haigustekitaja on isoleeritud, peaks edasine antibakteriaalne ravi lähtuma mikroorganismi antibiootikumitundlikkusest.
Vastsündinu varajase algusega infektsiooni riskitegurid, kliinilised sümptomid vastsündinu võimaliku varajase infektsiooni korral ja antibiootikumide annused on toodud lisas 15.
Ravijuhendi ajakohastamisel avati algse juhendi kliiniline küsimus. Lisaotsinguga leiti kaks metaanalüüsi ja kaks jälgimisuuringut. Seitset RCT-d kaasavas metaanalüüsis ei leitud erinevust nekrotiseeriva enterokoliidi tekkimisel üle viie päeva kestnud antibiootikumravi kasutamisel võrreldes selle mittekasutamisega, kuid võrdluses üle viie päeva kestnud profülaktilise antibiootikumravi ja üks kuni neli päeva kestnud profülaktilise raviga oli NEK risk kasvanud pikemaaegsel antibiootikumravi kasutamisel (408). Samuti leiti teises metaanalüüsis, kuhu kaasati viis jälgimisuuringut, et profülaktilise antibiootikumravi kasutamine üle viie päeva seostub NEK suurema riskiga (409).
Kanadas tehti aastatel 2010–2016 mahukas kohortuuring, kus väga väikse sünnikaaluga vastsündinutel (˂ 1500 g) leiti suurem suremus või komposiittulem (raske neuroloogiline kahjustus, nekrotiseeriv enterokoliit, BPD, ROP või haiglatekkene infektsioon), kui antibiootikumravi oli kestnud üle kolme päeva (410). Teise jälgimisuuringu tulemustena leiti, et suurem on bronhopulmonaalse düsplaasia ja hilise sepsise esinemine juhul, kui antibiootikumravi kasutati pikemalt kui viis päeva (411).
Enneaegsus üksi ei ole antibiootikumravi alustamise näidustus. Profülaktiline antibakteriaalne ravi peab lähtuma vastsündinu infektsiooni riskiteguritest, kliinilistest sümptomitest, kuid lähenemine peab olema individuaalne ning antibiootikumravi peab olema lühikese kestusega. Enne antibiootikumravi alustamist tuleb selgitada, kas ema on saanud enne sünnitust antibiootikumravi (nt GBS-i korral, pika veeta perioodi jooksul). Samas on tähtis, et ükski riskiteguriga vastsündinu ei jääks vajadusel ravita, kuid pigem liigutakse sinnapoole, et arvestatakse antibiootikumravist tingitud kõrvaltoimetega.
Vaata lisaks www.ravijuhend.ee 2017. aastal koostatud algse ravijuhendi tõendusmaterjali kokkuvõtet EvSu K27 ning ajakohastatud ravijuhendi kliinilise küsimuse nr 28 TõKo ja SoKo tabeleid.
Valu hindamine ja valuravi
| 111 |
Enneaegse vastsündinu valu hindamiseks kasutage standarditud skooringut. Skooringu korrektseks rakendamiseks peavad kasutajad olema vastavalt koolitatud. |
|
| 112 |
Kõikidel enneaegsetel vastsündinutel (k.a invasiivsel või mitteinvasiivsel hingamistoetusel olevatel) ärge kasutage rutiinselt farmakoloogilist valuravi. |
|
| 113 |
Enneaegsel vastsündinul kasutage valuravi selektiivselt, lähtudes valuskooringu tulemustest ja planeeritava sekkumise iseloomust (vt lisa 13). |
Vastsündinud intensiivravi osakonnas läbivad 10–15 valulikku protseduuri päevas. Valu põhjustab otseseid kardiovaskulaarseid ja käitumuslikke muutuseid, suurendab energiakulu ning häirib söömist ja und – need võivad kaasa tuua tüsistusi ja intensiivsema ning pikemaajalise ravi vajaduse. Ebaküps närvisüsteem ja korduv kokkupuude valuga võivad langetada valuläve, mis omakorda võib muuta lapse veelgi tundlikumaks järgnevate valulike toimingute suhtes. Valutundlikkuse muutused võivad ulatuda kaugemale vastsündinu perioodist ning põhjustada probleeme neuroloogilises arengus. (412)
Arvestades ühe kindla kuldstandardina kasutatava skaala puudumist, sisaldavad enamik riiklikke ja rahvusvahelisi juhendeid nimekirja kehtivatest ja usaldusväärsetest tööriistadest, mitte ei soovita konkreetset valu hindamise tööriista. Samuti rõhutatakse ühtse valuskooringu rakendamise ja personali koolitamise protsessi tähtsust raviasutustes. (413)
2019. aasta süstemaatilises ülevaates nimetati enneaegsetel kasutatavad valuskooringud, millel on võrreldes teistega väiksem nihke tõenäosus: COMFORT, EDIN, NFCS, N-PASS ja PIPP (414).
Eestis on seni kasutusel olnud valuskooringud FLACC, NIPS. Töörühm leidis, et valu hindamine enneaegsetel vastsündinutel on oluline, kuid tõendusmaterjali põhjal ei ole võimalik kindlat mõõdikut soovitada.
Valuravi
Rahvusvaheliste juhiste järgi peaks kaaluma premedikatsiooni (opioidanalgeetikumi ja neuromuskulaarse blokaatori kombinatsiooniga või propofooliga) enne plaanilist mitte-erakorralist intubatsiooni enneaegsetel imikutel. Lisaks ei soovitata kasutada hingamistoetusel olevatel enneaegsetel imikutel rutiinselt opioide (morfiini, midasolaami), vaid hinnata lapse valu kokkulepitud skooringuga ning teha otsuseid valuravi kohta vastavalt. Opioidi kasutamisel tuleks last monitoorselt jälgida, valu ja analgeesia efekti regulaarselt hinnata, kuna valu ja stress võivad viia ventilaatori asünkroonsuse, suboptimaalse ventilatsiooni ja kardiovaskulaarne ebastabiilsuseni. Opioidi kasutamise ajal tuleks muude sekkumiste läbiviimise korral kaaluda täiendavaid valuvaigistavaid (mittefarmakoloogilisi) meetmeid. Tähtis on opioidi manustamine võimalikult kiiresti lõpetada ning hinnata last võõrutussündroomi kujunemise osas. (39, 196, 417, 418)
WHO 2017. aasta juhise kohaselt võiks suuremate operatiivsete sekkumiste (nt torakotoomia ja abdominaalne laparotoomia) järel valuraviks kasutada morfiini või fentanüüli vähemalt 24 tunni jooksul, seejuures regulaarselt valu hinnata sobiva skooringuga. Väiksemate sekkumiste (nt songakirurgia) korral võiks rutiinselt kasutada paratsetamooli, valu püsimisel ka opioidi boolust.
Töörühm leidis, et analüüsitud uuringute põhjal ei ole valuvaigistite kasutamisel suurt efekti. Farmakoloogilise valuravi mittekasutamine ei välista mittefarmakoloogiliste sekkumiste kasutamist (vt täpsemalt perekeskse ravi soovitused).
Vaata lisaks ajakohastatud ravijuhendi kliiniliste küsimuste nr 29 ja 30 TõKo ja SoKo tabeleid.
Aju piltdiagnostika
| 114 |
Enneaegsel vastsündinul, kes on sündinud enne 32.+0 GN-i või kelle sünnikaal on < 1500 g, eelistage aju ultraheliskriiningut. |
|
| 115 |
Enneaegsele vastsündinule, kes on sündinud 32.+0–36.+6 GN-il, ärge pigem tehke aju ultraheliskriiningut (vt lisa 14). |
|
| 116 |
Enneaegsel vastsündinul, kes on sündinud 32.+0–36.+6 GN-il ja kellel kaasuvad enneaegsusega teised haigusseisundid või riskitegurid, eelistage aju ultraheliuuringut. Uuringu ajastus sõltub lapse seisundist (vt lisa 14). |
|
| 117 |
Enneaegsel vastsündinul, kes on sündinud enne 28. GN-i, kaaluge PMV-s 38–40 nädalat aju MRT uuringut. |
Enne 28. GN-i sünnib Eestis 0,5% lastest ehk umbes 50 last aastas. Handi jt 2020. aasta uuringus (419) selgus, et 63%-l vastsündinutest, kes sünnivad 22.–23.+6 GNil, esineb IVH-d, neist 36%-l raske IVH (3. või 4. aste). Enamik IVH-st tekib esimese kolme päeva jooksul, 50% hemorraagiatest esimese viie tunni jooksul ja 95% IVH-st seitsmendaks kuni kümnendaks elupäevaks.
Aju ultraheliskriiningul olulise kõrvalekalde leidmisel on näidustatud aju ultraheliuuringu kordamine kord nädalas. Enneaegse vastsündinu seisundi halvenemisel on näidustatud aju ultraheliskriiningu uuesti alustamine (vt lisa 14).
Guillot’ jt 2020. aastal avaldatud konsensusdokumendi (420) kohaselt on kordusuuring lisaks soovitatav neljandal kuni kuuendal elunädalal, et avastada aju valgeaine kahjustusi.
McLeani jt 2021. aasta uuringus (421) on öeldud, et IVH esineb peamiselt enne 32. rasedusnädalat või alla 1500-grammise sünnikaaluga sündinud enneaegsetel lastel, mistõttu ei soovitata rutiinset ultraheliuuringut teha ilma riskiteguriteta heas üldseisundis kasvaval enneaegselt sündinud lapsel.
Enneaegselt sündinud lastel, kellel esineb raske kuluga kaasuv haigusseisund või riskitegurid, on suurem risk ajupatoloogia kujunemiseks. Seetõttu soovitatakse aju ultraheliuuringut lastele, kes on sündinud rasedusnädalatel 32+0–36+0, eesmärgiga hinnata üldist aju seisundit, mitte ainult intraventrikulaarset hemorraagiat. Riskiteguriteks võivad olla elustamine, komplitseeritud monokoriaalne rasedus, mikrotsefaalia, SGA, sepsis, nekrotiseeriv enterokoliit ja kirurgilised sekkumised. Roufaeili jt 2022. aasta metaanalüüsis (422), kuhu kaasati juhuslikustamata uuringud, leiti, et SGA vastsündinutel võrreldes AGA vastsündinutega esineb suurem risk IVH tekkeks.
Hinojosa-Rodriguezi jt 2017. aastal avaldatud süstemaatilise ülevaate (423) kohaselt esineb 50–80%-l ekstreemselt ja väga enneaegselt sündinud lastel difuusset valgeaine kahjustust, mille tagajärjel esineb lastel motoorset ja kognitiivset häiret. Guillot’ jt 2020. aasta ülevaateartikli (420) kohaselt on MRT uuringuga võimalik paremini diagnoosida valgeaine mittetsüstilisi muutusi ja väikeaju hemorraagiat. Sama tulemi on avalikustanud Ibrahim jt 2018. aasta ülevaateartiklis (424), mille kohaselt tundlikkus aju valgeaine kahjustuse diagnoosimisel oli 26% ja positiivne ennustatav väärtus 36%. Seevastu tsüstiliste muutuste avastamise tundlikkus oli 75% ja spetsiifilisus 100%. Näidustuste korral võib teha MRT ka suurematele enneaegsetele ja ajaliselt sündinud vastsündinutele (nt terapeutilise hüpotermia lõpetamise järel, perinataalse insuldi kahtlusel).
Töörühma hinnangul ei peaks esimese 24 elutunni jooksul lapsele lisauuringuid tegema. Esimene aju ultraheliuuring peaks olema tehtud kolmandaks kuni viiendaks elupäevaks ning uuring on vajalik kõikidele enneaegsetele vastsündinutele, kes on sündinud enne 32.+0 GN-i. MRT uuringut ei ole mõistlik kõikidele enneaegsetele vastsündinutele teha. Töörühm koostas tõendusmaterjali põhjal lisamaterjali aju piltdiagnostika skriiningu ajastamiseks (vt lisa 14).
Vaata lisaks ajakohastatud ravijuhendi kliinilise küsimuse nr 31 TõKo ja SoKo tabelit.
Perekeskne hooldus ja ravi (vt lisa 15 ja 16)
| 118 |
Enneaegse vastsündinu hoolitsust ja ravi kohandage individuaalselt, soodustades tema arengut ning kaasates, arvestades ja toetades peret. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 119 |
Enneaegse vastsündinuga perele tagage optimaalsed tingimused perekeskseks raviks (piiramata juurdepääs lapsele, vanemate ja personali koostöö, võimaluse korral perepalat, psühhosotsiaalne tugi). Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 120 |
Enneaegsel vastsündinul alustage vaginaalse sünnituse ja keisrilõike järel nahakontakti ema või isaga kohe pärast seisundi esmast stabilisatsiooni, kui vastsündinu seisund seda võimaldab. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 121 |
Enneaegse vastsündinu nahakontakti soodustage kogu haiglaravi jooksul, CPAP-ravi ja invasiivne hingamistoetus ei ole nahakontakti vastunäidustuseks. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 122 |
Enneaegse vastsündinu nahakontakti eelistage kestusega vähemalt üks tund korraga. Nõrk positiivne soovitus, madal tõendatuse aste |
|
| 123 |
Enneaegsel vastsündinul viige valulike vahelesegamiste arv miinimumini, kasutage valu ja stressi leevendamiseks mittefarmakoloogilisi võtteid. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
Uuringute andmetel on emast eemaldamisel lapsele tugev negatiivne mõju, seda nii füsioloogilisele stabiilsusele, psühhosotsiaalsele heaolule kui ka aju arengule. VLBW-lastel, kes viibivad enamiku ajast oma vanematest eemal NICU-s, on suur risk arengu- ja käitumishäireteks (50, 425), nagu tähelepanu defitsiit, kognitiivsed häired, depressioon ja psühhootilised häired, autismispektri häired (426). Uuringutes, kus pered olid täielikult kaasatud NICU meeskonda ja osalesid aktiivselt lapse hoolduses, esines positiivne mõju nii vanematele kui ka lastele (50, 425).
Juhuslikustatud kontrolluuringust, kus käsitleti tõenduspõhiste perekesksete sekkumiste mõju haiglasviibimise ajale, perekesksuse rakendatavust ja ohutust intensiivravi osakonnas enneaegse lapse (raseduskestus 26+0–34+6 GN-i) eest hoolitsemisel, selgus, et lastel ei esinenud suurenenud hapniku- ega ravimivajadust ning sepsise, NEK, krampide ja ROP esinemine ei suurenenud. Perekeskne ravi NICU-s on teostatav ja ohutu (426).
Soovitused perekeskse arengulise ravi põhimõtete kasutamise kohta neonataalses intensiivravi osakonnas (50, 425) on toodud lisas 15.
On leitud, et modifitseeritud NIDCAP (MITP, mother infant transaction programme) vähendab vanemate stressitaset lapse esimesel eluaastal ja sel on kasulik toime lapse kognitiivsele arengule viie aasta vanuses ning IBAIP (infant behavioural assessment and intervention programme) parandab lapse motoorset arengut, eriti VLBW-lastel (50, 425, 427).
Uuringud on näidanud, et nahakontakt (vt lisa 15 ja 16) ja känguruhoolduse rakendamine tagab lapsele parema termoregulatsiooni (50, 428–431) ning sel on positiivne toime kardiorespiratoorsele stabiilsusele ja unele (429, 430, 432), nutuaeg lüheneb, hüpoglükeemia (426) ja nosokomiaalsete infektsioonide (NEK, pneumonia, sepsis) episoodide arv (50, 428, 433) väheneb, samuti lüheneb haiglas viibimise aeg (50, 428) ning väheneb suremus.
Emadel on täheldatud paremat laktatsiooni, pikemat imetamisperioodi (50, 428, 429) ning positiivset toimet vanema-lapse lähedussuhte ja kiindumuse tekkele (50, 428, 434, 435). Känguruhooldus võib parandada ema enneaegse sünnituse järgset negatiivset meeleolu (stressi ja depressiooni) (434). Känguruhooldus on valu leevendava toimega (436).
Nahakontakti rakendamine on ohutu ja efektiivne isegi ventilatsioonil olevatele enneaegsetele lastele (437). Ka VLBW-lapsed suudavad säilitada nahakontakti ajal adekvaatse kehatemperatuuri ja füüsilise stabiilsuse (hingamissagedus, südamesagedus, hapniku saturatsioon) (438).
Nahakontakti tuleks rakendada ka transpordi ajal ühest osakonnast teise (439).
Imetamine perekesksuse kontekstis
Tõhustatud nõustamine hõlmab:
- regulaarset ja personaalselt kohandatud juhendamist imetamise ja rinnapiima sõõrutamise teemal (nt sagedus, tehnika, pumpamise ajastus);
- emotsionaalse ja praktilise toe pakkumist – see aitab emal toime tulla stressi, väsimuse ja sünnitusest füsioloogilise taastumisega;
- tõenduspõhiste strateegiate selgitamist – need toetavad rinnapiima tootmist (nt varajane rinnapiima sõõrutamine (esimese 1–2 tunni jooksul pärast sünni- tust), nahk-naha kontakt, piisav energiasaamine).
Rinnale harjutamine ja ajastus. Kanada Lastearstide Ühingu (Canadian Pediatric Society) 2023. aasta juhiste (442) kohaselt tuleks lapse stabiilse seisundi korral alustada rinnale harjutamist juba PMV-s 28–32 nädalat. See on märkimisväärne muutus võrreldes varasemate suunistega, mis soovitasid alustada imetamist pigem 33.–34. nädalal. Varasem rinnale harjutamine soodustab lapse füsioloogilist stabiilsust ja imemisrefleksi arengut ning suurendab eduka rinnaga toitmise tõenäosust haiglast väljakirjutamisel (443).
Imetamise roll perekesksuse toetamisel. Imetamine on üks olulisemaid vahendeid perekesksuse rakendamisel intensiivravi tingimustes. Rinnapiima pakkumine ja rinnaga toitmine:
- toetab lapse arengut, seedesüsteemi küpsemist ja immuunkaitset;
- loob nahk-naha kontakti ja imetamise protsessi kaudu sideme lapse ja vanemate vahel;
- võimaldab vanematel olla aktiivsed hooldustegevuse osalised, vähendades abitustunnet ning toetades vanemliku kompetentsuse kasvu.
Perepalat
Mittemedikamentoosne valuravi
Süstemaatiliste ülevaadete andmetel on piisavalt tõendeid, et soovitada enneaegsete vastsündinute protseduuriaegseks valuraviks mittefarmakoloogiliste ravivõtetena känguruhooldust/nahakontakti (436), mittetoitelist imemist, kinnimähkimist/ kinnihoidmist (447) ja imetamist või rinnapiima andmist (448). Samasugune mõju on glükoosi/sahharoosi manustamisel, mida kasutada alternatiivina, kui imetamine ei ole võimalik (448).
Süstemaatilises ülevaates, mis põhineb nelja uuringu analüüsil, on soovitatud efektiivseks valuraviks väga väikese sünnikaaluga enneaegsetele manustada rutiinselt sahharoosi 0,012–0,12 g (0,05–0,5 ml 24% sahharoosi) kaks minutit enne ühekordset kannatorget ja veenipunktsiooni (449).
On jõutud järeldusteni, et valulike protseduuride ajal tuleb lapse une kaitsmiseks kasutada valutustamiseks mittefarmakoloogiliste võtete kombinatsioone (imemine, sahharoos, hoidmine). Soovituslikud 20%-lise sahharoosi kogused gestatsiooniajast lähtuvalt on järgmised: 26+0–27+6 GN-i = 0,2 ml; 28+0–29+6 GN-i = 0,5 ml; 30+0–31+6 GN-i = 1,0 ml; 32+0–36+6 GN-i = 1,5 ml; üle 37+0 GN-i = 2,0 ml (450). Alternatiivina sahharoosile võib valu leevendamiseks protseduuri ajal kasutada 1–2 ml 20–30%-list glükoosilahust (451).
Lisad
Lisa 1. Eesti perinataalstatistika 2019–2024 meditsiinilise sünniregistri andmetel
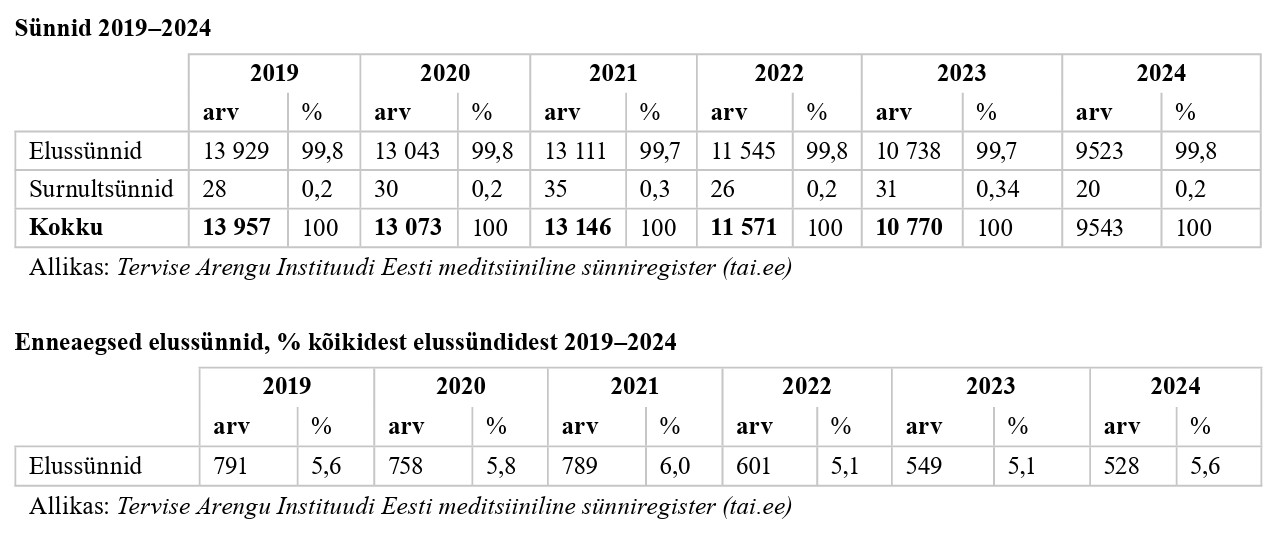
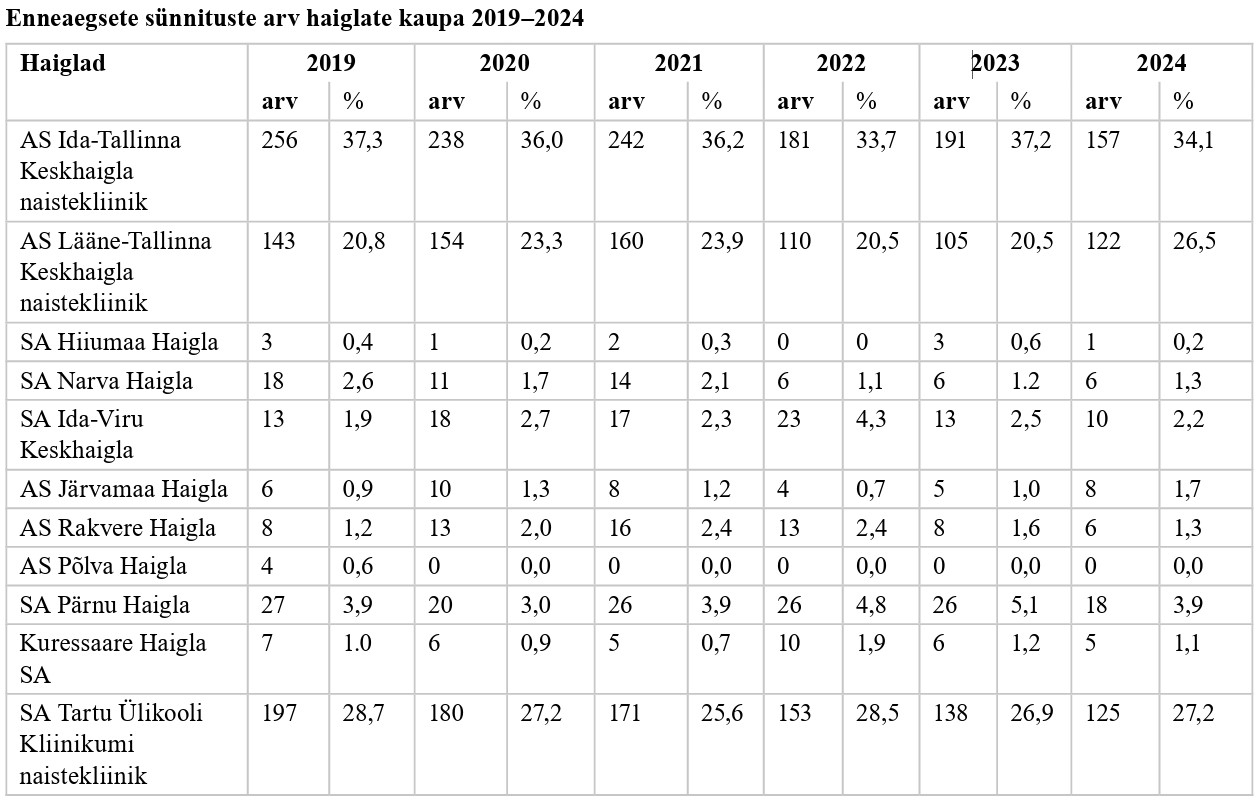
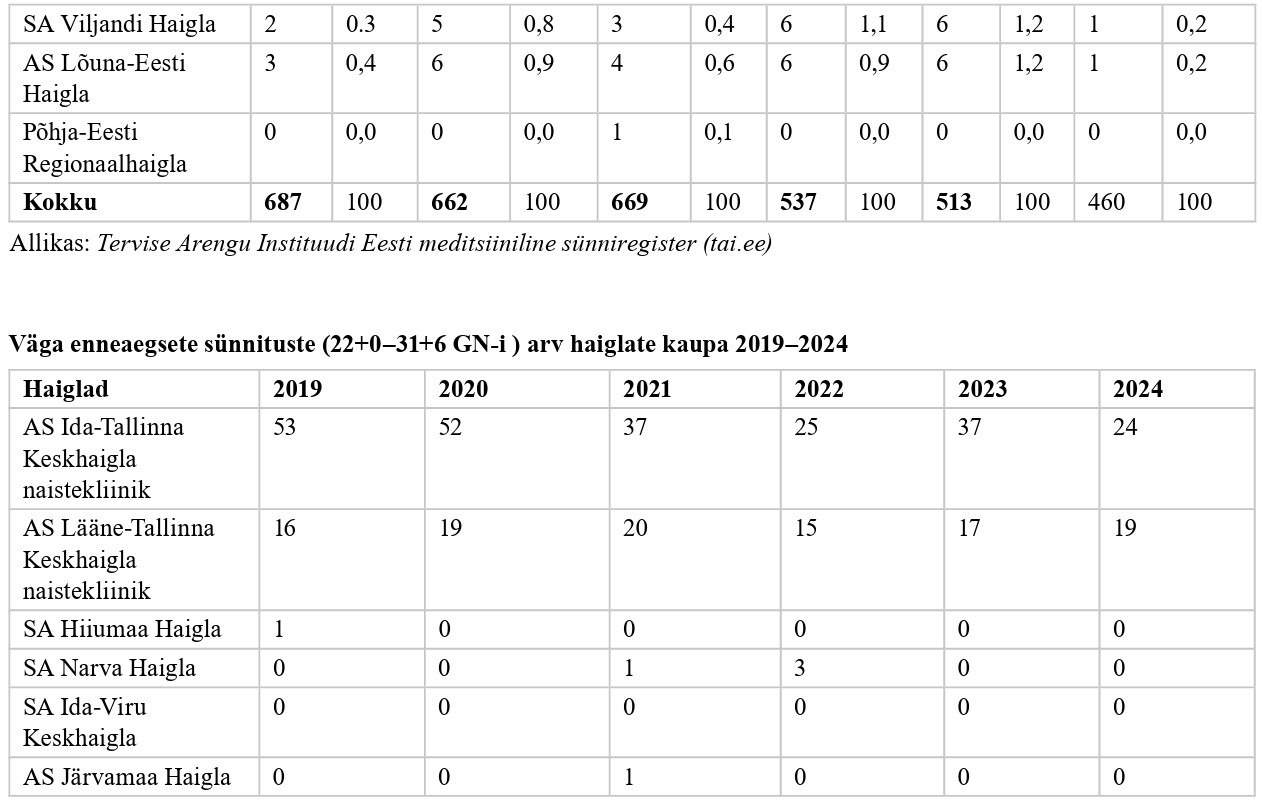
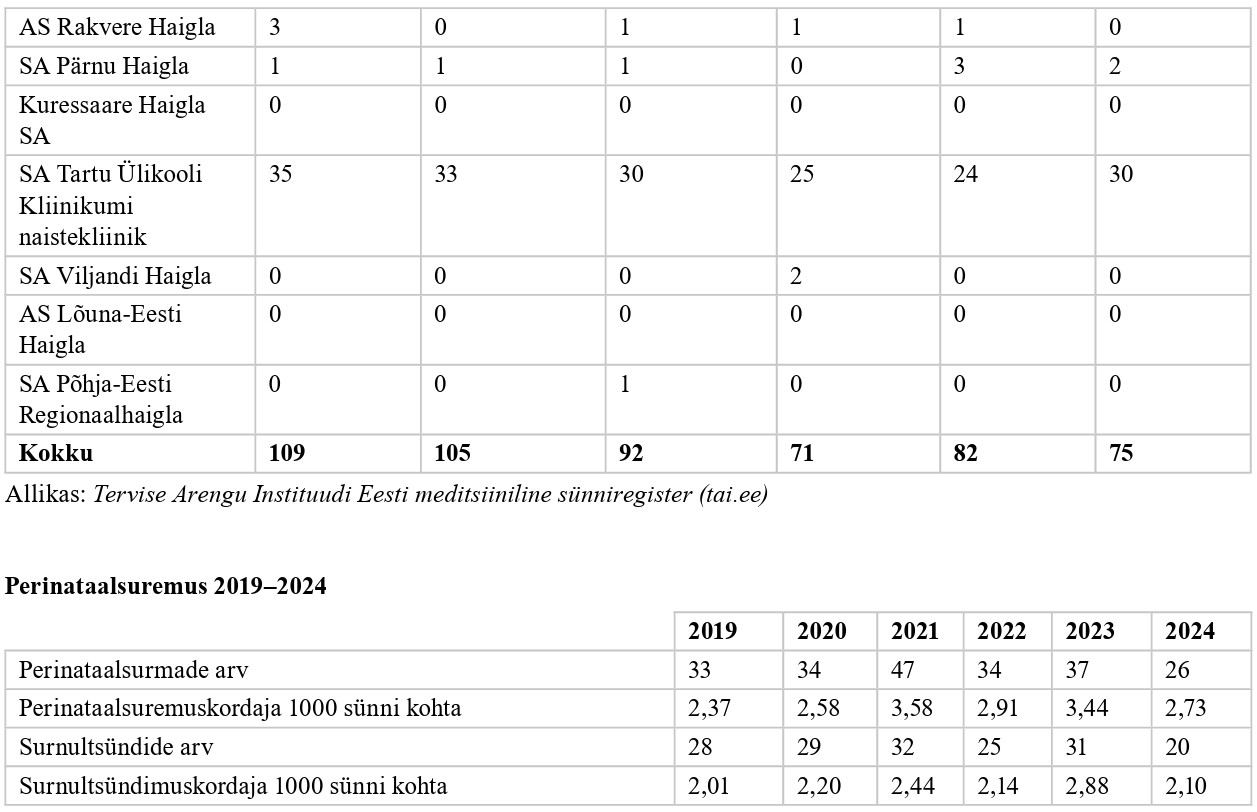
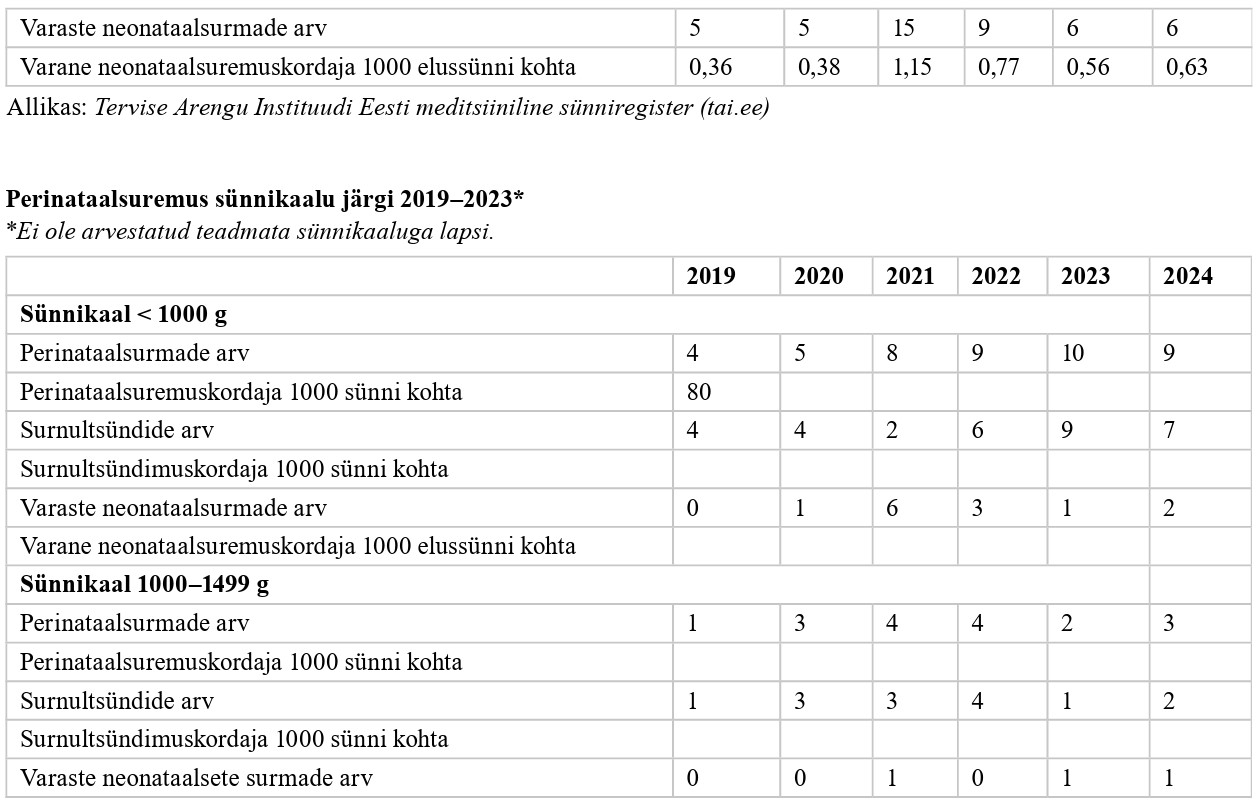
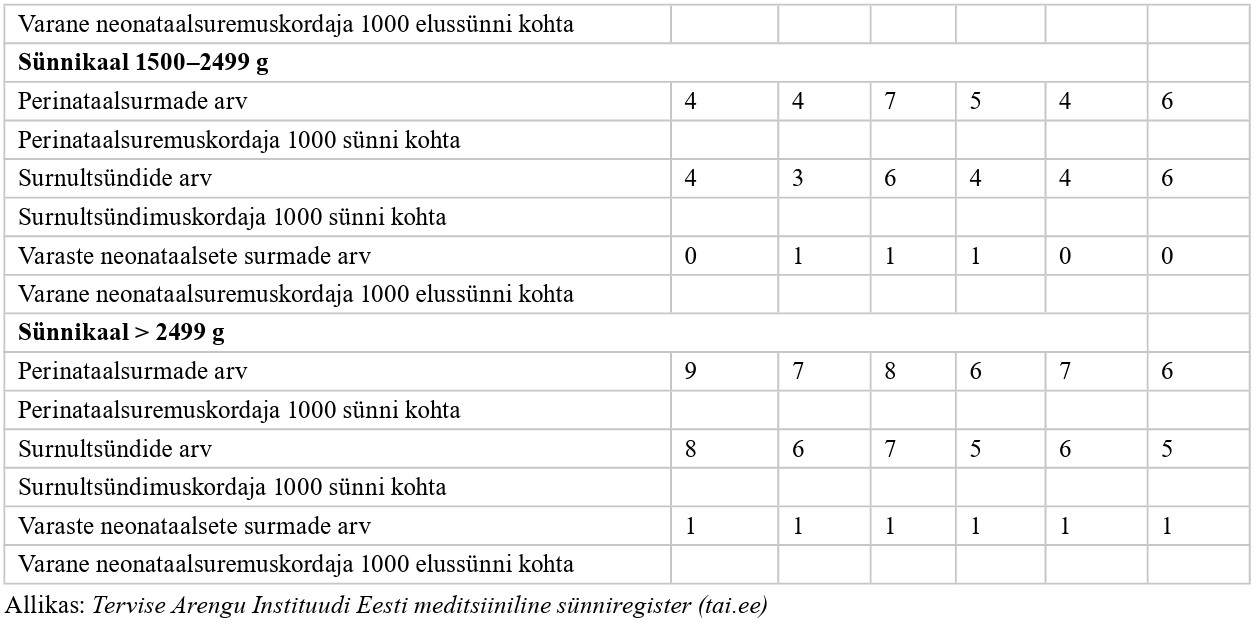
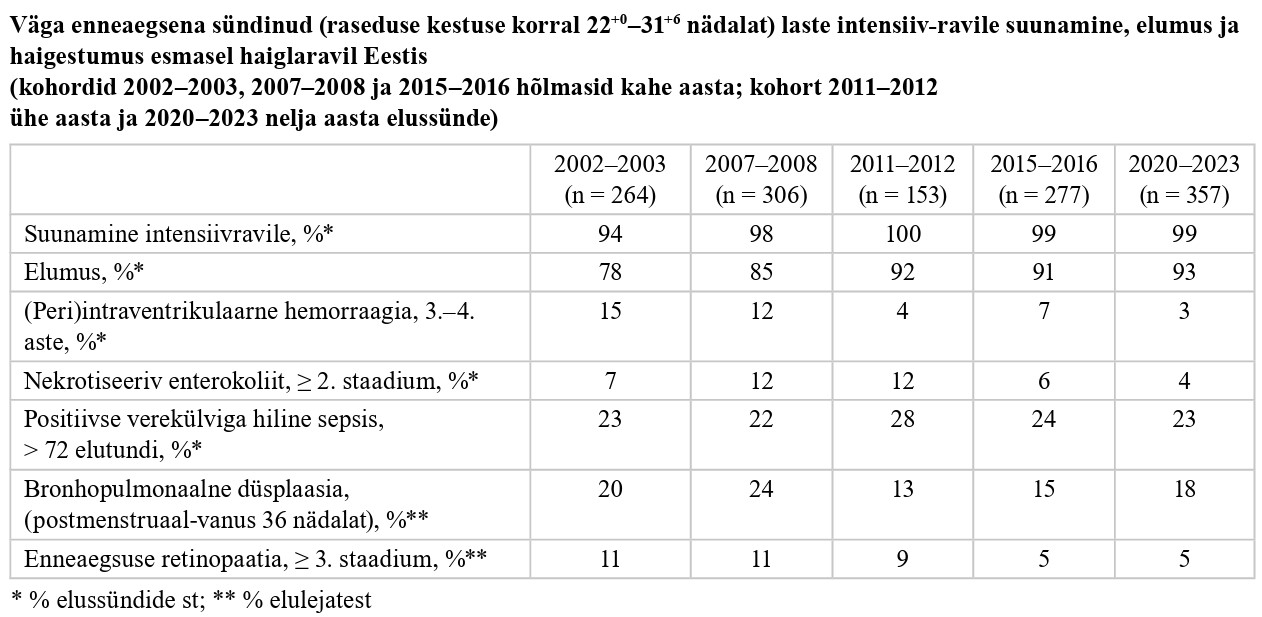
Lisa 2. Proaktiivne ravitaktika ähvardava enneaegse sünnituse korral raseduskestuse puhul 22+0–25+6 GN-i
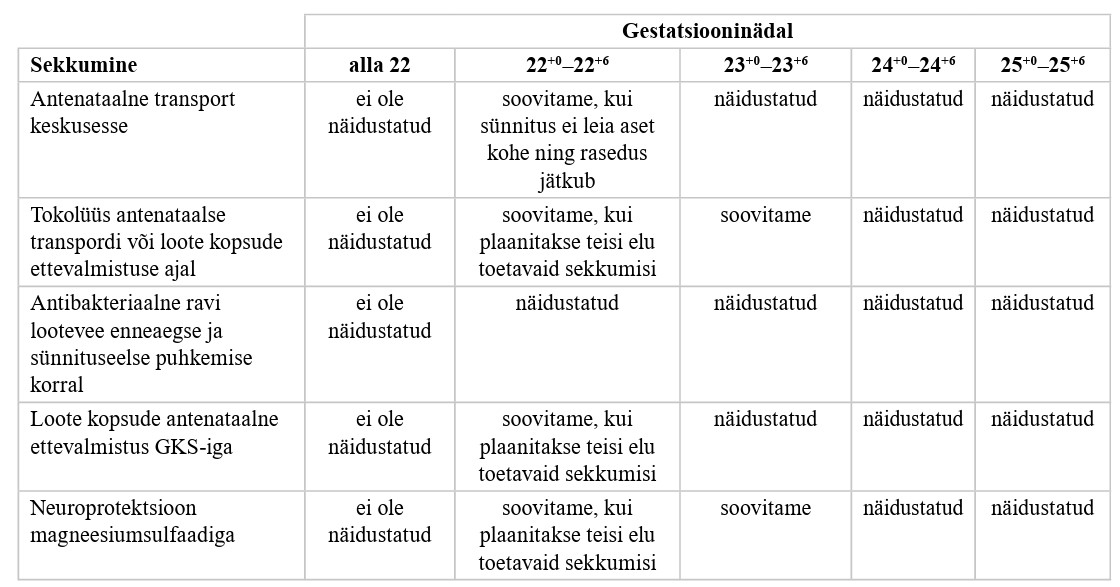
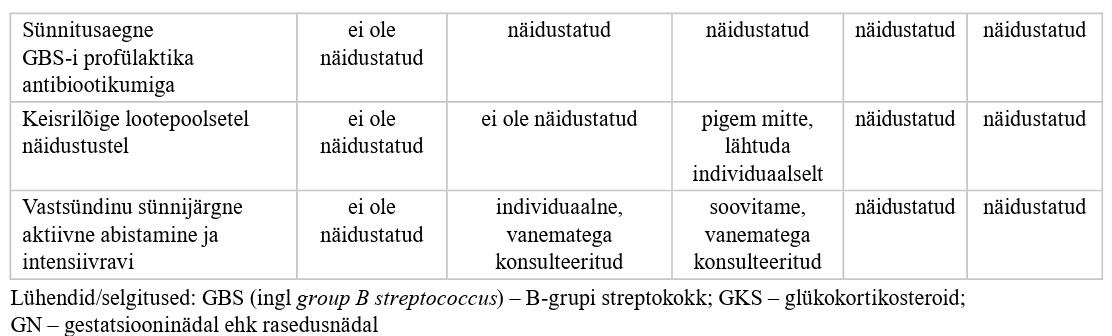
Lisa 3. Magneesiumsulfaadi manustamise jälgimise tabel
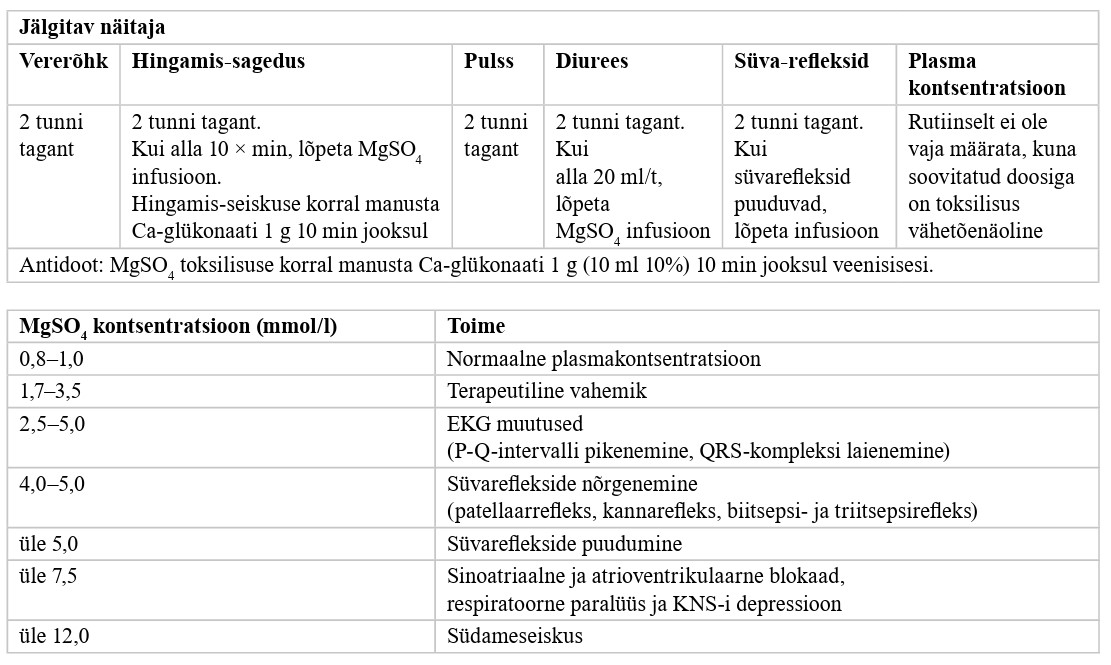
Lisa 4. Koorionamnioniidi kliinilised tunnused ja ravi


Lisa 5. Tokolüütiliste ravimite kasutamine
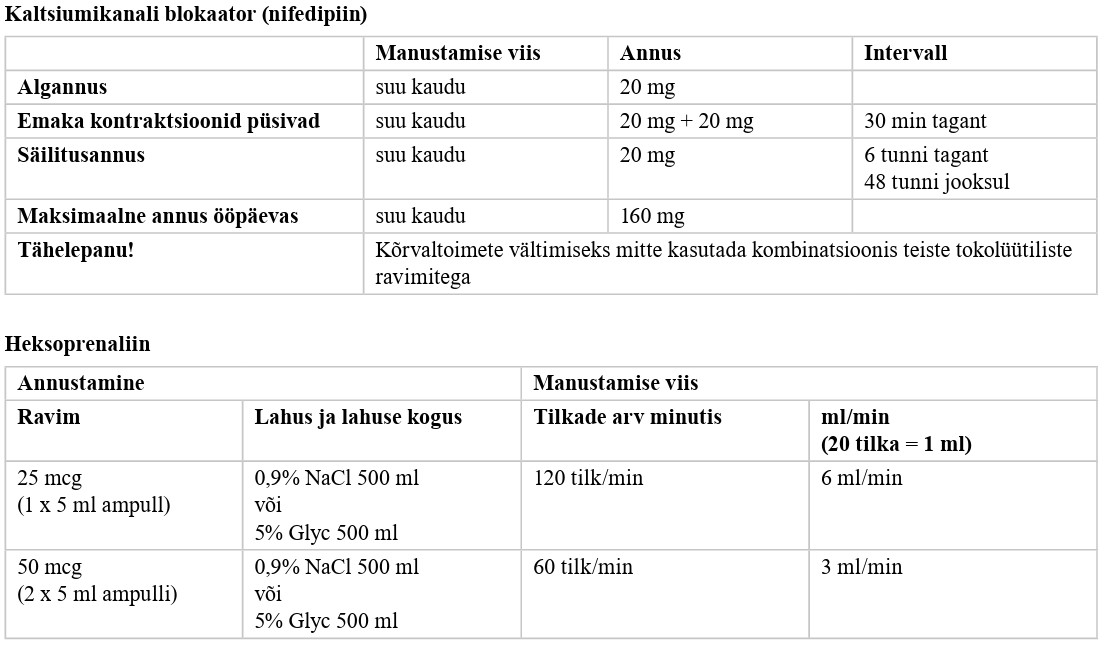
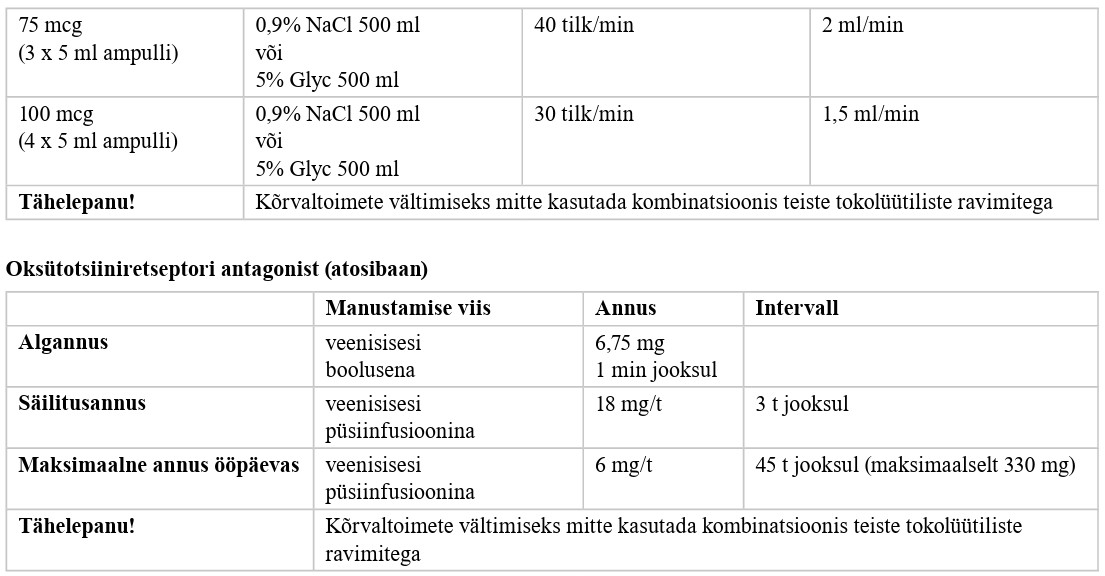

Lisa 6. Euroopas 2013. aastal litsentseeritud surfaktandipreparaadid ja nende annused
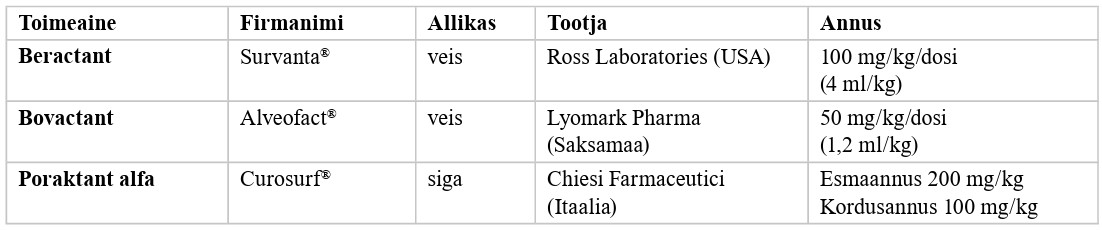
Lisa 7. Enneaegse vastsündinu hüpotensiooni raviks kasutatavad ravimid
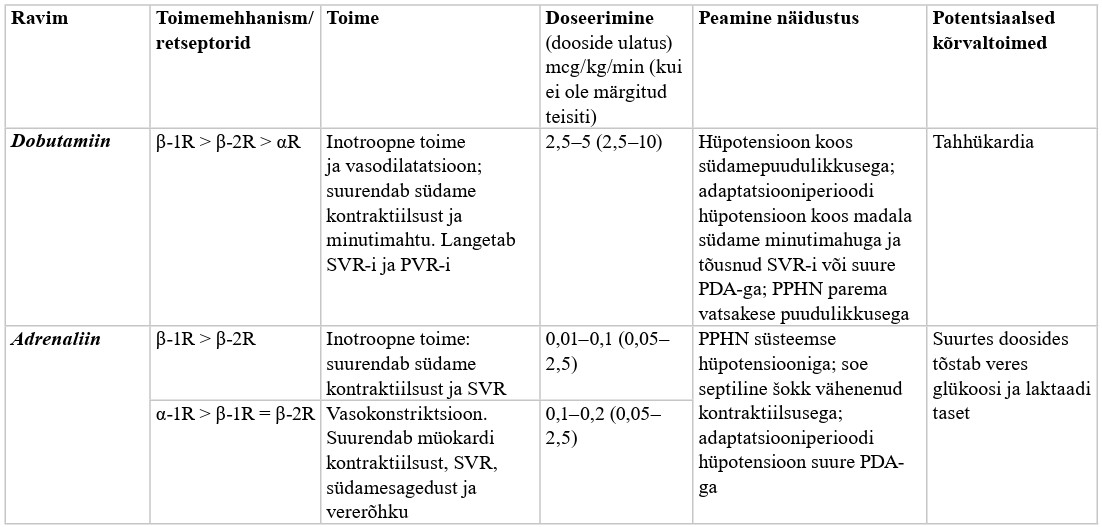
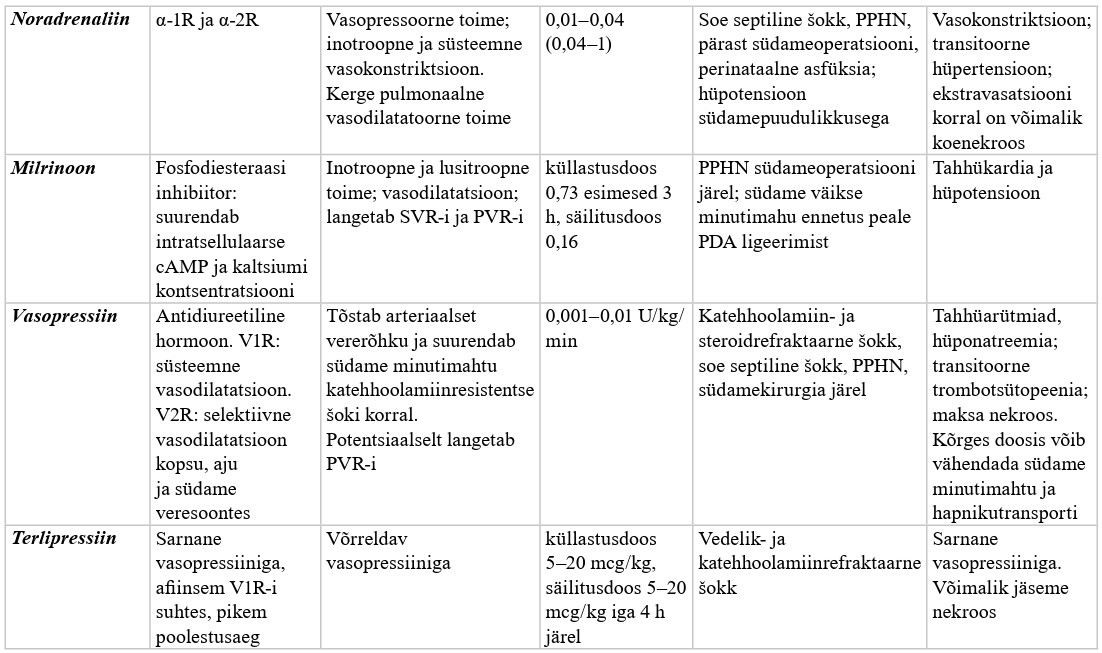
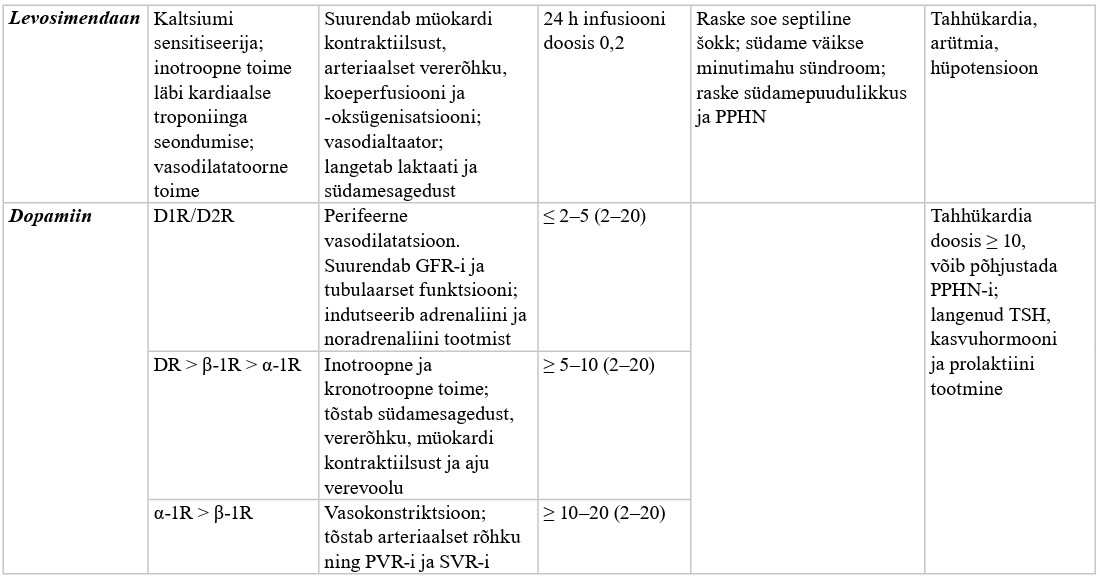
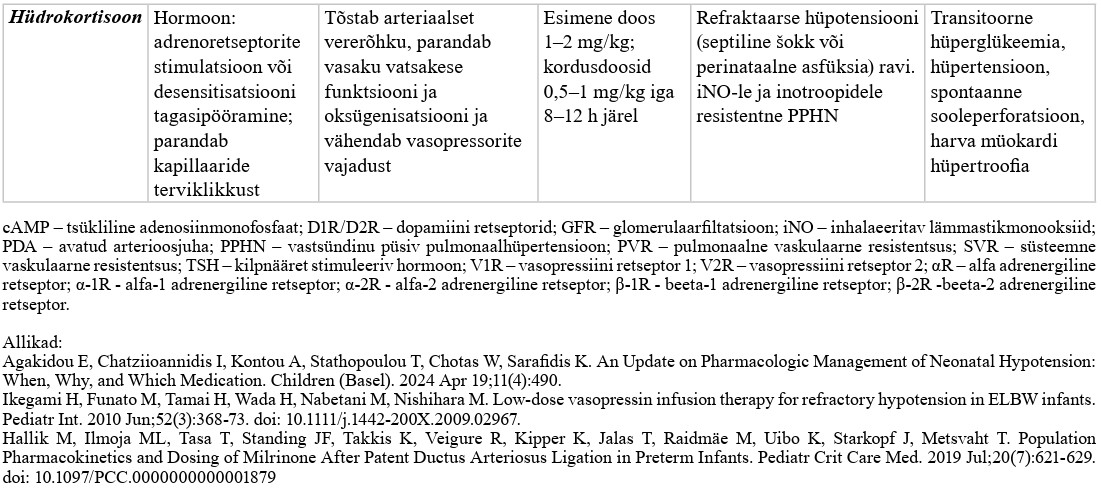
Lisa 8. Soovitatud toitainete- ja vedelikuvajadus väga väikese sünnikaaluga (VLBW) vastsündinul
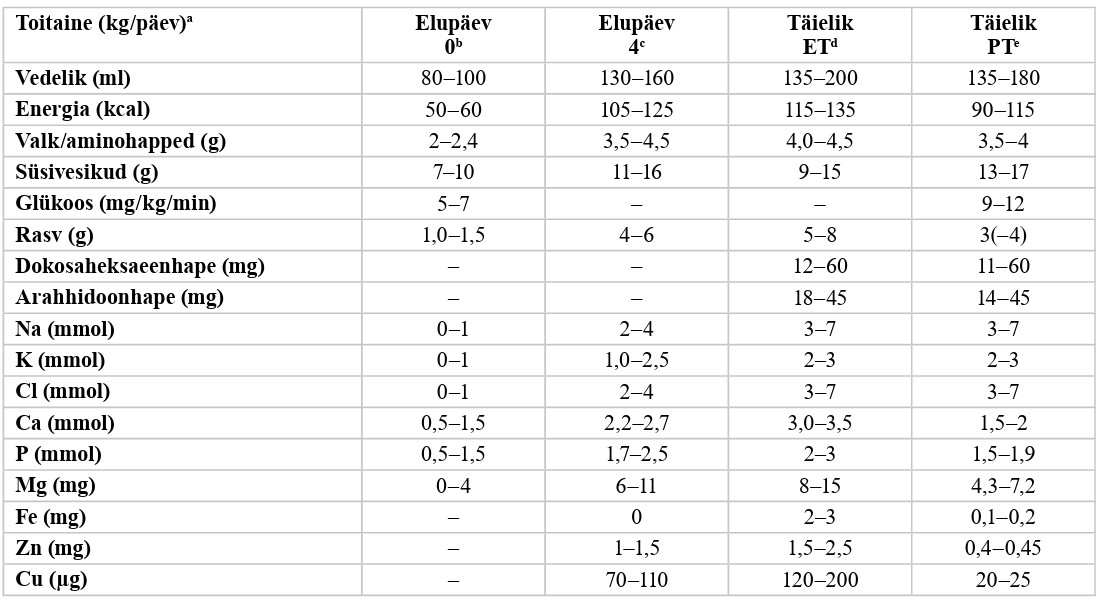
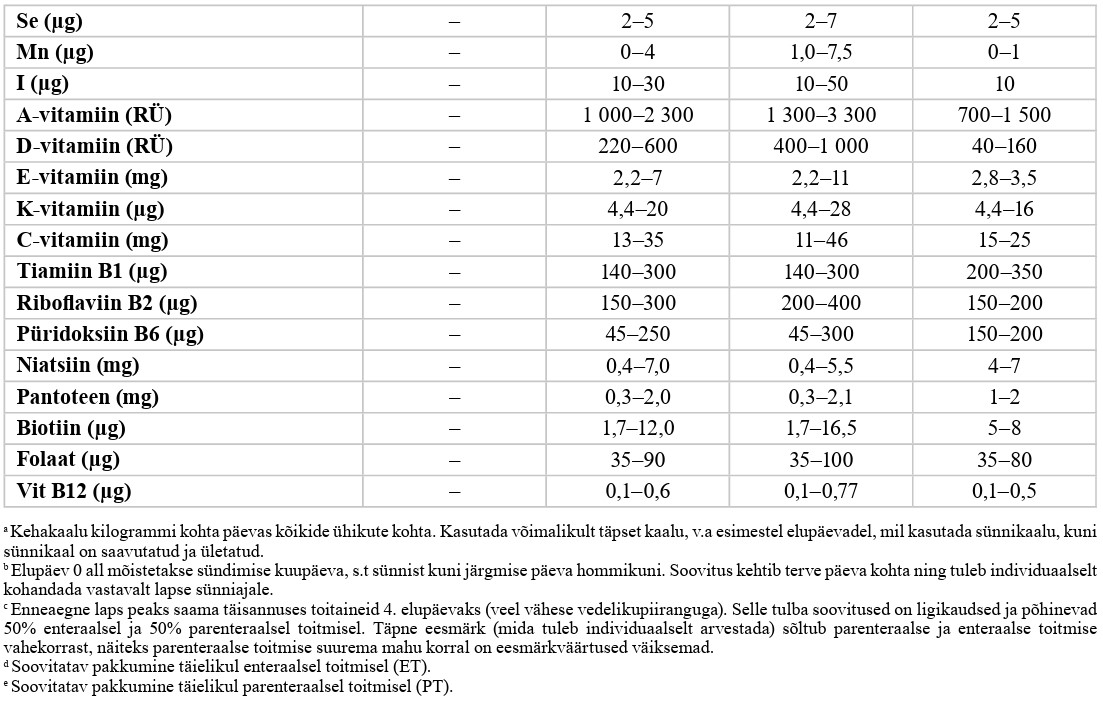
Lisa 9. Hemodünaamiliselt olulise avatud arterioosjuha farmakoloogiline ravi
Ibuprofeen veenisisesi või suukaudselt. Kui laps on täielikult enteraalsel toidul tuleks eelistada suukaudset manustamist
1. annus 10 mg/kg
2. annus 5 mg/kg 24 h peale 1. annust
3. annus 5 mg/kg 24 h peale 2. annust
Kordusravi või esmavalikuna raviarsti otsusel
1. annus 15 mg/kg
2. annus 7,5 mg/kg 24 h peale 1. annust
3. annus 7,5 mg/kg 24 h peale 2. annust
Teisene valik (rescue treatment):
Paratsetamool 15 mg x 4 suukaudselt või 7,5 mg–15 mg/kg x 4 veenisisesi 3–7 päeva
Lisa 10. Avatud arterioosjuha kliinilised sümptomid

Lisa 11. Vastsündinu varajase algusega infektsioon
Vastsündinu varajase algusega infektsiooni riskitegurid
| Parenteraalne antibiootikumravi emal kinnitatud invasiivse bakteriaalse infektsiooni või selle kahtluse korral (septitseemia) sünnituse ajal või 24 tundi enne ja pärast sünnitust (ei kehti sünnitusaegse antibiootikumprofülaktika kohta)* |
| Teisel lapsel kinnitatud infektsioon või selle kahtlus mitmikraseduse korral* |
| Invasiivne GBS-infektsioon eelmisel lapsel |
| Ema GBS-kolonisatsioon, GBS-i bakteriuuria või infektsioon käesoleva raseduse käigus |
| Lootevee puhkemine enne sünnitustegevust |
| Spontaanse sünnitustegevuse järel enneaegne sünnitus (enne 37. GN-i) |
| Lootevee kinnitatud puhkemine või kahtlus selle suhtes enam kui 18 tunni eest enneaegse sünnituse korral |
| Sünnitusaegne palavik üle 38 ºC või kinnitatud koorionamnioniit või kahtlus selle suhtes |
Kliinilised sümptomid vastsündinu võimaliku varajase infektsiooni korral
| Hingamishäired algusega 4 tundi pärast sündi* |
| Krambisündroom* |
| Invasiivse hingamistoetuse vajadus ajalisel lapsel* |
| Šoki sümptomaatika* |
| Muutunud lihastoonus |
| Muutunud käitumine või reageerimisvõime |
| Toitmisraskused |
| Toidutalumatus (k.a oksendamine, suured maojäägid ja kõhupuhitus) |
| Südamelöögisageduse muutused – bradükardia, tahhükardia |
| Hüpoksiale viitavad tunnused (nt tsentraalne tsüanoos või madalam hapniku saturatsioon) |
| Kollasuse ilmnemine esimese 24 tunni jooksul pärast sündi |
| Apnoe |
| Neonataalse entsefalopaatia tunnused |
| Kardiopulmonaalse elustamise vajadus |
| Invasiivse hingamistoetuse vajadus enneaegsel vastsündinul |
| Persisteeruv lootevereringe (persisteeruv pulmonaalne hüpertensioon) |
| Termolabiilsus (kehatemperatuur alla 36 ºC või üle 38 ºC ja see ei tulene keskkonnatingimustest) |
| Ebaselge põhjusega suur verejooks, trombotsütopeenia või ebanormaalne koagulatsioon |
| Oliguuria üle 24 tunni pärast sündi |
| Glükoosi häirunud metabolism (hüpoglükeemia, hüperglükeemia) |
| Metaboolne atsidoos BE (ingl base excess) –10 mmol/l või rohkem |
| Lokaalsed infektsioonikolded (nt nahk või silmad) |
Lisa 12. Empiirilise antibakteriaalse ravi annused (NEOFAX®)
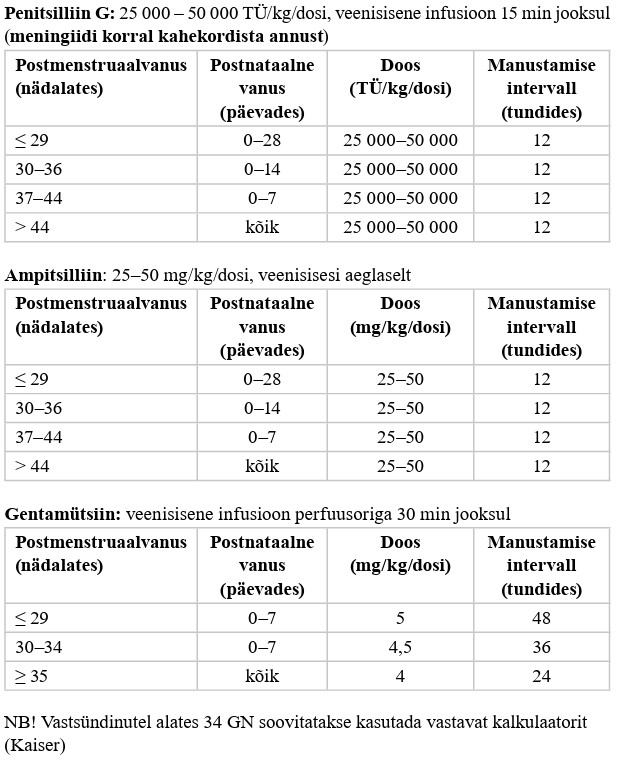
Lisa 13. Enneaegsete vastsündinute farmakoloogiline valuravi
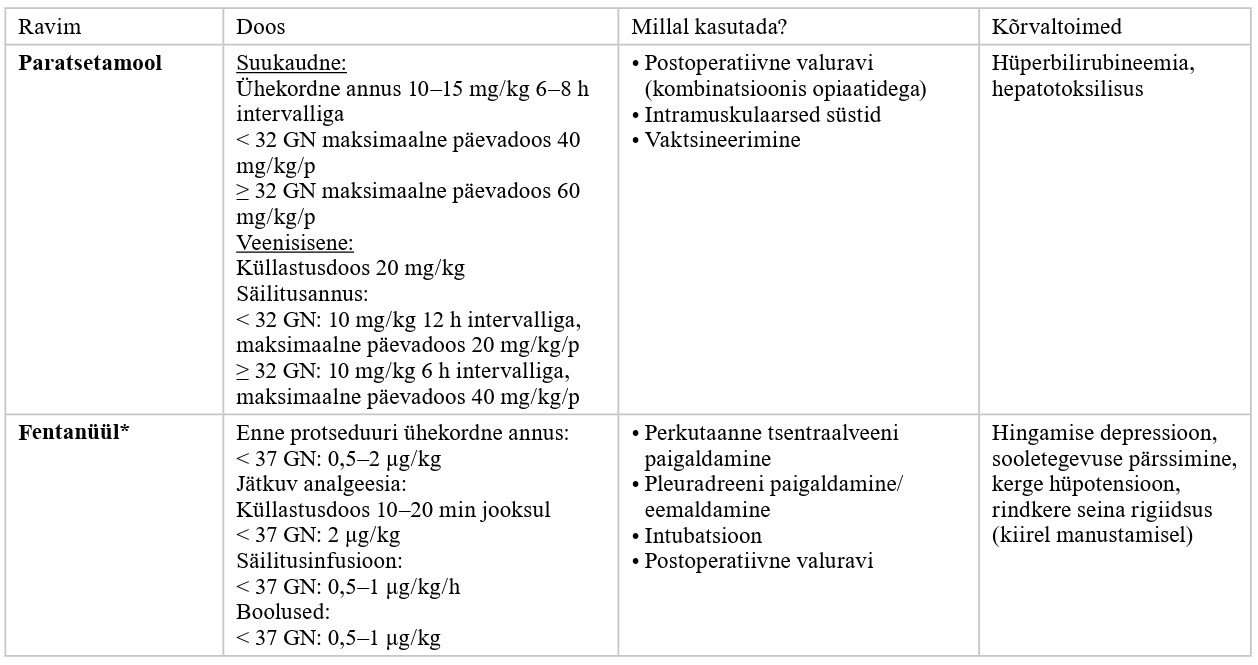

Lisa 14. Aju piltdiagnostika skriiningu ajastamine
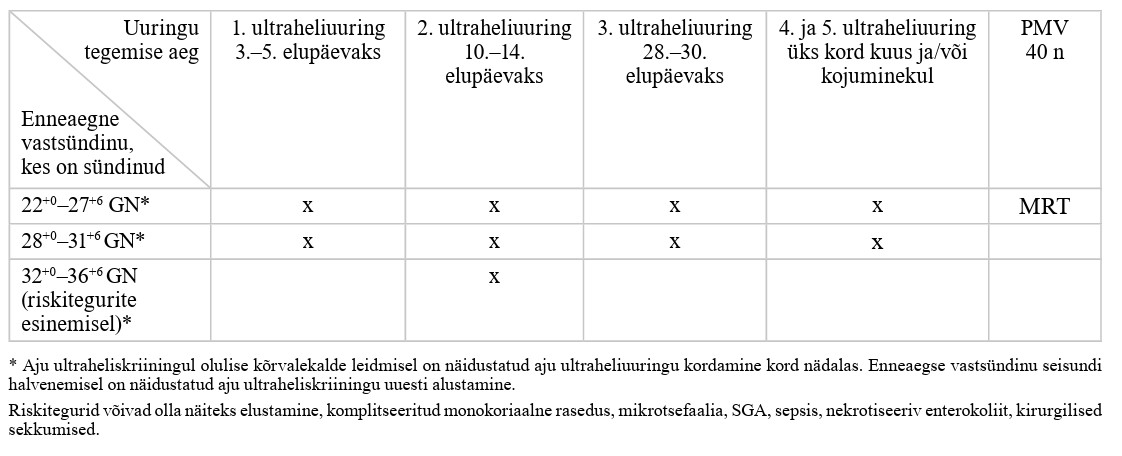
Lisa 15. Soovitused perekeskse arengulise ravi põhimõtete kasutamiseks vastsündinute raviga tegelevas osakonnas


Lisa 16. Nahakontakti alustamine enneaegsetel vastsündinutel

Lisa 17. Enneaegne sünnitus või PPROM
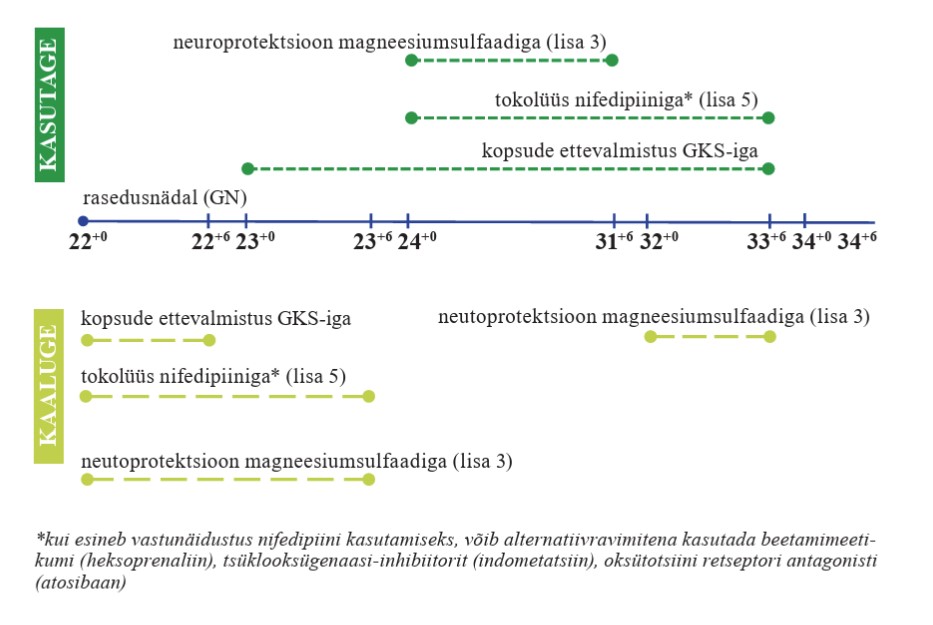
Lisa 18. Tegutsemine PPROM-i kahtluse korral
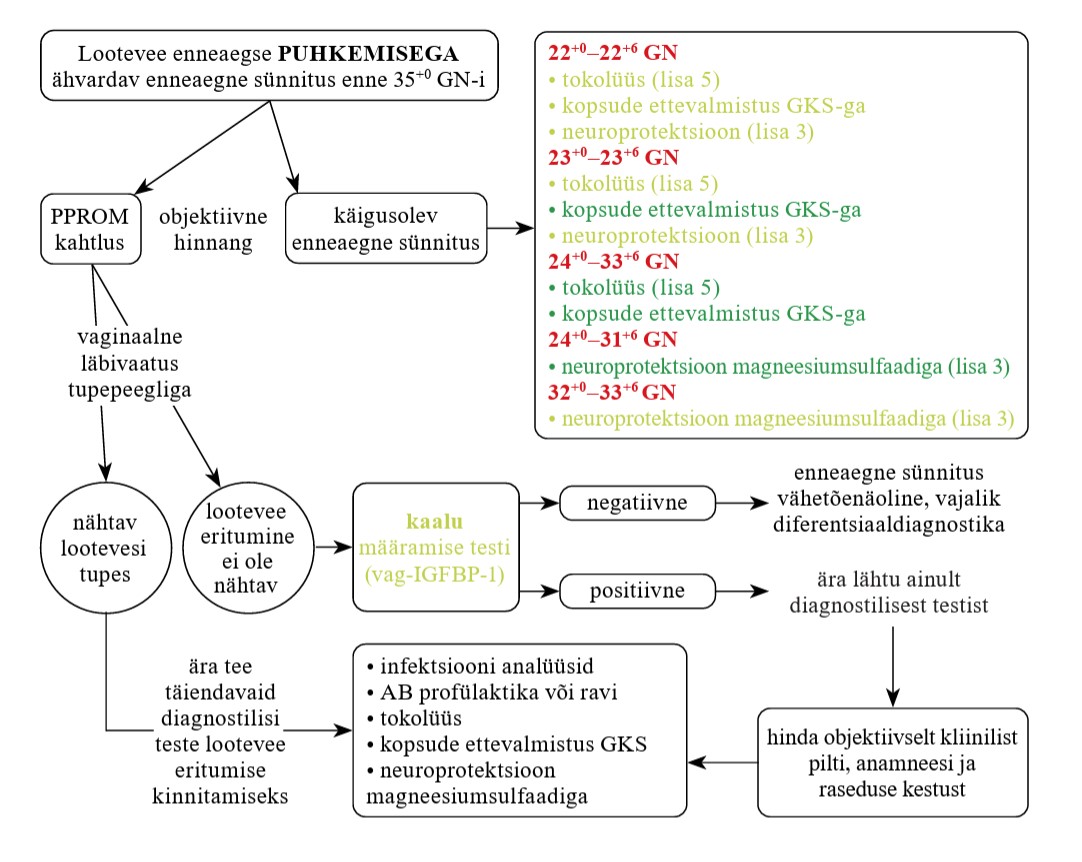
Lisa 19. Tegutsemine ähvardava enneaegse sünnituse kahtlusel
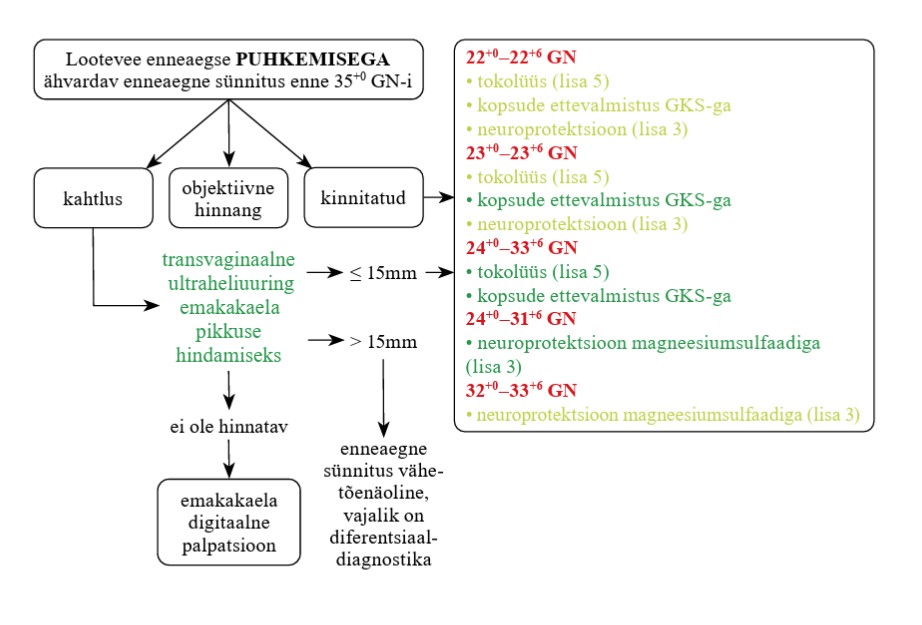
Kasutatud kirjandus
2.Eesti Haigekassa. Kliinilise auditi „Enneaegse sünnituse ja enneaegse vastsündinu perinataalperioodi käsitlus“ aruanne. Eesti Haigekassa; 2019. https://tervisekassa.ee/partnerile/tervishoiuteenuste-kvaliteet/kliinilised- auditid#tab-auditid-2019
3.Toome L, Ringmets I, Andresson P, et al. Changes in care and short-term outcome for very preterm infants in Estonia. Acta Paediatr 2012;101:390– 396.
4.Zeitlin J, Manktelow BN, Piedvache A, et al. Use of evidence based practices to improve survival without severe morbidity for very preterm infants: results from the EPICE population based cohort. BMJ 2016;354:i2976.
5.Tervise Arengu Instituut. Raseduse infosüsteem. https://www.tai.ee/et/ statistika-ja-registrid/raseduse-infosusteem.
6.Toome L, Varendi H, Männamaa M, et al. Follow-up study of 2-year-olds born at very low gestational age in Estonia. Acta Paediatr. 2013;102:300–307.
7.Draper ES, Zeitlin J, Manktelow BN, et al. EPICE group. EPICE cohort: two-year neurodevelopmental outcomes after very preterm birth. Arch Dis Child Fetal Neonatal Ed 2020;105:350–356.
8.Toome L, Varendi H, Joost U, et al. Väga enneaegsete vastsündinute ravitulemused ja ravikulud Eestis. Tartu: Tartu Ülikooli tervishoiu instituut; 2015.
9.National Collaborating Centre for Women’s and Children’s Health (UK). Preterm Labour and Birth. London: National Institute for Health and Care Excellence (UK); 2015. http://www.ncbi.nlm.nih.gov/books/NBK327571/
10.National Institute for Health and Care Excellence (NICE). Preterm Labour and Birth [Internet]. NICE Guideline, No. 25. London: National Institute for Health and Care Excellence (NICE); 2022. https://www.nice.org.uk/ guidance/ng25
11.Queensland Clinical Guidelines. Preterm labour and birth. Guideline No. MN20.6-V10-R25. Queensland Health (Australia); 2020. https://www.health. qld.gov.au/__data/assets/pdf_file/0019/140149/g-ptl.pdf
12.Berghella V, Saccone G, et al. Fetal fibronectin testing for prevention of preterm birth in singleton pregnancies with threatened preterm labor: a systematic review and meta-analysis of randomized controlled trials. Am J Obstet Gynecol. 2016;215:431–438.
13.Melchor JC, Khalil A, Wing D, et al. Prediction of preterm delivery in symptomatic women using PAMG-1, fetal fibronectin and phIGFBP-1 tests: systematic review and meta-analysis. Ultrasound Obstet Gynecol. 2018;52:442–451.
14.Toome L, Metsvaht T, Einberg Ü, et al. Tõenduspõhine lähenemine neonataalabi korraldusele Eestis. Eesti Arst. 2022;101:618–625.
15.Lasswell SM, Barfield WD, Rochat RW, et al. Perinatal regionalization for very low-birth-weight and very preterm infants: a meta-analysis. JAMA. 2010;304:992–1000.
16.Walther F, Küster DB, Bieber A, et al. Impact of regionalisation and case- volume on neonatal and perinatal mortality: an umbrella review. BMJ Open. 2020;10:e037135.
17.Jensen EA, Lorch SA, Srinivas SK, et al. Effects of a birth hospital’s neonatal intensive care unit level and annual volume of very low-birth-weight infant deliveries on morbidity and mortality. JAMA Pediatr. 2015;169:e151906.
18.Phibbs CS, Baker LC, Caughey AB, et al. Level and volume of neonatal intensive care and mortality in very-low-birth-weight infants. N Engl J Med. 2007;356:2165–2175.
19.Marlow N, Morris T, Brocklehurst P, et al. Perinatal outcomes for extremely preterm babies in relation to place of birth in England: the EPICure 2 study. Arch Dis Child Fetal Neonatal Ed. 2014;99:F181–F188.
20.Younge N, Goldsmith JP, Patel RM, et al. Survival and neurodevelopmental outcomes among periviable infants. N Engl J Med. 2017;376:617–628.
21.Rautava L, Häkkinen U, Korvenranta E, et al. for PERFECT Preterm Infant Study Group. Health and the use of health care services in 5-year-old very- low-birth-weight infants. Acta Paediatr. 2010;99:1073–9.
22.Rautava L, Andersson S, Gissler M, et al. Development and behaviour of 5-year-old very low birthweight infants. Eur Child Adolesc Psychiatry. 2010;19:669–77
23.Watson, SI et al on behalf of the Neonatal Data Analysis Unit and the NESCOP Group. The effects of designation and volume of neonatal care on mortality and morbidity outcomes of very preterm infants in England: retrospective population-based cohort study. BMJ Open. 2014;4:e004856
24.Locatelli A, Consonni S, Ghidini A. Preterm labor: approach to decreasing complications of prematurity. Obstet Gynecol Clin North Am. 2015;42:255– 74.
25.Lee BH, Stoll BJ, McDonald SA, et al. Neurodevelopmental outcomes of extremely low birth weight infants exposed prenatally to dexamethasone versus betamethasone. Pediatrics. 2008;121(2):289–296.
26.Shlossman PA, Manley JS, Sciscione AC, et al. An analysis of neonatal morbidity and mortality in maternal (in utero) and neonatal transports at 24–34 weeks’ gestation. Am J Perinatol. 1997;14(8):449–456.
27.Chung JH, Phibbs CS, Boscardin WJ, et al. Examining the effect of hospital- level factors on mortality of very low birth weight infants using multilevel modeling. J Perinatol Off J Calif Perinat Assoc. 2011;31:770–5.
28.Chien LY, Whyte R, Aziz K, et al. Improved outcome of preterm infants when delivered in tertiary care centers. Obstet Gynecol. 2001;98:247–52.
29.Towers CV, Bonebrake R, Padilla G, Rumney P. The effect of transport on the rate of severe intraventricular hemorrhage in very low birth weight infants. Obstet Gynecol. 2000;95:291–5.
30.Lorch SA, Baiocchi M, Ahlberg CE, Small DS. The differential impact of delivery hospital on the outcomes of premature infants. Pediatrics. 2012;130:270–8.
31.Lapcharoensap W, Gage SC, Kan P, et al. Hospital variation and risk factors for bronchopulmonary dysplasia in a population-based cohort. JAMA Pediatr. 2015;169:e143676.
32.Rautava L, Eskelinen J, Häkkinen U, Lehtonen L, PERFECT Preterm Infant Study Group. 5-year morbidity among very preterm infants in relation to level of hospital care. JAMA Pediatr. 2013;167:40–6.
33.Cantwell R, Clutton-Brock T, Cooper G, et al. Saving Mothers’ Lives: Reviewing maternal deaths to make motherhood safer: 2006–2008. The Eighth Report of the Confidential Enquiries into Maternal Deaths in the United Kingdom. BJOG Int J Obstet Gynaecol. 2011;118:1–203.
34.Shah KP, deRegnier RO, Grobman WA, Bennett AC. Neonatal Mortality After Interhospital Transfer of Pregnant Women for Imminent Very Preterm Birth in Illinois. JAMA Pediatr. 2020;174:358-365.
35.Edwards K, Impey L. Extreme preterm birth in the right place: a quality improvement project. Arch Dis Child Fetal Neonatal Ed. 2020;105:445–448.
36.Hirata K, Kimura T, Hirano S, et al; Neonatal Research Network of Japan. Outcomes of outborn very-low-birth-weight infants in Japan. Arch Dis Child Fetal Neonatal Ed. 2021;106:131–136.
37.Sasaki Y, Ishikawa K, Yokoi A, et al. Short- and Long-Term Outcomes of Extremely Preterm Infants in Japan According to Outborn/Inborn Birth Status. Pediatr Crit Care Med. 2019;20:963–969.
38.Longhini F, Jourdain G, Ammar F, et al. Outcomes of preterm neonates transferred between tertiary perinatal centers. Pediatr Crit Care Med. 2015;16:733–738.
39.Sweet DG, Carnielli VP, Greisen G, et al. European Consensus Guidelines on the management of respiratory distress syndrome: 2022 update. Neonatology. 2023;120:3–23. doi: 10.1159/000528914.
40.Mohamed MA, Aly H, El-Metwally D, et al. Transport of premature infants is associated with increased risk for intraventricular haemorrhage. Arch Dis Child Fetal Neonatal Ed. 2010;95:F403–F407.
41.Kaneko M, Yamashita R, Kai K, et al. Perinatal morbidity and mortality for extremely low-birthweight infants: a population-based study of regionalized maternal and neonatal transport. J Obstet Gynaecol Res. 2015;41:1056–1066.
42.Maheshwari R, Luig M, Patel V, et al. Review of respiratory management of extremely premature neonates during transport. Air Med J. 2014;33:286–291.
43.Arora P, Bajaj M, Natarajan G, et al. Impact of interhospital transport on the physiologic status of very low-birth-weight infants. Am J Perinatol. 2014;31:237–244.
44.Goldsmit G, Rabasa C, Rodríguez S, et al. Risk factors associated to clinical deterioration during the transport of sick newborn infants. Arch Argent Pediatr. 2012;110:304–309.
45.Araújo BF, Zatti H, Oliveira Filho PF, et al. Effect of place of birth and transport on morbidity and mortality of preterm newborns. J Pediatr (Rio J). 2011;87:257–262.
46.Shipley L, Gyorkos T, Dorling J, et al. Risk of severe intraventricular hemorrhage in the first week of life in preterm infants transported before 72 hours of age. Pediatr Crit Care Med. 2019;20:638–644.
47.Helenius K, Mäkikallio K, Valpas A, et al. Means of reaching successful antenatal transfers to level 3 hospitals in cases of threatened very preterm deliveries: a national survey. J Matern Fetal Neonatal Med. 2022;35:6779– 6781.
48.Arad I, Baras M, Bar-Oz B, et al. Neonatal transport of very low birth weight infants in Jerusalem, revisited. Isr Med Assoc J. 2006;8:477–482.
49.Queensland Clinical Guidelines. Perinatal care of the extremely preterm baby. Guideline No. MN20.32-V2-R25. Queensland Health. 2020. https:// www.health.qld.gov.au/qcg/documents/g-viability.pdf.
50.The Swedish National Board of Health and Welfare. Care of Extremely Premature Infants. A guideline for the care of children born before 28 full weeks of pregnancy have passed. The Swedish National Board of Health and Welfare; 2014. http://www.neonatologi.lv/wp-content/uploads/2010/01/ Care-of-extremely-premature-infants-Part-I.doc.
51.Berger TM, Bernet V, El Alama S, et al. Perinatal care at the limit of viability between 22 and 26 completed weeks of gestation in Switzerland. 2011 revision of the Swiss recommendations. Swiss Med Wkly. 2011;141:w13280.
52.Fellman V, Hellström-Westas L, Norman M, et al. One-year survival of extremely preterm infants after active perinatal care in Sweden. JAMA. 2009;301:2225–2233.
53.Antenatal Corticosteroids to Reduce Neonatal Morbidity and Mortality. Green–top Guideline No. 7. Royal College of Obstetricians and Gynaecologists.; 2010. https://www.rcog.org.uk/guidance/browse-all- guidance/green-top-guidelines/antenatal-corticosteroids-to-reduce-neonatal- morbidity-green-top-guideline-no-7/
54.Roberts D, Dalziel S, Smith A, et al. Antenatal corticosteroids for accelerating fetal lung maturation for women at risk of preterm birth. Cochrane Database Syst Rev. 2006:CD004454.
55.Onland W, de Laat MW, Mol BW, et al. Effects of antenatal corticosteroids given prior to 26 weeks’ gestation: a systematic review of randomized controlled trials. Am J Perinatol. 2011;28:33–44.
56.Carlo WA, McDonald SA, Fanaroff AA, et al. Association of antenatal corticosteroids with mortality and neurodevelopmental outcomes among infants born at 22 to 25 weeks’ gestation. JAMA. 2011;306:2348–2358.
57.Mori R, Kusuda S, Fujimura M, et al. Antenatal corticosteroids promote survival of extremely preterm infants born at 22 to 23 weeks of gestation. J Pediatr. 2011;159:110–114.e1.
58.Perinatal Management of Pregnant Women at the Threshold of Infant Viability – the Obstetric Perspective (Scientific Impact Paper No. 41). Royal College of Obstetricians and Gynaecologists. 2014. https://www.rcog.org. uk/en/guidelines-research-services/guidelines/sip41/.
59.Lannon SMR, Guthrie KA, Vanderhoeven JP, et al. Uterine rupture risk after periviable cesarean delivery. Obstet Gynecol. 2015;125:1095–1100.
60.Brownfoot FC, Gagliardi DI, Bain E, et al. Different corticosteroids and regimens for accelerating fetal lung maturation for women at risk of preterm birth. Cochrane Database Syst Rev. 2013;8:CD006764.
61.Norman M, Piedvache A, Børch K, et al. Association of short antenatal corticosteroid administration-to-birth intervals with survival and morbidity among very preterm infants: results from the EPICE cohort. JAMA Pediatr. 2017;171:678–686.
62.Morrison JL, Botting KJ, Soo PS, et al. Antenatal steroids and the IUGR fetus: are exposure and physiological effects on the lung and cardiovascular system the same as in normally grown fetuses? J Pregnancy. 2012;2012:839656.
63.Bonanno C, Wapner RJ, Davis JM, et al. Antenatal corticosteroids in the management of preterm birth: are we back where we started? Obstet Gynecol Clin North Am. 2012;39:47–63.
64.Amiya RM, Mlunde LB, Ota E, et al. Antenatal corticosteroids for reducing adverse maternal and child outcomes in special populations of women at risk of imminent preterm birth: a systematic review and meta-analysis. PLoS One. 2016;11:e0147604.
65.Crowther CA, McKinlay CJ, Middleton P, et al. Repeat doses of prenatal corticosteroids for women at risk of preterm birth for improving neonatal health outcomes. Cochrane Database Syst Rev. 2011:CD003935.
66.Bevilacqua E, Brunelli R, Anceschi MM, et al. Review and meta-analysis: benefits and risks of multiple courses of antenatal corticosteroids. J Matern Fetal Neonatal Med. 2010;23:244–260.
67.Peltoniemi OM, Kari MA, Hallman M, et al. Repeated antenatal corticosteroid treatment: a systematic review and meta-analysis. Acta Obstet Gynecol Scand. 2011;90:719–727.
68.Garite TJ, Kurtzman J, Maurel K, et al. Impact of a “rescue course” of antenatal corticosteroids: a multicenter randomized placebo-controlled trial. Am J Obstet Gynecol. 2009;200:248.e1–248.e9.
69.McEvoy C, Schilling D, Peters D, et al. Respiratory Compliance in Preterm Infants after a Single Rescue Course of Antenatal Steroids: A Randomized Controlled Trial. Am J Obstet Gynecol. 2010;202:544.e1-544.e9.
70.Cartwright RD, Crowther CA, Anderson PJ, et al. Association of fetal growth restriction with neurocognitive function after repeated antenatal betamethasone treatment vs placebo: secondary analysis of the ACTORDS randomized clinical trial. JAMA Netw Open. 2019;2:e187636.
71.Yum SK, Lee JH, Kim JY, et al. Dose completion of antenatal corticosteroids and neonatal outcomes in non-small-for-gestational age or small-for- gestational age very-low-birthweight infants: a Korean population-based cohort study. Pediatr Neonatol. 2022;63:165–171.
72.Ninan K, Liyanage SK, Murphy KE, et al. Evaluation of long-term outcomes associated with preterm exposure to antenatal corticosteroids: a systematic review and meta-analysis. JAMA Pediatr. 2022;176:e220483.
73.Deshmukh M, Patole S, Kulkarni A, et al. Antenatal corticosteroids for impending late preterm (34–36+6 weeks) deliveries: a systematic review and meta-analysis of RCTs. PLoS One. 2021;16:e0248774.
74.Melamed N, Asztalos E, Murphy K, et al. Neurodevelopmental disorders among term infants exposed to antenatal corticosteroids during pregnancy: a population-based study. BMJ Open. 2019;9:e031197.
75.Räikkönen K, Gissler M, Kajantie E, et al. Associations between maternal antenatal corticosteroid treatment and mental and behavioral disorders in children. JAMA. 2020;323:1924–1933.
76.Räikkönen K, Gissler M, Tapiainen T, et al. Associations between maternal antenatal corticosteroid treatment and psychological developmental and neurosensory disorders in children. JAMA Netw Open. 2022;5:e2228518.
77.Blankenship SA, Brown KE, Simon LE, et al. Antenatal corticosteroids in preterm small-for-gestational age infants: a systematic review and meta- analysis. Am J Obstet Gynecol MFM. 2020;2:100215.
78.Battarbee AN, Sandoval G, Grobman WA, et al. Antenatal corticosteroids and preterm neonatal morbidity and mortality among women with and without diabetes in pregnancy. Am J Perinatol. 2022;39:67–74.
79.Drummond PM, Colver AF, Smith JP, et al. Analysis by gestational age of cerebral palsy in singleton births in north-east England 1970–94. Paediatr Perinat Epidemiol. 2002;16:172–180.
80.Doyle LW, Crowther CA, Middleton P, et al. Magnesium sulphate for women at risk of preterm birth for neuroprotection of the fetus. Cochrane Database Syst Rev. 2009;(1):CD004661.
81.Conde-Agudelo A, Romero R, Smith J, et al. Antenatal magnesium sulfate for the prevention of cerebral palsy in preterm infants less than 34 weeks’ gestation: a systematic review and meta-analysis. Am J Obstet Gynecol. 2009;200:595–609.
82.Costantine MM, Weiner SJ, Johnson DL, et al. Effects of antenatal exposure to magnesium sulfate on neuroprotection and mortality in preterm infants: a meta-analysis. Obstet Gynecol. 2009;114:354–364.
83.Bickford CD, Magee LA, Mitton C, et al. Magnesium sulphate for fetal neuroprotection: a cost-effectiveness analysis. BMC Health Serv Res. 2013;13:527.
84.Royal College of Obstetricians and Gynaecologists. Magnesium sulphate to prevent cerebral palsy following preterm birth (Scientific Impact Paper No. 29). RCOG. https://www.rcog.org.uk/en/guidelines-research-services/ guidelines/sip29/
85.Bain ES, Middleton PF, Yelland LN, et al. Maternal adverse effects with different loading infusion rates of antenatal magnesium sulphate for preterm fetal neuroprotection: the IRIS randomised trial. BJOG. 2014;121:595–603.
86.Magee L, Sawchuck D, Synnes A, et al. SOGC Clinical Practice Guideline: magnesium sulphate for fetal neuroprotection. J Obstet Gynaecol Can. 2011;33:516–529.
87.The Antenatal Magnesium Sulphate for Neuroprotection Guideline Development Panel. Antenatal magnesium sulphate prior to preterm birth for neuroprotection of the fetus, infant and child: national clinical practice guidelines. The University of Adelaide; 2010. https://ontrack.perinatalsociety. org.nz/wp-content/uploads/2020/04/Antenatal-magnesium-sulphate-prior- to-preterm-birth-for-neuroprotection-of-the-fetus-infant-child-National- clinical-practice-guidelines.pdf
88.Medicines and Healthcare products Regulatory Agency (MHRA). Magnesium sulfate: risk of skeletal adverse effects in the neonate following prolonged or repeated use in pregnancy. Drug Safety Update. MHRA 2019;12.
89.Queensland Clinical Guidelines. Preterm Labour and Birth. 2014. https:// www.health.qld.gov.au/qcg/documents/g-ptl.pdf.
90.Anderson BL, Simhan HN, Simons KM, et al. Untreated asymptomatic group B streptococcal bacteriuria early in pregnancy and chorioamnionitis at delivery. Am J Obstet Gynecol. 2007;196:524.e1–524.e5.
91.Valkenburg-van den Berg AW, Sprij AJ, Dekker FW, et al. Association between colonization with group B Streptococcus and preterm delivery: a systematic review. Acta Obstet Gynecol Scand. 2009;88:958–967.
92.Di Renzo GC, Melin P, Berardi A, et al. Intrapartum GBS screening and antibiotic prophylaxis: a European consensus conference. J Matern Fetal Neonatal Med. 2014;1–17.
93.Tita ATN, Andrews WW, Johnson DL, et al. Diagnosis and management of clinical chorioamnionitis. Clin Perinatol. 2010;37:339–354.
94.Brocklehurst P, Gordon A, Heatley E, et al. Antibiotics for treating bacterial vaginosis in pregnancy. Cochrane Database Syst Rev. 2013;1:CD000262.
95.Leitich H, Kiss H, Maier R, et al. Asymptomatic bacterial vaginosis and intermediate flora as risk factors for adverse pregnancy outcome. Best Pract Res Clin Obstet Gynaecol. 2007;21:375–390.
96.Eesti Naistearstide Selts. Raseduse jälgimise juhend. 2018. http:// rasedajalgimine.weebly.com/
97.Kenyon S, Boulvain M, Neilson JP, et al. Antibiotics for preterm rupture of membranes. Cochrane Database Syst Rev. 2010;(8):CD001058.
98.Flenady V, Hawley G, Stock OM, et al. Prophylactic antibiotics for inhibiting preterm labour with intact membranes. Cochrane Database Syst Rev. 2013;12:CD000246.
99.Kenyon SL, Taylor DJ, Tarnow-Mordi W, et al. Broad-spectrum antibiotics for preterm, prelabour rupture of fetal membranes: the ORACLE I randomised trial. Lancet. 2001;357:979–988.
100.Kenyon SL, Taylor DJ, Tarnow-Mordi W, et al. Broad-spectrum antibiotics for spontaneous preterm labour: the ORACLE II randomised trial. Lancet. 2001;357:989–994.
101.Kenyon S, Pike K, Jones DR, et al. Childhood outcomes after prescription of antibiotics to pregnant women with preterm rupture of the membranes: 7-year follow-up of the ORACLE I trial. Lancet. 2008;372:1310–1318.
102.Kenyon S, Pike K, Jones DR, et al. Childhood outcomes after prescription of antibiotics to pregnant women with spontaneous preterm labour: 7-year follow-up of the ORACLE II trial. Lancet. 2008;372:1319–1327.
103.Preterm Labour, Antibiotics and Cerebral Palsy (Scientific Impact Paper No. 33). Royal College of Obstetricians and Gynaecologists. https://www. rcog.org.uk/en/guidelines-research-services/guidelines/sip33/
104.Preterm Prelabour Rupture of Membranes (Green-top Guideline No. 44). Royal College of Obstetricians and Gynaecologists. https://www.rcog.org. uk/en/guidelines-research-services/guidelines/gtg44/.
105.Been JV, Lievense S, Zimmermann LJI, et al. Chorioamnionitis as a risk factor for necrotizing enterocolitis: a systematic review and meta-analysis. J Pediatr. 2013;162:236–242.e2.
106.Wu YW, Colford JM, Smith A, et al. Chorioamnionitis as a risk factor for cerebral palsy: a meta-analysis. JAMA. 2000;284:1417–1424.
107.Chapman E, Reveiz L, Illanes E, et al. Antibiotic regimens for management of intra-amniotic infection. Cochrane Database Syst Rev. 2014;12:CD010976.
108.Ohlsson A, Shah VS, Johnson DL, et al. Intrapartum antibiotics for known maternal group B streptococcal colonization. Cochrane Database Syst Rev. 2014;6:CD007467.
109.Group B Streptococcal Disease, Early-onset (Green-top Guideline No. 36). Royal College of Obstetricians & Gynaecologists. https://www.rcog.org.uk/ en/guidelines-research-services/guidelines/gtg36/.
110.Lin LL, Hung JN, Shiu SI, et al. Efficacy of prophylactic antibiotics for preterm premature rupture of membranes: a systematic review and network meta-analysis. Am J Obstet Gynecol MFM. 2023;5:100978.
111.Chatzakis C, Papatheodorou S, Sarafidis K, et al. Effect on perinatal outcome of prophylactic antibiotics in preterm prelabor rupture of membranes: network meta-analysis of randomized controlled trials. Ultrasound Obstet Gynecol. 2020;55:20–31.
112.Thomson AJ, Roberts D, Johnson DL, et al. Care of women presenting with suspected preterm prelabour rupture of membranes from 24+0 weeks of gestation. BJOG. 2019;126:e152–e166.
113.American College of Obstetricians and Gynecologists, Society for Maternal- Fetal Medicine. ACOG Practice Bulletin No. 144: multifetal gestations: twin, triplet, and higher-order multifetal pregnancies. Obstet Gynecol. 2014;123:1118–1132.
114.Alfirevic Z, Milan SJ, Livio S, et al. Caesarean section versus vaginal delivery for preterm birth in singletons. Cochrane Database Syst Rev. 2012;6:CD000078.
115.Källén K, Serenius F, Westgren M, et al. Impact of obstetric factors on outcome of extremely preterm births in Sweden: prospective population- based observational study (EXPRESS). Acta Obstet Gynecol Scand. 2015;94:1203–1214.
116.Reddy UM, Zhang J, Sun L, et al. Neonatal mortality by attempted route of delivery in early preterm birth. Am J Obstet Gynecol. 2012;207:117.e1–117. e8.
117.Werner EF, Savitz DA, Janevic TM, et al. Mode of delivery and neonatal outcomes in preterm, small-for-gestational-age newborns. Obstet Gynecol. 2012 ;120:560–4.
118.Käypä hoito. Ennenaikainen synnytys. Käypä hoito -suositus. Suomalainen Lääkäriseura Duodecim; 2018.
119.Barzilay E, Gadot Y, Koren G, et al. Safety of vaginal delivery in very low birthweight vertex singletons: a meta-analysis. J Matern Fetal Neonatal Med. 2016.
120.Jarde A, Feng YY, Viaje KA, et al. Vaginal birth vs caesarean section for extremely preterm vertex infants: a systematic review and meta-analyses. Arch Gynecol Obstet. 2019.
121.Royal College of Obstetricians and Gynaecologists. Management of breech presentation. Green-top Guideline No. 20. London: RCOG; 2017.
122.O’Reilly C, Hehir MP, Mahony R, et al. Influence of mode of delivery on outcomes in preterm breech infants presenting in labor. J Matern Fetal Neonatal Med. 2018.
123.Niles KM, Barrett JFR, Ladhani NNN, et al. Comparison of cesarean versus vaginal delivery of extremely preterm gestations in breech presentation: retrospective cohort study. J Matern Fetal Neonatal Med. 2019.
124.Toijonen A, Heinonen S, Gissler M, et al. Neonatal outcome in vaginal breech labor at 32+0 to 36+0 weeks of gestation: a nationwide, population- based record linkage study. BMC Pregnancy Childbirth. 2022.
125.Schmidt S, Norman M, Misselwitz B, et al. Mode of delivery and mortality and morbidity for very preterm singleton infants in a breech position: a European cohort study. Eur J Obstet Gynecol Reprod Biol. 2021.
126.Lorthe E, Sentilhes L, Quere M, et al. Planned delivery route of preterm breech singletons, and neonatal and 2-year outcomes: a population-based cohort study. BJOG. 2019;126:91–99.
127.Bergenhenegouwen L, Vlemmix F, Ensing S, et al. Preterm breech presentation: a comparison of intended vaginal and intended cesarean delivery. Obstet Gynecol. 2015;126:1223–1230.
128.Blanc J, Rességuier N, Loundou A, et al. Severe maternal morbidity in preterm cesarean delivery: a systematic review and meta-analysis. Eur J Obstet Gynecol Reprod Biol. 2021;261:116–123.
129.Thanh BYL, Lumbiganon P, Pattanittum P, et al. Mode of delivery and pregnancy outcomes in preterm birth: a secondary analysis of the WHO Global and Multi-country Surveys. Sci Rep. 2019;9:15556.
130.Toijonen A, Hinnenberg P, Gissler M, et al. Maternal and neonatal outcomes in the following delivery after previous preterm caesarean breech birth: a national cohort study. J Obstet Gynaecol. 2022;42:49–54.
131.Barrett J, et al. The SOGC consensus statement: management of twin pregnancies. 2000. https://www.jogc.com/article/S0849-5831(16)30135-5/pdf
132.Hogle KL, Hutton EK, McBrien KA, et al. Cesarean delivery for twins: a systematic review and meta-analysis. Am J Obstet Gynecol. 2003;188:220– 227.
133.Mol BW, Bergenhenegouwen L, Ensing S, et al. The impact of mode of delivery on the outcome in very preterm twins. J Matern Fetal Neonatal Med. 2020;33:2089–2095.
134.Hunter T, Shah J, Synnes A, et al. Neonatal outcomes of preterm twins according to mode of birth and presentation. J Matern Fetal Neonatal Med. 2018;31:682–688.
135.Hiersch L, Shah PS, Khurshid F, et al. Mode of delivery and neonatal outcomes in extremely preterm vertex/nonvertex twins. Am J Obstet Gynecol. 2021;224:613.e1–613.e10.
136.Dagenais C, Lewis-Mikhael AM, Grabovac M, et al. What is the safest mode of delivery for extremely preterm cephalic/non-cephalic twin pairs? A systematic review and meta-analyses. BMC Pregnancy Childbirth. 2017;17:397
137.Lappen JR, Hackney DN, Bailit JL. Maternal and neonatal outcomes of attempted vaginal compared with planned cesarean delivery in triplet gestations. Am J Obstet Gynecol. 2016;215:493.e1-6.
138.Lobb MO, Duthie SJ, Cooke RW. The influence of episiotomy on the neonatal survival and incidence of periventricular haemorrhage in very-low-birth- weight infants. Eur J Obstet Gynecol Reprod Biol. 1986;22:17–21.
139.The TG. Is routine episiotomy beneficial in the low birth weight delivery? Int J Gynaecol Obstet. 1990;31:135–40.
140.Carroli G, Belizan J. Episiotomy for vaginal birth. Cochrane Database Syst Rev. 2007;(4):CD000081.
141.Institute of Obstetricians and Gynaecologists, Royal College of Physicians of Ireland; Directorate of Strategy and Clinical Care, Health Service Executive. Preterm prelabour rupture of the membranes (PPROM). Guideline No. 24. 2013. https://www.hse.ie/eng/about/Who/clinical/natclinprog/ obsandgynaeprogramme/pretermrupture.pdf
142.Denzler A, Burkhardt T, Natalucci G, Zimmermann R. Latency after preterm prelabor rupture of the membranes: increased risk for periventricular leukomalacia. J Pregnancy. 2014;2014:874984.
143.Mercer BM, Crocker LG, Boe NM, Sibai BM. Induction versus expectant management in premature rupture of the membranes with mature amniotic f luid at 32 to 36 weeks: a randomized trial. Am J Obstet Gynecol. 1993;169:775–82.
144.Naef RW, Allbert JR, Ross EL, et al. Premature rupture of membranes at 34 to 37 weeks’ gestation: aggressive versus conservative management. Am J Obstet Gynecol. 1998;178:126–30.
145.Cox SM, Leveno KJ. Intentional delivery versus expectant management with preterm ruptured membranes at 30–34 weeks’ gestation. Obstet Gynecol. 1995;86:875–9.
146.Buchanan SL, Crowther CA, Levett KM, et al. Planned early birth versus expectant management for women with preterm prelabour rupture of membranes prior to 37 weeks’ gestation for improving pregnancy outcome. Cochrane Database Syst Rev. 2010;(3):CD004735.
147.Al-Mandeel H, Alhindi MY, Sauve R. Effects of intentional delivery on maternal and neonatal outcomes in pregnancies with preterm prelabour rupture of membranes between 28 and 34 weeks of gestation: a systematic review and meta-analysis. J Matern Fetal Neonatal Med. 2013;26:83–9.
148.Kayem G, Bernier-Dupreelle A, Goffinet F, et al. Active versus expectant management for preterm prelabor rupture of membranes at 34–36 weeks of completed gestation: comparison of maternal and neonatal outcomes. Acta Obstet Gynecol Scand. 2010;89:776–81.
149.van der Ham DP, Vijgen SMC, Nijhuis JG, et al. Induction of labor versus expectant management in women with preterm prelabor rupture of membranes between 34 and 37 weeks: a randomized controlled trial. PLoS Med. 2012;9:e1001208.
150.van der Ham DP, Nijhuis JG, Mol BWJ, et al. Induction of labour versus expectant management in women with preterm prelabour rupture of membranes between 34 and 37 weeks (the PPROMEXIL-trial). BMC Pregnancy Childbirth. 2007;7:11.
151.van der Ham DP, van der Heyden JL, Opmeer BC, et al. Management of late-preterm premature rupture of membranes: the PPROMEXIL-2 trial. Am J Obstet Gynecol. 2012;207:276.e1-10.
152.Tajik P, van der Ham DP, Zafarmand MH, et al. Using vaginal Group B Streptococcus colonisation in women with preterm premature rupture of membranes to guide the decision for immediate delivery: a secondary analysis of the PPROMEXIL trials. BJOG. 2014;121:1263–72.
153.Bond DM, Middleton P, Levett KM, et al. Planned early birth versus expectant management for women with preterm prelabour rupture of membranes prior to 37 weeks’ gestation for improving pregnancy outcome. Cochrane Database Syst Rev. 2017;3:CD004735.
154.Iams JD, Berghella V. Care for women with prior preterm birth. Am J Obstet Gynecol. 2010;203:89–100.
155.Royal College of Obstetricians & Gynaecologists. Preterm labour, tocolytic drugs (Green-top Guideline No. 1B). https://www.rcog.org.uk/en/guidelines- research-services/guidelines/gtg1b/
156.Naik Gaunekar N, Raman P, Bain E, et al. Maintenance therapy with calcium channel blockers for preventing preterm birth after threatened preterm labour. Cochrane Database Syst Rev. 2013;10:CD004071.
157.Papatsonis D, Flenady V, Liley H, et al. Maintenance therapy with oxytocin antagonists for inhibiting preterm birth after threatened preterm labour. Cochrane Database Syst Rev. 2009;(1):CD005938.
158.Chawanpaiboon S, Laopaiboon M, Lumbiganon P, et al. Terbutaline pump maintenance therapy after threatened preterm labour for reducing adverse neonatal outcomes. Cochrane Database Syst Rev. 2014;3:CD010800.
159.Haas DM, Caldwell DM, Kirkpatrick P, et al. Tocolytic therapy for preterm delivery: systematic review and network meta-analysis. BMJ. 2012;345:e6226.
160.Flenady V, Wojcieszek AM, Papatsonis DNM, et al. Calcium channel blockers for inhibiting preterm labour and birth. Cochrane Database Syst Rev. 2014;6:CD002255.
161.Conde-Agudelo A, Romero R, Kusanovic JP, et al. Nifedipine in the management of preterm labor: a systematic review and metaanalysis. Am J Obstet Gynecol. 2011;204:134.e1-20.
162.Flenady V, Reinebrant HE, Liley HG, et al. Oxytocin receptor antagonists for inhibiting preterm labour. Cochrane Database Syst Rev. 2014;6:CD004452.
163.Reinebrant HE, Pileggi-Castro C, Romero CLT, et al. Cyclo-oxygenase (COX) inhibitors for treating preterm labour. Cochrane Database Syst Rev. 2015;6:CD001992.
164.Vogel JP, Nardin JM, Dowswell T, et al. Combination of tocolytic agents for inhibiting preterm labour. Cochrane Database Syst Rev. 2014;7:CD006169.
165.Wilson A, Hodgetts-Morton VA, Marson EJ, et al. Tocolytics for delaying preterm birth: a network meta-analysis. Cochrane Database Syst Rev. 2022;8:CD014978.
166.van Winden TMS, Nijman TAJ, Kleinrouweler CE, et al. Tocolysis with nifedipine versus atosiban and perinatal outcome: an individual participant data meta-analysis. BMC Pregnancy Childbirth. 2022;22:567.
167.van Vliet EOG, Nijman TAJ, Schuit E, et al. Nifedipine versus atosiban for threatened preterm birth (APOSTEL III): a multicentre, randomised controlled trial. Lancet. 2016;387:2117–24.
168.Nijman TAJ, Goedhart MM, Naaktgeboren CN, et al. Effect of nifedipine and atosiban on perinatal brain injury: secondary analysis of the APOSTEL-III trial. Ultrasound Obstet Gynecol. 2018;51:806–12.
169.van Winden T, Klumper J, Kleinrouweler CE, et al. Effects of tocolysis with nifedipine or atosiban on child outcome: follow-up of the APOSTEL III trial. BJOG. 2020;127:1129–37.
170.Nijman T, van Baaren GJ, van Vliet E, et al. Cost effectiveness of nifedipine compared with atosiban in the treatment of threatened preterm birth (APOSTEL III trial). BJOG. 2019;126:875–83.
171.Sweet DG, Carnielli V, Greisen G, et al. European consensus guidelines on the management of neonatal respiratory distress syndrome in preterm infants—2013 update. Neonatology. 2013;103:353–68.
172.Rabe H, Diaz-Rossello JL, Duley L, et al. Effect of timing of umbilical cord clamping and other strategies to influence placental transfusion at preterm birth on maternal and infant outcomes. Cochrane Database Syst Rev. 2012;8:CD003248.
173.Mathew JL. Timing of umbilical cord clamping in term and preterm deliveries and infant and maternal outcomes: a systematic review of randomized controlled trials. Indian Pediatr. 2011;48:123–9.
174.Backes CH, Rivera BK, Haque U, et al. Placental transfusion strategies in very preterm neonates: a systematic review and meta-analysis. Obstet Gynecol. 2014;124:47–56.
175.Committee on Obstetric Practice, American College of Obstetricians and Gynecologists. Committee Opinion No.543: Timing of umbilical cord clamping after birth. Obstet Gynecol. 2012;120:1522–6.
176.Wyllie J, Bruinenberg J, Roehr CC, et al. European Resuscitation Council Guidelines for Resuscitation 2015. Resuscitation. 2015;95:249–63.
177.Royal College of Obstetricians & Gynaecologists. Clamping of the umbilical cord and placental transfusion (Scientific Impact Paper No. 14). https://www. rcog.org.uk/en/guidelines-research-services/guidelines/sip14/
178.Al-Wassia H, Shah PS. Efficacy and safety of umbilical cord milking at birth: a systematic review and meta-analysis. JAMA Pediatr. 2015;169:18–25.
179.Dang D, Zhang C, Shi S, et al. Umbilical cord milking reduces need for red cell transfusions and improves neonatal adaptation in preterm infants: meta-analysis. J Obstet Gynaecol Res. 2015;41:890–5.
180.Garofalo M, Abenhaim HA. Early versus delayed cord clamping in term and preterm births: a review. J Obstet Gynaecol Can. 2012;34:525–531.
181.Seidler AL, Libesman S, Hunter KE, et al; iCOMP Collaborators. Short, medium, and long deferral of umbilical cord clamping compared with umbilical cord milking and immediate clamping at preterm birth: a systematic review and network meta-analysis with individual participant data. Lancet. 2023;402:2223–34.
182.Rabe H, Gyte GM, Dķaz-Rossello JL, et al. Effect of timing of umbilical cord clamping and other strategies to influence placental transfusion at preterm birth on maternal and infant outcomes. Cochrane Database Syst Rev. 2019;9:CD003248.
183.Reilly MC, Vohra S, Rac VE, et al. Randomized trial of occlusive wrap for heat loss prevention in preterm infants. J Pediatr. 2015;166:262–8.
184.Miller SS, Lee HC, Gould JB, et al. Hypothermia in very low birth weight infants: distribution, risk factors and outcomes. J Perinatol. 2011;31:S49–56.
185.Costeloe K, Hennessy E, Gibson AT, et al. The EPICure study: outcomes to discharge from hospital for infants born at the threshold of viability. Pediatrics. 2000;106:659–71.
186.Richmond S, Wyllie J. European Resuscitation Council Guidelines for Resuscitation 2010 Section 7. Resuscitation of babies at birth. Resuscitation. 2010;81:1389–99.
187.Fischer HS, Bührer C. Avoiding endotracheal ventilation to prevent bronchopulmonary dysplasia: a meta-analysis. Pediatrics. 2013;132:e1351–60.
188.Schmölzer GM, Kumar M, Pichler G, et al. Non-invasive versus invasive respiratory support in preterm infants at birth: systematic review and meta- analysis. BMJ. 2013;347:f5980.
189.Szyld E, Aguilar A, Musante GA, et al. Comparison of devices for newborn ventilation in the delivery room. J Pediatr. 2014;165:234–9.
190.Li W, Long C, Zhangxue H, et al. Nasal intermittent positive pressure ventilation versus nasal continuous positive airway pressure for preterm infants with respiratory distress syndrome: a meta-analysis and up-date. Pediatr Pulmonol. 2015;50:402–9.
191.Shi Y, Tang S, Zhao J, et al. A prospective, randomized, controlled study of NIPPV versus nCPAP in preterm and term infants with respiratory distress syndrome. Pediatr Pulmonol. 2014;49:673–8.
192.Lista G, Boni L, Scopesi F, et al. Sustained lung inflation at birth for preterm infants: a randomized clinical trial. Pediatrics. 2015;135:e457–64.
193.Schmölzer GM, Kumar M, Aziz K, et al. Sustained inflation versus positive pressure ventilation at birth: a systematic review and meta-analysis. Arch Dis Child Fetal Neonatal Ed. 2014;100:F361–8.
194.Kirpalani H, Millar D, Lemyre B, et al. A trial comparing noninvasive ventilation strategies in preterm infants. N Engl J Med. 2013;369:611–20.
195.Salvo V, Lista G, Lupo E, et al. Noninvasive ventilation strategies for early treatment of RDS in preterm infants: an RCT. Pediatrics. 2015;135:444–51.
196.National Guideline Alliance (UK). Evidence reviews for respiratory support: Specialist neonatal respiratory care for babies born preterm: Evidence review B. London: NICE; 2019.
197.Madar J, Roehr CC, Ainsworth S, et al. European Resuscitation Council Guidelines 2021: newborn resuscitation and support of transition of infants at birth. Resuscitation. 2021;161:291–326.
198.Margus K, Süvari L, Eelmäe I, et al. Vastsündinu elustamine ja esmase adaptatsiooni toetamine. Eesti Perinatoloogia Selts; 2022.
199.Solevåg AL, Cheung PY, Schmölzer GM, et al. Bi-level noninvasive ventilation in neonatal respiratory distress syndrome: a systematic review and meta-analysis. Neonatology. 2021;118:264–73.
200.Yagui AC, Meneses J, Zólio BA, et al. Nasal continuous positive airway pressure (NCPAP) or noninvasive neurally adjusted ventilatory assist (NIV- NAVA) for preterm infants with respiratory distress after birth: a randomized controlled trial. Pediatr Pulmonol. 2019;54:1704–11.
201.Li J, Chen L, Shi Y, et al. Nasal high-frequency oscillatory ventilation versus nasal continuous positive airway pressure as primary respiratory support strategies for respiratory distress syndrome in preterm infants: a systematic review and meta-analysis. Eur J Pediatr. 2022;181:215–23.
202.Bruet S, Butin M, Dutheil F, et al. Systematic review of high-flow nasal cannula versus continuous positive airway pressure for primary support in preterm infants. Arch Dis Child Fetal Neonatal Ed. 2022;107:56–9.
203.Ramaswamy VV, More K, Roehr CC, et al. Efficacy of noninvasive respiratory support modes for primary respiratory support in preterm neonates with respiratory distress syndrome: systematic review and network meta-analysis. Pediatr Pulmonol. 2020;55:2940–63.
204.Luo K, Huang Y, Xiong T, et al. High-flow nasal cannula versus continuous positive airway pressure in primary respiratory support for preterm infants: a systematic review and meta-analysis. Front Pediatr. 2022;10:980024.
205.Lee J, Parikka V, Oda A, et al. NIV-NAVA versus NCPAP immediately after birth in premature infants: a randomized controlled trial. Respir Physiol Neurobiol. 2022;302:103916.
206.Kallio M, Mahlman M, Koskela U, et al. NIV NAVA versus nasal CPAP in premature infants: a randomized clinical trial. Neonatology. 2019;116:380–4.
207.Malakian A, Bashirnezhadkhabaz S, Aramesh MR, et al. Noninvasive high- frequency oscillatory ventilation versus nasal continuous positive airway pressure in preterm infants with respiratory distress syndrome: a randomized controlled trial. J Matern Fetal Neonatal Med. 2020;33:2601–7.
208.Saugstad OD, Aune D, Aguar M, et al. Systematic review and meta-analysis of optimal initial fraction of oxygen levels in the delivery room at ≤32 weeks. Acta Paediatr. 2014;103:744–51.
209.Brown JVE, Moe-Byrne T, Harden M, et al. Lower versus higher oxygen concentration for delivery room stabilisation of preterm neonates: systematic review. PLoS One. 2012;7:e52033.
210.Rook D, Schierbeek H, Vento M, et al. Resuscitation of preterm infants with
different inspired oxygen fractions. J Pediatr. 2014;164:1322–6.e3.
211.Tataranno ML, Oei JL, Perrone S, et al. Resuscitating preterm infants with 100% oxygen is associated with higher oxidative stress than room air. Acta Paediatr. 2015;104:759–65.
212.Dawson JA, Kamlin COF, Vento M, et al. Defining the reference range for
oxygen saturation for infants after birth. Pediatrics. 2010;125:e1340–7.
213.Lui K, Jones LJ, Foster JP, et al. Lower versus higher oxygen concentrations titrated to target oxygen saturations during resuscitation of preterm infants at birth. Cochrane Database Syst Rev. 2018;5:CD010239.
214.Oei JL, Kapadia V, Rabi Y, et al. Neurodevelopmental outcomes of preterm infants after randomisation to initial resuscitation with lower (FiO2<0.3) or higher (FiO2>0.6) initial oxygen levels: an individual patient meta-analysis. Arch Dis Child Fetal Neonatal Ed. 2022;107:386–92.
215.Thamrin V, Saugstad OD, Tarnow-Mordi W, et al. Preterm infant outcomes after randomization to initial resuscitation with FiO2 0.21 or 1.0. J Pediatr. 2018;201:55–61.e1.
216.Boronat N, Aguar M, Rook D, et al. Survival and neurodevelopmental outcomes of preterms resuscitated with different oxygen fractions. Pediatrics. 2016;138:e20161405.
217.Oei JL, Vento M, Rabi Y, et al. Higher or lower oxygen for delivery room resuscitation of preterm infants below 28 completed weeks gestation: a meta-analysis. Arch Dis Child Fetal Neonatal Ed. 2017;102:F24–30.
218.Tataranno ML, Oei JL, Perrone S, et al. Resuscitating preterm infants with 100% oxygen is associated with higher oxidative stress than room air. Acta Paediatr. 2015;104:759–65.
219.Solevåg AL, Schmölzer GM, Cheung PY, et al. Hypoxia-reoxygenation in neonatal cardiac arrest: results from experimental models. Semin Fetal Neonatal Med. 2020;25:101085.
220.Hassan MA, Mendler M, Maurer M, et al. Reliability of pulse oximetry during cardiopulmonary resuscitation in a piglet model of neonatal cardiac arrest. Neonatology. 2015;107:113–9.
221.Chen ML, Guo L, Smith LEH, et al. High or low oxygen saturation and severe retinopathy of prematurity: a meta-analysis. Pediatrics. 2010;125:e1483–92.
222.Saugstad OD, Aune D, et al. In search of the optimal oxygen saturation for extremely low birth weight infants: a systematic review and meta-analysis. Neonatology. 2011;100:1–8.
223.Saugstad OD, Aune D, et al. Optimal oxygenation of extremely low birth weight infants: a meta-analysis and systematic review of the oxygen saturation target studies. Neonatology. 2014;105:55–63.
224.Manja V, Lakshminrusimha S, Cook DJ, et al. Oxygen saturation target range for extremely preterm infants: a systematic review and meta-analysis. JAMA Pediatr. 2015;169:332–40.
225.Waitz M, Schmid MB, Fuchs H, et al. Effects of automated adjustment of the inspired oxygen on fluctuations of arterial and regional cerebral tissue oxygenation in preterm infants with frequent desaturations. J Pediatr. 2015;166:240–4.e1.
226.Claure N, Bancalari E, D’Ugard C, et al. Multicenter crossover study of automated control of inspired oxygen in ventilated preterm infants. Pediatrics. 2011;127:e76–83.
227.Wilinska M, Bachman T, Swietlinski J, et al. Automated FiO2-SpO2 control system in neonates requiring respiratory support: a comparison of a standard to a narrow SpO2 control range. BMC Pediatr. 2014;14:130.
228.Hallenberger A, Poets CF, Horn W, et al. Closed-loop automatic oxygen control (CLAC) in preterm infants: a randomized controlled trial. Pediatrics. 2014;133:e379–85.
229.Zapata J, Gómez JJ, Araque Campo R, et al. A randomised controlled trial of an automated oxygen delivery algorithm for preterm neonates receiving supplemental oxygen without mechanical ventilation. Acta Paediatr. 2014;103:928–33.
230.Askie LM, Darlow BA, Davis PG, et al. Effects of targeting lower versus higher arterial oxygen saturations on death or disability in preterm infants. Cochrane Database Syst Rev. 2017;4:CD011190.
231.Navarrete CT, Wrage LA, Carlo WA, et al. Growth outcomes of preterm infants exposed to different oxygen saturation target ranges from birth. J Pediatr. 2016;176:62–8.e4.
232.Walsh MC, Di Fiore JM, Martin RJ, et al. Association of oxygen target and growth status with increased mortality in small for gestational age infants: further analysis of the Surfactant, Positive Pressure and Pulse Oximetry Randomized Trial. JAMA Pediatr. 2016;170:292–4.
233.Engle WA, American Academy of Pediatrics Committee on Fetus and Newborn. Surfactant-replacement therapy for respiratory distress in the preterm and term neonate. Pediatrics. 2008;121:419–32.
234.Walsh BK, Daigle B, DiBlasi RM, et al. AARC clinical practice guideline: surfactant replacement therapy. Respir Care. 2013;58:367–75.
235.Polin RA, Carlo WA, Committee on Fetus and Newborn, American Academy of Pediatrics. Surfactant replacement therapy for preterm and term neonates with respiratory distress. Pediatrics. 2014;133:156–63.
236.Soll RF, et al. Prophylactic natural surfactant extract for preventing morbidity and mortality in preterm infants. Cochrane Database Syst Rev. 2000;(2):CD000511.
237.Soll RF, et al. Synthetic surfactant for respiratory distress syndrome in preterm infants. Cochrane Database Syst Rev. 2000;(2):CD001149.
238.Seger N, Soll R, et al. Animal derived surfactant extract for treatment of respiratory distress syndrome. Cochrane Database Syst Rev. 2009;(2):CD007836.
239.Soll R, Ozek E, et al. Prophylactic protein free synthetic surfactant for preventing morbidity and mortality in preterm infants. Cochrane Database Syst Rev. 2010;(1):CD001079.
240.Suresh GK, Soll RF, et al. Overview of surfactant replacement trials. J Perinatol. 2005;25 Suppl 2:S40–4.
241.Philip AG, et al. Neonatal mortality rate: is further improvement possible? J Pediatr. 1995;126:427–33.
242.Soll RF, Morley CJ, et al. Prophylactic versus selective use of surfactant in preventing morbidity and mortality in preterm infants. Cochrane Database Syst Rev. 2001;(2):CD000510.
243.Rojas-Reyes MX, Morley CJ, Soll R, et al. Prophylactic versus selective use of surfactant in preventing morbidity and mortality in preterm infants. Cochrane Database Syst Rev. 2012;3:CD000510.
244.Dunn MS, Kaempf J, de Klerk A, et al. Randomized trial comparing 3 approaches to the initial respiratory management of preterm neonates. Pediatrics. 2011;128:e1069–76.
245.Sandri F, Plavka R, Ancora G, et al. Prophylactic or early selective surfactant combined with nCPAP in very preterm infants. Pediatrics. 2010;125:e1402–9.
246.Finer NN, Carlo WA, Walsh MC, et al. Early CPAP versus surfactant in extremely preterm infants. N Engl J Med. 2010;362:1970–9.
247.Isayama T, Chai-Adisaksopha C, McDonald SD, et al. Noninvasive ventilation with vs without early surfactant to prevent chronic lung disease in preterm infants: a systematic review and meta-analysis. JAMA Pediatr. 2015;169:731–9.
248.Rojas MA, Lozano JM, Rojas MX, et al. Very early surfactant without mandatory ventilation in premature infants treated with early continuous positive airway pressure: a randomized controlled trial. Pediatrics. 2009;123:137–42.
249.Tapia JL, Urzua S, Bancalari A, et al. Randomized trial of early bubble continuous positive airway pressure for very low birth weight infants. J Pediatr. 2012;161:75–80.e1.
250.Stevens TP, Finer NN, Carlo WA, et al. Respiratory outcomes of the surfactant positive pressure and oximetry randomized trial (SUPPORT). J Pediatr. 2014;165:240–9.e4.
251.Nakhshab M, Tajbakhsh M, Khani S, et al. Comparison of the effect of surfactant administration during nasal continuous positive airway pressure with that of nasal continuous positive airway pressure alone on complications of respiratory distress syndrome: a randomized controlled study. Pediatr Neonatol. 2015;56:88–94.
252.Roehr CC, Proquitté H, Hammer H, et al. Positive effects of early continuous positive airway pressure on pulmonary function in extremely premature infants: results of a subgroup analysis of the COIN trial. Arch Dis Child Fetal Neonatal Ed. 2011;96:F371–3.
253.Rodriguez-Fanjul J, Jordan I, Balaguer M, et al. Early surfactant replacement guided by lung ultrasound in preterm newborns with RDS: the ULTRASURF randomised controlled trial. Eur J Pediatr. 2020;179:1913–20.
254.Capasso L, Pacella D, Migliaro F, et al. Can lung ultrasound score accurately predict surfactant replacement? A systematic review and meta-analysis of diagnostic test studies. Pediatr Pulmonol. 2023;58:1427–37.
255.Stevens TP, Harrington EW, Blennow M, et al. Early surfactant administration with brief ventilation vs selective surfactant and continued mechanical ventilation for preterm infants with or at risk for respiratory distress syndrome. Cochrane Database Syst Rev. 2007:CD003063.
256.Verder H, Robertson B, Greisen G, et al. Surfactant therapy and nasal continuous positive airway pressure for newborns with respiratory distress syndrome. N Engl J Med. 1994;331:1051–5.
257.Aldana-Aguirre JC, Pinto M, Featherstone RM, et al. Less invasive surfactant administration versus intubation for surfactant delivery in preterm infants with respiratory distress syndrome: a systematic review and meta-analysis. Arch Dis Child Fetal Neonatal Ed. 2017;102:F17–23.
258.Silveira RC, Panceri C, Munõz NP, et al. Less invasive surfactant administration versus intubation-surfactant-extubation in the treatment of neonatal respiratory distress syndrome: a systematic review and meta- analyses. J Pediatr (Rio J). 2024;100:8–24.
259.Al Ali RA, Gautam B, Miller MR, et al. Laryngeal mask airway for surfactant administration versus standard treatment methods in preterm neonates with respiratory distress syndrome: a systematic review and meta- analysis. Am J Perinatol. 2022;39:1433–40.
260.Gallup JA, Ndakor SM, Pezzano C, et al. Randomized trial of surfactant therapy via laryngeal mask airway versus brief tracheal intubation in neonates born preterm. J Pediatr. 2023;254:17–24.e2.
261.Rebello CM, Precioso AR, Mascaretti RS, et al. A multicenter, randomized, double-blind trial of a new porcine surfactant in premature infants with respiratory distress syndrome. Einstein (Sao Paulo). 2014;12:397–404.
262.Trembath A, Hornik CP, Clark R, et al. Comparative effectiveness of
surfactant preparations in premature infants. J Pediatr. 2013;163:955–60.e1.
263.Dani C, Ravasio R, Fioravanti L, et al. Analysis of the cost-effectiveness of surfactant treatment (Curosurf) in respiratory distress syndrome therapy in preterm infants: early treatment compared to late treatment. Ital J Pediatr. 2014;40:40.
264.Eras Z, Dizdar EA, Kanmaz G, et al. Neurodevelopmental outcomes of very low birth weight preterm infants treated with poractant alfa versus beractant for respiratory distress syndrome. Am J Perinatol. 2014;31:463–8.
265.Singh N, Hawley KL, Viswanathan K, et al. Efficacy of porcine versus bovine surfactants for preterm newborns with respiratory distress syndrome: systematic review and meta-analysis. Pediatrics. 2011;128:e1588–95.
266.Speer CP, Robertson B, Curstedt T, et al. Randomized European multicenter trial of surfactant replacement therapy for severe neonatal respiratory distress syndrome: single versus multiple doses of Curosurf. Pediatrics. 1992;89:13–20.
267.Carnielli VP, Zimmermann LJI, Hamvas A, et al. Pulmonary surfactant kinetics of the newborn infant: novel insights from studies with stable isotopes. J Perinatol. 2009;29 Suppl 2:S29–37.
268.Cogo PE, Facco M, Simonato M, et al. Dosing of porcine surfactant: effect on kinetics and gas exchange in respiratory distress syndrome. Pediatrics. 2009;124:e950–7.
269.Rong Z, Chang L, Cheng H, et al. A multicentered randomized study on early versus rescue Calsurf administration for the treatment of respiratory distress syndrome in preterm infants. Am J Perinatol. 2019;36:1492–7.
270.Henderson-Smart DJ, De Paoli AG, et al. Methylxanthine treatment for apnoea in preterm infants. Cochrane Database Syst Rev. 2010;(12):CD000140.
271.Henderson-Smart DJ, Davis PG, et al. Prophylactic methylxanthines for endotracheal extubation in preterm infants. Cochrane Database Syst Rev. 2010:CD000139.
272.Schmidt B, Roberts RS, Davis P, et al. Caffeine therapy for apnea of
prematurity. N Engl J Med. 2006;354:2112–21.
273.Katheria AC, Sauberan JB, Akotia D, et al. A pilot randomized controlled trial of early versus routine caffeine in extremely premature infants. Am J Perinatol. 2015;32:879–86.
274.Schmidt B, Roberts RS, Davis P, et al. Long-term effects of caffeine therapy
for apnea of prematurity. N Engl J Med. 2007;357:1893–902.
275.Schmidt B, Anderson PJ, Doyle LW, et al. Survival without disability to age 5 years after neonatal caffeine therapy for apnea of prematurity. JAMA. 2012;307:275–82.
276.Davis PG, Schmidt B, Roberts RS, et al. Caffeine for Apnea of Prematurity trial: benefits may vary in subgroups. J Pediatr. 2010;156:382–7.
277.Doyle LW, Cheong J, Hunt RW, et al. Caffeine and brain development in
very preterm infants. Ann Neurol. 2010;68:734–42.
278.Charles BG, Townsend SR, Steer PA, et al. Caffeine citrate treatment for extremely premature infants with apnea: population pharmacokinetics, absolute bioavailability, and implications for therapeutic drug monitoring. Ther Drug Monit. 2008;30:709–16.
279.Steer P, Flenady V, Shearman A, et al. High dose caffeine citrate for extubation of preterm infants: a randomised controlled trial. Arch Dis Child Fetal Neonatal Ed. 2004;89:F499–503.
280.Mohammed S, Nour I, Shabaan AE, et al. High versus low-dose caffeine for apnea of prematurity: a randomized controlled trial. Eur J Pediatr. 2015;174:949–56.
281.Skouroliakou M, Bacopoulou F, Markantonis SL, et al. Caffeine versus theophylline for apnea of prematurity: a randomised controlled trial. J Paediatr Child Health. 2009;45:587–92.
282.Schmidt B, Roberts RS, Anderson PJ, et al. Academic performance, motor function, and behavior 11 years after neonatal caffeine citrate therapy for apnea of prematurity: an 11-year follow-up of the CAP randomized clinical trial. JAMA Pediatr. 2017;171:564–72.
283.Pakvasa MA, Saroha V, Patel RM, et al. Optimizing caffeine use and risk of bronchopulmonary dysplasia in preterm infants: a systematic review, meta-analysis, and application of grading of recommendations assessment, development, and evaluation methodology. Clin Perinatol. 2018;45:273–91.
284.Sajjadian N, Taheri PA, Jabbari M, et al. Is early preventive caffeine safe and effective in premature neonates? A clinical trial. Int J Pediatr. 2022;2022:8701598.
285.Lodha A, Entz R, Synnes A, et al. Early caffeine administration and neurodevelopmental outcomes in preterm infants. Pediatrics. 2019;143:e20181348.
286.Kua KP, Lee SW, et al. Systematic review and meta-analysis of clinical outcomes of early caffeine therapy in preterm neonates. Br J Clin Pharmacol. 2017;83:180–91.
287.Chen J, Jin L, Chen X, et al. Efficacy and safety of different maintenance doses of caffeine citrate for treatment of apnea in premature infants: a systematic review and meta-analysis. Biomed Res Int. 2018;2018:9061234.
288.Brattström P, Russo C, Ley D, et al. High-versus low-dose caffeine in preterm infants: a systematic review and meta-analysis. Acta Paediatr. 2019;108:401– 10.
289.McPherson C, Lean RE, Cyr PEP, et al. Five-year outcomes of premature infants randomized to high or standard loading dose caffeine. J Perinatol. 2022;42:631–5.
290.Vesoulis ZA, McPherson C, Neil JJ, et al. Early high-dose caffeine increases seizure burden in extremely preterm neonates: a preliminary study. J Caffeine Res. 2016;6:101–7.
291.Chung J, Tran Lopez K, Amendolia B, et al. Stopping caffeine in premature neonates: how long does it take for the level of caffeine to fall below the therapeutic range? J Matern Fetal Neonatal Med. 2022;35:551–5.
292.Dempsey EM, Barrington KJ, et al. Treating hypotension in the preterm infant: when and with what: a critical and systematic review. J Perinatol. 2007;27:469–78.
293.Ibrahim CPH, et al. Hypotension in preterm infants. Indian Pediatr. 2008;45:285–94.
294.Dempsey EM, Barrington KJ, et al. Evaluation and treatment of hypotension in the preterm infant. Clin Perinatol. 2009;36:75–85.
295.Dempsey EM, Barrington KJ, Marlow N, et al. Management of hypotension in preterm infants (The HIP Trial): a randomised controlled trial of hypotension management in extremely low gestational age newborns. Neonatology. 2014;105:275–81.
296.Batton B, Li L, Newman NS, et al. Use of antihypotensive therapies in extremely preterm infants. Pediatrics. 2013;131:e1865–73.
297.Vargo L, Seri I, et al. New NANN practice guideline: the management of hypotension in the very-low-birth-weight infant. Adv Neonatal Care. 2011;11:272–8.
298.Synnes AR, Chien LY, Peliowski A, et al. Variations in intraventricular hemorrhage incidence rates among Canadian neonatal intensive care units. J Pediatr. 2001;138:525–31.
299.British Association of Perinatal Medicine; Royal College of Physicians. Development of audit measures and guidelines for good practice in the management of neonatal respiratory distress syndrome. Arch Dis Child. 1992;67:1221–7.
300.Dempsey EM, Al Hazzani F, Barrington KJ, et al. Permissive hypotension in the extremely low birthweight infant with signs of good perfusion. Arch Dis Child Fetal Neonatal Ed. 2009;94:F241–4.
301.Gale C, et al. Question 2. Is capillary refill time a useful marker of haemodynamic status in neonates? Arch Dis Child. 2010;95:395–7.
302.Miletin J, Pichova K, Dempsey EM, et al. Bedside detection of low systemic flow in the very low birth weight infant on day 1 of life. Eur J Pediatr. 2009;168:809–13.
303.Wardle SP, Yoxall CW, Weindling AM, et al. Peripheral oxygenation in hypotensive preterm babies. Pediatr Res. 1999;45:343–9.
304.Nerdrum Aagaard E, Solevåg AL, Saugstad OD, et al. Significance of neonatal heart rate in the delivery room—a review. Children (Basel). 2023;10:1551.
305.Kapadia V, Oei JL, Finer N, et al. Outcomes of delivery room resuscitation of bradycardic preterm infants: a retrospective cohort study of randomised trials of high vs low initial oxygen concentration and an individual patient data analysis. Resuscitation. 2021;167:209–17.
306.Dempsey EM, Barrington KJ, Marlow N, et al. Hypotension in Preterm Infants (HIP) randomised trial. Arch Dis Child Fetal Neonatal Ed. 2021;106:398–403.
307.Thewissen L, Naulaers G, Hendrikx D, et al. Cerebral oxygen saturation and autoregulation during hypotension in extremely preterm infants. Pediatr Res. 2021;90:373–80.
308.da Costa CS, Czosnyka M, Smielewski P, et al. Optimal mean arterial blood pressure in extremely preterm infants within the first 24 hours of life. J Pediatr. 2018;203:242–8.
309.Chock VY, Kwon SH, Ambalavanan N, et al. Cerebral oxygenation and autoregulation in preterm infants (Early NIRS study). J Pediatr. 2020;227:94– 100.e1.
310.Gautam B, Surak A, Campbell SM, et al. Superior vena cava flow in preterm infants and neonatal outcomes: a systematic review. Am J Perinatol. 2024;41:e2356–64.
311.da Costa CS, Cardim D, Molnar Z, et al. Changes in hemodynamics, cerebral oxygenation and cerebrovascular reactivity during the early transitional circulation in preterm infants. Pediatr Res. 2019;86:247–53.
312.Seri I, et al. Circulatory support of the sick preterm infant. Semin Neonatol. 2001;6:85–95.
313.Seri I, Evans J, et al. Controversies in the diagnosis and management of hypotension in the newborn infant. Curr Opin Pediatr. 2001;13:116–23.
314.Fanaroff JM, Fanaroff AA, et al. Blood pressure disorders in the neonate:
hypotension and hypertension. Semin Fetal Neonatal Med. 2006;11:174–81.
315.Osborn DA, Evans N, et al. Early volume expansion for prevention of morbidity and mortality in very preterm infants. Cochrane Database Syst Rev. 2004;(2):CD002055.
316.Osborn DA, Evans N, et al. Early volume expansion versus inotrope for prevention of morbidity and mortality in very preterm infants. Cochrane Database Syst Rev. 2001;(2):CD002056.
317.Wong W, Fok TF, Lee CH, et al. Randomised controlled trial: comparison of colloid or crystalloid for partial exchange transfusion for treatment of neonatal polycythaemia. Arch Dis Child Fetal Neonatal Ed. 1997;77:F115–8.
318.Sarafidis K, Verykouki E, Nikopoulos S, et al. Systematic review and meta- analysis of cardiovascular medications in neonatal hypotension. Biomed Hub. 2022;7:70–9.
319.Osborn DA, Paradisis M, Evans N, et al. The effect of inotropes on morbidity and mortality in preterm infants with low systemic or organ blood flow. Cochrane Database Syst Rev. 2007;(1):CD005090.
320.McNamara PJ, Giesinger RE, Lakshminrusimha S, et al. Dopamine and neonatal pulmonary hypertension—pressing need for a better pressor? J Pediatr. 2022;246:242–50.
321.Cheung PY, Barrington KJ, et al. The effects of dopamine and epinephrine on hemodynamics and oxygen metabolism in hypoxic anesthetized piglets. Crit Care. 2001;5:158–66.
322.Bouissou A, Rakza T, Klosowski S, et al. Hypotension in preterm infants with significant patent ductus arteriosus: effects of dopamine. J Pediatr. 2008;153:790–4.
323.Gupta S, Donn SM, et al. Neonatal hypotension: dopamine or dobutamine? Semin Fetal Neonatal Med. 2014;19:54–9.
324.Noori S, Seri I, et al. Neonatal blood pressure support: the use of inotropes, lusitropes, and other vasopressor agents. Clin Perinatol. 2012;39:221–38.
325.Seri I, et al. Management of hypotension and low systemic blood flow in the very low birth weight neonate during the first postnatal week. J Perinatol. 2006;26 Suppl 1:S8–13.
326.Ibrahim H, Sinha IP, Subhedar NV, et al. Corticosteroids for treating hypotension in preterm infants. Cochrane Database Syst Rev. 2011;(12):CD003662.
327.Paradisis M, Evans N, Kluckow M, et al. Randomized trial of milrinone versus placebo for prevention of low systemic blood flow in very preterm infants. J Pediatr. 2009;154:189–95.
328.El-Khuffash AF, Jain A, Weisz D, et al. Assessment and treatment of post
patent ductus arteriosus ligation syndrome. J Pediatr. 2014;165:46–52.e1.
329.Hallik M, Ilmoja ML, Tasa T, et al. Population pharmacokinetics and dosing of milrinone after patent ductus arteriosus ligation in preterm infants. Pediatr Crit Care Med. 2019;20:621–9.
330.Koletzko B, Goulet O, Hunt J, et al. Guidelines on paediatric parenteral nutrition of ESPGHAN and ESPEN, supported by ESPR. J Pediatr Gastroenterol Nutr. 2005;41 Suppl 2:S1–87.
331.Moyses HE, Johnson MJ, Leaf AA, et al. Early parenteral nutrition and growth outcomes in preterm infants: a systematic review and meta-analysis. Am J Clin Nutr. 2013;97:816–26.
332.Vlaardingerbroek H, Veldhorst MAB, Spronk S, et al. Parenteral lipid administration to very-low-birth-weight infants—early introduction of lipids and use of new lipid emulsions: a systematic review and meta-analysis. Am J Clin Nutr. 2012;96:255–68.
333.Uthaya S, Modi N, et al. Practical preterm parenteral nutrition: systematic literature review and recommendations for practice. Early Hum Dev. 2014;90:747–53.
334.Koletzko B, Poindexter B, Uauy R, et al. Recommended nutrient intake levels for stable, fully enterally fed very low birth weight infants. World Rev Nutr Diet. 2014;110:297–9.
335.Blanco CL, Gong AK, Schoolfield J, et al. Impact of early and high amino acid supplementation on ELBW infants at 2 years. J Pediatr Gastroenterol Nutr. 2012;54:601–7.
336.Sinclair JC, Bottino M, Cowett RM, et al. Interventions for prevention of neonatal hyperglycemia in very low birth weight infants. Cochrane Database Syst Rev. 2011;(10):CD007615.
337.Trivedi A, Sinn JKH, et al. Early versus late administration of amino acids in preterm infants receiving parenteral nutrition. Cochrane Database Syst Rev. 2013;7:CD008771.
338.Bell EF, Acarregui MJ, et al. Restricted versus liberal water intake for preventing morbidity and mortality in preterm infants. Cochrane Database Syst Rev. 2014;12:CD000503.
339.Bhatia J, et al. Human milk and the premature infant. Ann Nutr Metab. 2013;62 Suppl 3:8–14.
340.Ziegler EE, et al. Meeting the nutritional needs of the low-birth-weight infant. Ann Nutr Metab. 2011;58 Suppl 1:8–18.
341.Colaizy TT, et al. Donor human milk for preterm infants: what it is, what it can do, and what still needs to be learned. Clin Perinatol. 2014;41:437–50.
342.Quigley M, McGuire W, et al. Formula versus donor breast milk for feeding preterm or low birth weight infants. Cochrane Database Syst Rev. 2014;4:CD002971.
343.Agostoni C, Buonocore G, Carnielli VP, et al. Enteral nutrient supply for preterm infants: commentary from the ESPGHAN Committee on Nutrition. J Pediatr Gastroenterol Nutr. 2010;50:85–91.
344.Morgan J, Young L, McGuire W, et al. Delayed introduction of progressive enteral feeds to prevent necrotising enterocolitis in very low birth weight infants. Cochrane Database Syst Rev. 2014;12:CD001970.
345.Rövekamp-Abels LWW, Hogewind-Schoonenboom JE, de Wijs-Meijler DPM, et al. Intermittent bolus or semi-continuous feeding for preterm infants? A randomised controlled trial. J Pediatr Gastroenterol Nutr. 2015;60:754–60.
346.Morgan J, Bombell S, McGuire W. Early trophic feeding versus enteral fasting for very preterm or very low birth weight infants. Cochrane Database Syst Rev. 2013;3:CD000504.
347.Premji SS, Chessell L, et al. Continuous nasogastric milk feeding versus intermittent bolus milk feeding for premature infants less than 1500 grams. Cochrane Database Syst Rev. 2011;(11):CD001819.
348.Arslanoglu S, Boquien CY, King C, et al. Fortification of human milk for preterm infants: update and recommendations of the European Milk Bank Association Working Group on Human Milk Fortification. Front Pediatr. 2019;7:76.
349.ESPGHAN Committee on Nutrition, Arslanoglu S, Corpeleijn W, et al. Donor human milk for preterm infants: current evidence and research directions. J Pediatr Gastroenterol Nutr. 2013;57:535–42.
350.Senterre T, et al. Practice of enteral nutrition in very low birth weight and extremely low birth weight infants. World Rev Nutr Diet. 2014;110:201–14.
351.Sharif S, Meader N, Oddie SJ, et al. Probiotics to prevent necrotising enterocolitis in very preterm or very low birth weight infants. Cochrane Database Syst Rev. 2020;10:CD005496.
352.Sun J, Marwah G, Westgarth M, et al. Effects of probiotics on necrotizing enterocolitis, sepsis, intraventricular hemorrhage, mortality, length of hospital stay, and weight gain in very preterm infants: a meta-analysis. Adv Nutr. 2017;8:749–63.
353.Aceti A, Maggio L, Beghetti I, et al. Probiotics prevent late-onset sepsis in human milk-fed, very low birth weight preterm infants: systematic review and meta-analysis. Nutrients. 2017;9:904.
354.Dermyshi E, Wang Y, Yan C, et al. The “golden age” of probiotics: a systematic review and meta-analysis of randomized and observational studies in preterm infants. Neonatology. 2017;112:9–23.
355.Thomas JP, Raine T, Reddy S, et al. Probiotics for the prevention of necrotising enterocolitis in very low-birth-weight infants: a meta-analysis and systematic review. Acta Paediatr. 2017;106:1729–41.
356.van den Akker CHP, van Goudoever JB, Shamir R, et al. Probiotics and preterm infants: a position paper by ESPGHAN Committee on Nutrition and ESPGHAN Working Group for Probiotics and Prebiotics. J Pediatr Gastroenterol Nutr. 2020;70:664–80.
357.Embleton ND, Moltu SJ, Lapillonne A, et al. Enteral nutrition in preterm infants (2022): a position paper from the ESPGHAN Committee on Nutrition and invited experts. J Pediatr Gastroenterol Nutr. 2023;76:248–68.
358.Darlow BA, Graham PJ, Rojas-Reyes MX, et al. Vitamin A supplementation to prevent mortality and short- and long-term morbidity in very low birth weight infants. Cochrane Database Syst Rev. 2016;(8):CD000501.
359.Ye Y, Yang X, Zhao J, et al. Early vitamin A supplementation for prevention of short-term morbidity and mortality in very-low-birth-weight infants: a systematic review and meta-analysis. Front Pediatr. 2022;10:788409.
360.Basu S, Khanna P, Srivastava R, et al. Oral vitamin A supplementation in very low birth weight neonates: a randomized controlled trial. Eur J Pediatr. 2019;178:1255–65.
361.Rakshasbhuvankar AA, Simmer K, Patole SK, et al. Enteral vitamin A for reducing severity of bronchopulmonary dysplasia: a randomized trial. Pediatrics. 2021;147:e20200193.
362.Meyer S, Gortner L, NeoVitaA Trial Investigators, et al. Early postnatal additional high-dose oral vitamin A supplementation versus placebo for 28 days for preventing bronchopulmonary dysplasia or death in extremely low birth weight infants. Neonatology. 2014;105:182–8.
363.Phattraprayoon N, Ungtrakul T, Soonklang K, et al. Oral vitamin A supplementation in preterm infants to improve health outcomes: a systematic review and meta-analysis. PLoS One. 2022;17:e0265876.
364.Manapurath RM, Kumar M, Pathak BG, et al. Enteral low-dose vitamin A supplementation in preterm or low birth weight infants to prevent morbidity and mortality: a systematic review and meta-analysis. Pediatrics. 2022;150:e2022057092L.
365.Araki S, Kato S, Namba F, et al. Vitamin A to prevent bronchopulmonary dysplasia in extremely low birth weight infants: a systematic review and meta-analysis. PLoS One. 2018;13:e0207730.
366.Benitz WE, Committee on Fetus and Newborn, et al. Patent ductus arteriosus in preterm infants. Pediatrics. 2016;137:1–6.
367.Schmidt B, Davis P, Moddemann D, et al. Long-term effects of indomethacin prophylaxis in extremely-low-birth-weight infants. N Engl J Med. 2001;344:1966–72.
368.de Carvalho Nunes G, Wutthigate P, Simoneau J, et al. Natural evolution of the patent ductus arteriosus in the extremely premature newborn and respiratory outcomes. J Perinatol. 2022;42:642–8.
369.Ohlsson A, Shah SS, et al. Ibuprofen for the prevention of patent ductus arteriosus in preterm and/or low birth weight infants. Cochrane Database Syst Rev. 2011;(7):CD004213.
370.Fowlie PW, Davis PG, McGuire W, et al. Prophylactic intravenous indomethacin for preventing mortality and morbidity in preterm infants. Cochrane Database Syst Rev. 2010;(7):CD000174.
371.Stewart A, Brion LP, Soll R, et al. Diuretics for respiratory distress syndrome in preterm infants. Cochrane Database Syst Rev. 2011;(12):CD001454.
372.De Buyst J, Rakza T, Pennaforte T, et al. Hemodynamic effects of fluid restriction in preterm infants with significant patent ductus arteriosus. J Pediatr. 2012;161:404–8.
373.Nayeri FS, Esmaeilnia Shirvani T, Aminnezhad M, et al. Comparison of INSURE method with conventional mechanical ventilation after surfactant administration in preterm infants with respiratory distress syndrome: therapeutic challenge. Acta Med Iran. 2014;52:596–600.
374.Sydney Local Health District. PDA guideline. 2014. http://www.slhd.nsw. gov.au/rpa/neonatal/content/pdf/guidelines/PDA_2014_guideline.pdf.
375.DeMauro SB, Cohen MS, Ratcliffe SJ, et al. Serial echocardiography in very
preterm infants: a pilot randomized trial. Acta Paediatr. 2013;102:1048–53.
376.Rozé JC, Cambonie G, Marchand-Martin L, et al. Association between early screening for patent ductus arteriosus and in-hospital mortality among extremely preterm infants. JAMA. 2015;313:2441–8.
377.Thankavel PP, Rosenfeld CR, Christie L, et al. Early echocardiographic prediction of ductal closure in neonates ≤30 weeks gestation. J Perinatol. 2013;33:45–51.
378.Mitra S, Weisz D, Jain A, et al. Management of the patent ductus arteriosus in preterm infants. Paediatr Child Health. 2022;27:63–4.
379.Hanke K, Fortmann I, Humberg A, et al. Indomethacin prophylaxis is associated with reduced risk of intraventricular hemorrhage in extremely preterm infants born in the context of amniotic infection syndrome. Neonatology. 2023;120:334–43.
380.Clyman RI, Hills NK, et al. Effects of prophylactic indomethacin on morbidity and mortality in infants <25 weeks’ gestation: a protocol driven intention to treat analysis. J Perinatol. 2022;42:1662–8.
381.Hamrick SEG, Sallmon H, Rose AT, et al. Patent ductus arteriosus of the preterm infant. Pediatrics. 2020;146:e20201209.
382.Schmidt B, Davis P, Moddemann D, et al. Long-term effects of indomethacin prophylaxis in extremely-low-birth-weight infants. N Engl J Med. 2001;344:1966–72.
383.Mitra S, de Boode WP, Weisz DE, et al. Interventions for patent ductus arteriosus (PDA) in preterm infants: an overview of Cochrane systematic reviews. Cochrane Database Syst Rev. 2023;4:CD013588.
384.Hundscheid T, Jansen EJS, Onland W, et al. Conservative management of patent ductus arteriosus in preterm infants: a systematic review and meta- analyses assessing differences in outcome measures between randomized controlled trials and cohort studies. Front Pediatr. 2021;9:626261.
385.Rozé JC, Cambonie G, Le Thuaut A, et al. Effect of early targeted treatment of ductus arteriosus with ibuprofen on survival without cerebral palsy at 2 years in infants with extreme prematurity: a randomized clinical trial. J Pediatr. 2021;233:33–42.e2.
386.Hundscheid T, Onland W, Kooi EMW, et al. Expectant management or early ibuprofen for patent ductus arteriosus. N Engl J Med. 2023;388:980–90.
387.Bornehag CG, Reichenberg A, Hallerback MU, et al. Prenatal exposure to acetaminophen and children’s language development at 30 months. Eur Psychiatry. 2018;51:98–103.
388.Bauer AZ, Kriebel D, Herbert MR, et al. Prenatal paracetamol exposure and child neurodevelopment: a review. Horm Behav. 2018;101:125–47.
389.Ohlsson A, Shah SS, et al. Ibuprofen for the prevention of patent ductus arteriosus in preterm and/or low birth weight infants. Cochrane Database Syst Rev. 2020;1:CD004213.
390.National Collaborating Centre for Women’s and Children’s Health (UK). Antibiotics for early-onset neonatal infection: antibiotics for the prevention and treatment of early-onset neonatal infection. London: RCOG Press; 2012. http://www.ncbi.nlm.nih.gov/books/NBK116610/.
391.Caffrey Osvald E, Prentice P, et al. NICE clinical guideline: antibiotics for the prevention and treatment of early-onset neonatal infection. Arch Dis Child Educ Pract Ed. 2014;99:98–100.
392.Clifford V, Garland SM, Grimwood K, et al. Prevention of neonatal group B streptococcus disease in the 21st century. J Paediatr Child Health. 2012;48:808–15.
393.Brady MT, Polin RA, et al. Prevention and management of infants with suspected or proven neonatal sepsis. Pediatrics. 2013;132:166–8.
394.Polin RA, Committee on Fetus and Newborn, et al. Management of neonates with suspected or proven early-onset bacterial sepsis. Pediatrics. 2012;129:1006–15.
395.Tagare A, Kadam S, Vaidya U, et al. Routine antibiotic use in preterm neonates: a randomised controlled trial. J Hosp Infect. 2010;74:332–6.
396.Stocker M, Berger C, McDougall J, et al. Recommendations for term and late preterm infants at risk for perinatal bacterial infection. Swiss Med Wkly. 2013;143:w13873.
397.Tzialla C, Borghesi A, Longo S, et al. Which is the optimal algorithm for the prevention of neonatal early-onset group B streptococcus sepsis? Early Hum Dev. 2014;90 Suppl 1:S35–8.
398.Verani JR, McGee L, Schrag SJ, et al. Prevention of perinatal group B streptococcal disease—revised guidelines from CDC, 2010. MMWR Recomm Rep. 2010;59:1–36.
399.Committee on Infectious Diseases, Committee on Fetus and Newborn, Baker CJ, et al. Recommendations for the prevention of perinatal group B streptococcal disease. Pediatrics. 2011;128:611–6.
400.Campbell N, Eddy A, Darlow B, et al. The prevention of early-onset neonatal group B streptococcus infection: technical report from the New Zealand GBS Consensus Working Party. N Z Med J. 2004;117:U1023.
401.Escobar GJ, Li DK, Armstrong MA, et al. Neonatal sepsis workups in infants ≥2000 grams at birth: a population-based study. Pediatrics. 2000;106:256–63.
402.Cotten CM, Smith PB, et al. Duration of empirical antibiotic therapy for infants suspected of early-onset sepsis. Curr Opin Pediatr. 2013;25:167–71.
403.Kuppala VS, Meinzen-Derr J, Morrow AL, et al. Prolonged initial empirical antibiotic treatment is associated with adverse outcomes in premature infants. J Pediatr. 2011;159:720–5.
404.Pasha YZ, Ahmadpour-Kacho M, Behmadi R, et al. 3-day versus 5-day course of intravenous antibiotics for suspected early onset neonatal sepsis: a randomized controlled trial. Iran J Pediatr. 2014;24:673–8.
405.Metsvaht T, Ilmoja ML, Parm U, et al. Ampicillin versus penicillin in the empiric therapy of extremely low-birthweight neonates at risk of early onset sepsis. Pediatr Int. 2011;53:873–80.
406.Metsvaht T, Ilmoja ML, Parm U, et al. Comparison of ampicillin plus gentamicin vs. penicillin plus gentamicin in empiric treatment of neonates at risk of early onset sepsis. Acta Paediatr. 2010;99:665–72.
407.Stockmann C, Spigarelli MG, Campbell SC, et al. Considerations in the pharmacologic treatment and prevention of neonatal sepsis. Paediatr Drugs. 2014;16:67–81.
408.Fan X, Zhang L, Tang J, et al. The initial prophylactic antibiotic usage and subsequent necrotizing enterocolitis in high-risk premature infants: a systematic review and meta-analysis. Pediatr Surg Int. 2018;34:35–45.
409.Rina P, Zeng Y, Ying J, et al. Association of initial empirical antibiotic therapy with increased risk of necrotizing enterocolitis. Eur J Pediatr. 2020;179:1047–56.
410.Ting JY, Roberts A, Sherlock R, et al. Duration of initial empirical antibiotic therapy and outcomes in very low birth weight infants. Pediatrics. 2019;143:e20182286.
411.Fajardo C, Alshaikh B, Harabor A, et al. Prolonged use of antibiotics after birth is associated with increased morbidity in preterm infants with negative cultures. J Matern Fetal Neonatal Med. 2019;32:4060–6.
412.Ohlsson A, Shah PS, et al. Paracetamol (acetaminophen) for prevention or treatment of pain in newborns. Cochrane Database Syst Rev. 2020;1:CD011219.
413.Eriksson M, Campbell-Yeo M, et al. Assessment of pain in newborn infants. Semin Fetal Neonatal Med. 2019;24:101003.
414.Giordano V, Edobor J, Deindl P, et al. Pain and sedation scales for neonatal and pediatric patients in a preverbal stage of development: a systematic review. JAMA Pediatr. 2019;173:1186–93.
415.World Health Organization. Guidelines on neonatal pain assessment and management. Geneva: WHO; 2017.
416.Kinoshita M, Olsson E, Borys F, et al. Opioids for procedural pain in neonates. Cochrane Database Syst Rev. 2023;4:CD015056.
417.East of England Benchmarking Group. Clinical guideline: pain management. Version 4.0. NHS; 2021.
418.Bellù R, Romantsik O, Nava C, et al. Opioids for newborn infants receiving mechanical ventilation. Cochrane Database Syst Rev. 2021;3:CD013732.
419.Hand IL, Shellhaas RA, Milla SS, et al. Routine neuroimaging of the preterm brain. Pediatrics. 2020;146:e2020029082.
420.Guillot M, Chau V, Lemyre B, et al. Routine imaging of the preterm neonatal brain. Paediatr Child Health. 2020;25:249–62.
421.McLean G, Malhotra A, Lombardo P, et al. Cranial ultrasound screening protocols for very preterm infants. Ultrasound Med Biol. 2021;47:1645–56.
422.Roufaeil C, Razak A, Malhotra A, et al. Cranial ultrasound abnormalities in small for gestational age or growth-restricted infants born over 32 weeks gestation: a systematic review and meta-analysis. Brain Sci. 2022;12:1713.
423.Hinojosa-Rodríguez M, Harmony T, Carrillo-Prado C, et al. Clinical neuroimaging in the preterm infant: diagnosis and prognosis. Neuroimage Clin. 2017;16:355–68.
424.Ibrahim J, Mir I, Chalak L, et al. Brain imaging in preterm infants <32 weeks gestation: a clinical review and algorithm for the use of cranial ultrasound and qualitative brain MRI. Pediatr Res. 2018;84:799–806.
425.Craig JW, Glick C, Phillips R, et al. Recommendations for involving the family in developmental care of the NICU baby. J Perinatol. 2015;35 Suppl 1:S5–8.
426.Welch MG, Hofer MA, Stark RI, et al. Randomized controlled trial of Family Nurture Intervention in the NICU: assessments of length of stay, feasibility and safety. BMC Pediatr. 2013;13:148.
427.Ohlsson A, Jacobs SE, et al. NIDCAP: a systematic review and meta- analyses of randomized controlled trials. Pediatrics. 2013;131:e881–93.
428.Conde-Agudelo A, Díaz-Rossello JL, et al. Kangaroo mother care to reduce morbidity and mortality in low birthweight infants. Cochrane Database Syst Rev. 2014;4:CD002771.
429.Moore ER, Anderson GC, Bergman N, et al. Early skin-to-skin contact for mothers and their healthy newborn infants. Cochrane Database Syst Rev. 2012;5:CD003519.
430.Mori R, Khanna R, Pledge D, et al. Meta-analysis of physiological effects of skin-to-skin contact for newborns and mothers. Pediatr Int. 2010;52:161–70.
431.Nimbalkar SM, Patel VK, Patel DV, et al. Effect of early skin-to-skin contact following normal delivery on incidence of hypothermia in neonates more than 1800 g: randomized control trial. J Perinatol. 2014;34:364–8.
432.Ludington-Hoe SM, Johnson MW, Morgan K, et al. Neurophysiologic assessment of neonatal sleep organization: preliminary results of a randomized, controlled trial of skin contact with preterm infants. Pediatrics. 2006;117:e909–23.
433.Lawn JE, Mwansa-Kambafwile J, Horta BL, et al. “Kangaroo mother care” to prevent neonatal deaths due to preterm birth complications. Int J Epidemiol. 2010;39 Suppl 1:i144–54.
434.Athanasopoulou E, Fox JRE, et al. Effects of kangaroo mother care on maternal mood and interaction patterns between parents and their preterm, low birth weight infants: a systematic review. Infant Ment Health J. 2014;35:245–62.
435.Korja R, Latva R, Lehtonen L, et al. The effects of preterm birth on mother- infant interaction and attachment during the infant’s first two years. Acta Obstet Gynecol Scand. 2012;91:164–73.
436.Johnston C, Campbell-Yeo M, Fernandes A, et al. Skin-to-skin care for procedural pain in neonates. Cochrane Database Syst Rev. 2014;1:CD008435.
437.Carbasse A, Kracher S, Hausser M, et al. Safety and effectiveness of skin- to-skin contact in the NICU to support neurodevelopment in vulnerable preterm infants. J Perinat Neonatal Nurs. 2013;27:255–62.
438.Maastrup R, Greisen G, et al. Extremely preterm infants tolerate skin-to-skin contact during the first weeks of life. Acta Paediatr. 2010;99:1145–9.
439.Nyqvist KH, Anderson GC, Bergman N, et al. State of the art and recommendations. Kangaroo mother care: application in a high-tech environment. Breastfeed Rev. 2010;18:21–8.
440.Underwood MA. Human milk for the premature infant. Pediatr Clin North Am. 2013;60:189–207.
441.Lamport L, Weinberger B, Maffei D. Human Milk Fortifier After Neonatal Intensive Care Unit Discharge Improves Human Milk Usage Rates for Preterm Infants. J Nutr. 2024;154:610–616.
442.Tomlinson C, Haiek LN. Breastfeeding and human milk in the NICU: From birth to discharge. Paediatr Child Health. 2023;28:510–526.
443.Jiang X, Ding L, Wu N, et al. Longitudinal studies on breastfeeding among preterm infants: a scoping review. BMC Pregnancy Childbirth. 2025;25:738.
444.Aljawad B, Miraj SA, Alameri F, Alzayer H. Family-centered care in neonatal and pediatric critical care units: a scoping review of interventions, barriers, and facilitators. BMC Pediatr. 2025;25:291.
445.Hansen K, Gladdis T, Kukora S. Parental mental health & well-being in the NICU: Addressing the surgeon general’s advisory. Semin Perinatol. 2025;49:152111.
446.Lester BM, Hawes K, Abar B, et al. Single-family room care and neurobehavioral and medical outcomes in preterm infants. Pediatrics. 2014;134:754–60.
447.Pillai Riddell R, Racine N, Turcotte K, et al. Nonpharmacological management of procedural pain in infants and young children: an abridged Cochrane review. Pain Res Manag. 2011;16:321–30.
448.Shah PS, Herbozo C, Aliwalas LL, et al. Breastfeeding or breast milk for procedural pain in neonates. Cochrane Database Syst Rev. 2012;12:CD004950.
449.Stevens B, Yamada J, Lee GY, et al. Sucrose for analgesia in newborn infants undergoing painful procedures. Cochrane Database Syst Rev. 2013;1:CD001069.
450.Liaw JJ, Yang L, Lee CM, et al. Effects of combined use of non-nutritive sucking, oral sucrose, and facilitated tucking on infant behavioural states across heel-stick procedures: a prospective, randomised controlled trial. Int J Nurs Stud. 2013;50:883–94.
451.Bueno M, Yamada J, Harrison D, et al. A systematic review and meta- analyses of nonsucrose sweet solutions for pain relief in neonates. Pain Res Manag. 2013;18:153–61.